
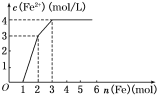
【题目】某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如图所示,则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为____,按反应的先后顺序写出该过程的离子反应方程式:___________。
【答案】1:1:4 Fe+4H++NO3-= Fe3++NO↑+2H2O 2 Fe3++ Fe=3 Fe2+ Cu 2++ Fe=Fe2++Cu
【解析】
氧化性顺序为HNO3>Fe (NO3) 3>Cu (NO3) 2,加入铁后,铁依次发生氧化还原反应,根据发生的反应结合图像分析解答。
稀溶液中各物质的氧化性顺序为HNO3>Fe(NO3)3>Cu(NO3) 2,加入铁后会依次发生氧化还原反应,①Fe+4H++NO3-= Fe3++NO↑+2H2O;②Fe+2Fe3+=3Fe2+;③Fe+Cu2+=Cu+Fe2+;从图像中可知铁为1mol时,无Fe2+生成,发生的反应①,消耗硝酸为4mol,生成Fe3+1mol;再加入1mol铁发生反应②,生成Fe2+物质的量为3mol,反应的Fe3+物质的量为2mol,其中原溶液中的Fe3+物质的量1mol;再加入1mol铁发生反应③,此时又生成Fe2+1mol,说明原溶液中Cu2+物质的量为1mol;综上所述可知原溶液中Fe (NO3) 3为1mol,Cu (NO3) 2物质的量为1mol,HNO3物质的量为4mol,稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为1∶1∶4,故答案为:1∶1∶4;Fe+4H++NO3-= Fe3++NO↑+2H2O;Fe+2Fe3+=3Fe2+;Fe+Cu2+=Cu+Fe2+。


科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是
A. 用NaNO2氧化酸性溶液中的KI:2I— + NO2—+ 2H+ = I2 + NO↑+ H2O
B. 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4+ + OH— ![]() NH3 ↑+ H2O
NH3 ↑+ H2O
C. 将过量SO2通入冷氨水中:SO2 + NH3·H2O = HSO3- + NH4+
D. 用稀硝酸洗涤试管内壁的银镜:Ag + 4H+ + NO3—= Ag+ + NO↑+ 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某镁燃料电池以镁片、石墨作为电极,电池反应为:Mg+H2O2+ H2SO4=MgSO4 +2H2O。 电池工作时,下列说法正确的是
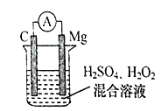
A.镁片的质量减小
B.镁片是电池的正极
C.电子由镁片 经导线流向石墨棒
D.镁片上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态 Cl原子核外电子排布式为__________________________,P、S、Cl的第一电离能由大到小顺序为____________________,P、S、Cl的电负性由大到小顺序为_______________。
(2)SCl2分子中的中心原子杂化轨道类型是_____________,该分子构型为__________。
(3)Ni与CO能形成配合物Ni(CO)4,该分子中配位键个数为_______;以“—”表示σ键、“→”表示配位键,写出CO分子的结构式__________。
(4)已知MgO与NiO的晶体结构(如图1)相同, 其中Mg2+和Ni2+的离子半径分别为66 pm和69pm。则熔点:MgO_____NiO(填“>”、“<”或“=”),理由是_______________________________。
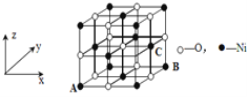
(5)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_______。
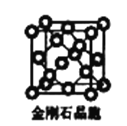
(6)金刚石晶胞含有____个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= ______a,列式表示碳原子在晶胞中的空间占有率____(请用r和a表示不要求计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )


A. 图①中ΔH1=ΔH2+ΔH3
B. 图②在催化剂条件下,反应的活化能等于E1+E2
C. 图③表示醋酸溶液滴定 NaOH溶液和氨水混合溶液的电导率变化曲线
D. 图④可表示由CO(g)生成CO2(g)的过程中要放出566 kJ 热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用Na2CO3和NaHCO3溶液进行如图所示实验。下列说法中,正确的是
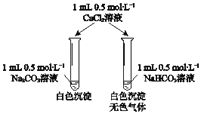
A. 实验前两溶液的pH相等 B. 实验前两溶液中离子种类完全相同
C. 加入CaCl2溶液后生成的沉淀一样多 D. 反应的离子方程式都是CO32-+Ca2+═CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向20 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
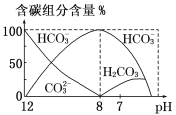
下列说法正确的是
A. 在同一溶液中,H2CO3、HCO3—、CO32—不能大量共存
B. 当pH=7时,溶液中各种离子(CO32—除外)的物质的量浓度的大小关系为:c(Cl-)>c(Na+)>c(HCO3-)>c(H+)=c(OH-)
C. 0.1 mol/L Na2CO3溶液中c(OH-)-c(H+)=c(H2CO3)+c(HCO3-)
D. 当 pH=8时,NaHCO3溶液的物质的量浓度为0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于2SO2(g)+O2(g) 2SO3(g),ΔH<0,根据下图,下列说法错误的是( )

A.t2时使用了催化剂B.t3时采取减小反应体系压强的措施
C.t5时采取升温的措施D.反应在t6时刻,SO3体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )

A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com