
【题目】铜元素在化合物中其化合价可以呈现![]() 、
、![]() 价。
价。![]() 和
和![]() 是常见的
是常见的![]() 价铜的化合物,
价铜的化合物,![]() 是较为常见的
是较为常见的![]() 价铜的化合物。
价铜的化合物。
(1)铜元素位于周期表的_______区。属于________族。
(2)请写出![]() 的电子排布式__________________,S的价层电子排布图______________
的电子排布式__________________,S的价层电子排布图______________
(3)向![]() 溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式__________________。比较
溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式__________________。比较![]() 和
和![]() 中
中![]() 中键角的大小:
中键角的大小:![]() ___________
___________![]() (填“
(填“![]() ” “
” “![]() ” 或“=”)。
” 或“=”)。
(4)![]() 中阴离子的空间构型为_______
中阴离子的空间构型为_______
(5)![]() 的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
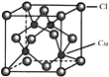
①每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为________________。
②若以铜原子为顶点构成晶胞,面心原子为________(Cu、Cl)
【答案】ds IB 1s22s22p63s23p6 3d10 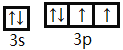 [Cu(NH3)4]SO4H2O < 平面三角形 4 Cu
[Cu(NH3)4]SO4H2O < 平面三角形 4 Cu
【解析】
(1)铜为29号元素,据此书写铜原子的电子排布式,并判断在周期表中的位置;
(2) 根据铜原子的电子排布式书写![]() 的电子排布式;S是16号元素,结合电子排布式书写价层电子排布图;
的电子排布式;S是16号元素,结合电子排布式书写价层电子排布图;
(3))[Cu(NH3)4]SO4在乙醇中的溶解度小于在水中的溶解度,向溶液中加入乙醇后会析出蓝色晶体[Cu(NH3)4]SO4H2O;NH3中N原子含有3个共价键和1个孤电子对,[Cu(NH3)2]+中N原子形成4个共价键,孤电子对和成键电子对之间的排斥力大于成键电子对之间的排斥力;
(4)根据价层电子对个数=σ键个数+孤电子对个数分析判断NO3-的空间构型;
(5)①晶胞中Cu原子数与Cl原子数为1∶1,故配位数相等,根据Cu原子与周围4个Cl原子形成正四面体,Cu的配位数为4解答;
②晶胞中Cu原子与Cl原子的数目相等,在图示晶胞中C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心,若以铜原子为顶点构成晶胞,则Cu和C1原子位置互换,据此解答。
(1)铜为29号元素,电子排布式为1s22s22p63s23p6 3d104s1,位于周期表的ds区。属于IB族元素,故答案为:ds;IB;
(2) 铜为29号元素,电子排布式为1s22s22p63s23p6 3d104s1,则![]() 的电子排布式为1s22s22p63s23p6 3d10,S是16号元素,电子排布式为1s22s22p63s23p4,价层电子排布图为
的电子排布式为1s22s22p63s23p6 3d10,S是16号元素,电子排布式为1s22s22p63s23p4,价层电子排布图为 ,故答案为:1s22s22p63s23p6 3d10;
,故答案为:1s22s22p63s23p6 3d10; ;
;
(3) 向![]() 溶液中滴加氨水,可以得到深蓝色的溶液,再向深蓝色透明溶液加入乙醇,由于[Cu(NH3)4]SO4在乙醇中的溶解度小于在水中的溶解度,所以会析出深蓝色的晶体:Cu(NH3)4SO4H2O;NH3中N原子含有3个共价键和1个孤电子对,[Cu(NH3)2]+中N原子形成4个共价键,孤电子对和成键电子对之间的排斥力大于成键电子对之间的排斥力,NH3与Cu+形成配位键,N-H键斥力减小,键角增大或NH3分子内存在孤电子对,孤电子对与共用电子对之间的斥力更大,所以NH3的键角更小,故答案为:Cu(NH3)4SO4H2O;<;
溶液中滴加氨水,可以得到深蓝色的溶液,再向深蓝色透明溶液加入乙醇,由于[Cu(NH3)4]SO4在乙醇中的溶解度小于在水中的溶解度,所以会析出深蓝色的晶体:Cu(NH3)4SO4H2O;NH3中N原子含有3个共价键和1个孤电子对,[Cu(NH3)2]+中N原子形成4个共价键,孤电子对和成键电子对之间的排斥力大于成键电子对之间的排斥力,NH3与Cu+形成配位键,N-H键斥力减小,键角增大或NH3分子内存在孤电子对,孤电子对与共用电子对之间的斥力更大,所以NH3的键角更小,故答案为:Cu(NH3)4SO4H2O;<;
(4)NO3-中N原子孤电子对数=![]() =0,价层电子对数=3+0=3,离子空间构型为平面三角形,故答案为:平面三角形;
=0,价层电子对数=3+0=3,离子空间构型为平面三角形,故答案为:平面三角形;
(5)①晶胞中Cu原子数目为4,由化学式可知晶胞中Cl原子数目也是4,二者原子数目为1∶1,故配位数也相等,Cu原子与周围4个Cl原子形成正四面体,Cu的配位数为4,故Cl原子配位数也是4,即每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为4,故答案为:4;
②根据①的分析,晶胞中Cu原子数目为4,由化学式可知晶胞中Cl原子数目也是4,二者原子数目为1∶1,在题示晶胞中C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心,若以铜原子为顶点构成晶胞,则Cu原子位于立方体的顶点和面心,C1原子位于Cu原子构成的四面体体心,故答案为:Cu。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】T℃时,在一固定容积的密闭容器中发生反应:A(g)+B(g)![]() C(s)△H<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
C(s)△H<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是

A. T℃时,该反应的平衡常数值为4
B. c点没有达到平衡,此时反应向逆向进行
C. 若c点为平衡点,则此时容器内的温度高于T℃
D. T℃时,直线cd上的点均为平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列9种物质:①氯气;②二氧化硫;③稀硫酸;④铁;⑤BaCl2固体;⑥氢氧化钾;⑦KNO3溶液;⑧酒精(C2H5OH);⑨氧化钙,请将上述物质按要求完成下列问题:
(1)用相应化学式填写下列空白:属于酸性氧化物的有_____________,属于碱性氧化物的有____________,属于电解质的是______,属于非电解质的是_______。(用序号填空)
(2)写出NaHCO3电离方程式:______
(3)用双线桥表示Cl2与二氧化硫的反应________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A. 溶液中![]() 不变
不变
B. 溶液中导电粒子的数目减少
C. 醋酸的电离程度增大,c(H+)也增大
D. 再加入10 mL pH=11的NaOH溶液后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,非金属元素被还原的是( )
A. MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2OB. H2+CuO
MnCl2+Cl2↑+2H2OB. H2+CuO![]() Cu+H2O
Cu+H2O
C. 2FeCl2+Cl2===2FeCl3D. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A. 常温下,0.1 mol·L一1的碳酸钠溶液中含有的阴离子数大于0.1NA
B. 标准状况下,33.6 mL氯气通人足量水中发生反应,转移电子数为1.5×10-3NA
C. 常温常压下,28 g由C3H6和C4H8组成的混合气体中含共用电子对数目为6NA
D. 同温下,pH=1体积为1 L的硫酸溶液所含氢离子数与pH=13体积为1 L的氢氧化钠溶液所含氢氧根离子数均为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度时,N2与H2反应过程中能量变化的曲线如图,其中a表示不使用催化剂时的能量变化曲线,b表示使用催化剂时的能量变化曲线。下列叙述正确的是

A. 状态M和N均表示2molN(g)+6mol H(g)
B. 该反应的热化学方程式为:N2+3H2![]() 2NH3 △H=-92kJ·mol-l
2NH3 △H=-92kJ·mol-l
C. 使用催化剂,降低了反应进行所需的最低能量,增大了反应放出的能量
D. 使用催化剂,并不能改变反应的△H
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(加试题)
(一)以一氯代乙酸钠(CH2ClCOONa)水溶液为原料,通过电解法可以制备1,2-二氯乙烷(CH2ClCH2Cl),装置如图1所示。
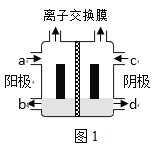
(1)所用的离子交换膜是___(填“阳”或“阴”)离子交换膜。
(2)写出电解池总反应___。
(二)1940年,我国著名化工专家侯德榜先生成功冲破了“索尔维”法的技术封锁,并加以改进,用NaCl固体代替生石灰,加入母液,并联合合成氨厂一起生产出纯碱和氯化铵。这便是举世闻名的“侯氏联合制碱法”,工艺流程如图2。
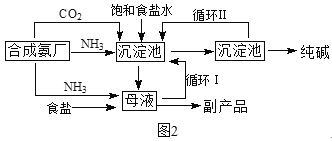
请回答:
(1)关于合成氨反应,下列说法合理的是___。
A.反应体系中一般用V2O5作催化剂
B.因为该反应ΔS小于零,所以反应的ΔH一定也小于零
C.因为该反应的ΔS小于零,所以反应的压强控制越高越好
D.该反应往往控制在500℃左右,是因为该温度下反应物转化率最高
(2)一定温度下合成氨反应的平衡常数K=48。若在该温度下,在9L的恒容容器中投入1mol氮气和3mol氢气进行反应,则氨气的平衡产率y=___;若氮气和氢气的物质的量之比为n∶1,相应平衡体系中氨气的物质的量分数为x,请在图3中绘制x随n变化的示意图(计算时不计副反应)。______
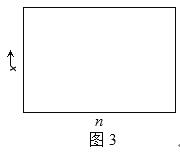
(3)侯氏制碱法最大的优点是使原料氯化钠的利用率从70%提高到90%以上,主要是设计了____(填上述编号)的循环。
(4)关于侯氏联合制碱法,下列说法合理的是_____。
A.往沉淀池中先通入CO2再通入氨气的目的是提高NaHCO3的产量
B.往母液中加入食盐的目的是使NaHCO3更多地析出
C.从母液中经过循环Ⅰ进入沉淀池的主要是Na2CO3、NH4Cl和氨水
D.往母液中通氨气目的仅仅是增大NH4+的浓度,使NH4Cl更多地析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中央电视台报道联华超市在售的某品牌鸡蛋为“橡皮弹”,专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚所致。其结构简式如图:下列说法不正确的是( )
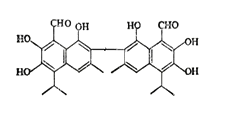
A. 该化合物的分子式为:C30H30O8
B. 1mol棉酚最多可与10mol H2加成,与6molNaOH反应
C. 在一定条件下,可与乙酸反应生成酯类物质
D. 该物质可以使酸性高锰酸钾溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com