
运用元素周期律分析下面的推断,其中错误的是( )
A.锗单质是一种优良的半导体材料 B.砹化银不溶于水也不溶于稀硝酸
C.硫酸镭是难溶于水的白色固体 D.硒化氢是无色、有毒、比硫化氢稳定的气体
科目:高中化学 来源: 题型:
(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为__________。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为__________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为____________。
(4)相同条件下,体积比为a∶b和质量比为a∶b的H2和O2的混合气体,其平均相对分子质量分别是____________和____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知34Se、35Br位于同一周期,下列关系正确的是
A.热稳定性:HCl>H2Se>HBr B.还原性:Se2->S2->Cl-
C.原子半径:Se>Cl>P D.酸性:H2SeO4>H2SO4>H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:常温下,0.01 mol/L MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,这项研究曾获2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是( )
A.13C与15N有相同的中子数 B.13C与C60互为同素异形体
C.15N 与14N 互为同位素 D.15N的核外电子数与中子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于粒子结构的描述不正确的是( )
A.H2S和NH3价电子总数均是8
B.次氯酸分子的结构式为:H—Cl—O
C.HS-和HCl均是含一个极性键的18电子粒子
D.1 mol D216O中含中子、质子、电子各10 NA(NA代表阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)如上面右图所示的原电池装置,Cu电极反应式为 ;当导线上通过2.408×1022个电子时,锌片质量减少______g。
(2)氢氧燃料电池不仅能量转化率高,而且产物是水,属于环境友好电池,总反应方程式为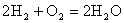 。其中氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,消耗标准状况下H2的体积是________L。
。其中氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,消耗标准状况下H2的体积是________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g) + 3H2(g) 2NH3(g) △H=-92.4 kJ/mol。
2NH3(g) △H=-92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是( )
A.放出热量关系:a < b < 92.4
B.三个容器内反应的平衡常数:③ > ① > ②
C.平衡时氨气的体积分数:① > ③
D.N2的转化率:② > ① > ③
查看答案和解析>>
科目:高中化学 来源: 题型:
酚酞是常用的酸碱指示剂,结构简式如图所示:下列关于酚酞的说法错误的是( )
A.酚酞与水可以形成氢键 
B.酚酞的分子式为C20H14O4
C.酚酞结构中含有羟基(—OH),故酚酞属于醇
D.酚酞在一定条件下能够发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com