
【题目】在一定温度下,向a L密闭容器中加入1molX气体和2 molY气体,发生如下反应:X(g) + 2Y(g)![]() 2Z(g) 此反应达到平衡的标志是( )
2Z(g) 此反应达到平衡的标志是( )
A.正反应和逆反应的速率都为零
B.容器内各物质的浓度不随时间变化
C.容器内X、Y、Z的浓度之比为1∶2∶2
D.单位时间消耗0.1molX同时生成0.2molZ
科目:高中化学 来源: 题型:
【题目】N2与H2反应生成NH3的过程中能量变化曲线如图所示。若在一个固定容积的密闭容器中充入1 mol N2和3 mol H2,使反应N2+3H2![]() 2NH3达到平衡,测得反应放出热量为Q1。
2NH3达到平衡,测得反应放出热量为Q1。
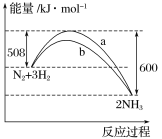
(1)该反应的热化学方程式为__________________________。
(2)Q1________92 kJ(填“>”“<”或“=”)。
(3)曲线a和曲线b中,加了催化剂的是________。
(4)上述反应达到平衡后,升高温度H2的转化率________(填“增大”“不变”或“减小”)。
(5)在温度体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则2Q1与Q2的关系为: Q2 ______2Q1(“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
A. 该溶液的pH=4 B. 升高温度,溶液的pH增大 C. 此酸的电离平衡常数约为1×10-7 D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述正确的是( )
A.碳酸比苯酚酸性强:2C6H5ONa+CO2+H2O=2C6H5OH+Na2CO3
B.实验室用氯化铝溶液和氨水制备氢氧化铝:Al3++3OH-=Al(OH)3↓
C.工业上用电解法制镁:MgCl2(熔融)![]() Mg+Cl2↑
Mg+Cl2↑
D.向NaOH溶液中通入过量的二氧化硫:SO2+2NaOH=Na2SO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2(g)+O2(g) ![]() 2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L,当反应达平衡时,可能存在的数据是
2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.4mol/L、0.2mol/L、0.4mol/L,当反应达平衡时,可能存在的数据是
A. SO2为0.8mol/L,O2为0.4mol/L
B. SO2为0.5mol/L
C. SO3为0.8mol/L
D. SO2、SO3一定均为0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生如下反应:COCl2(g)![]() CO(g)+Cl2(g) △H<0下列有关说法正确的是
CO(g)+Cl2(g) △H<0下列有关说法正确的是
A.单位时间内生成CO和Cl2的物质的量比为1∶1时,反应达到平衡状态
B.用催化剂能提高反应物的平衡转化率
C.平衡时其他条件不变,升高温度能提高COCl2的转化率
D.当反应达平衡时,恒温恒压条件下通入Ar能提高COCl2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿德罗常数。下列说法正确的是( )
A.2L1mol/LNH4Cl溶液含NH4+和Cl-均为2NA
B.在常温常压下,22g二氧化碳含有共有电子对总数为2NA
C.0.1molOH-的质子数与0.1molH2O的电子数均为NA
D.在标准状况下,11.2L辛烷中的碳原子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。

请参照下表给出的数据填空。
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Cu2+ | 4.7 | 6.7 |
Fe2+ | 7.0 | 9.0 |
Fe3+ | 1.9 | 3.7 |
(1)操作I加入X的目的是_________________。
(2)下列物质都可以作为X,适合本实验的X物质可以是(填选项)_________ 。
A、KMnO4 B、NaClO C、H2O2 D、Cl2
(3)操作II的Y试剂为____________(填化学式),并调节溶液的pH在______范围。
(4)实验室在配制CuCl2溶液时需加入少许_________(填物质名称),理由是(文字叙述并用有关离子方程式表示)_________________ __________。
(5)若将CuCl2溶液蒸干灼烧,得到的固体是_________________(填化学式);若要得无水CuCl2,请简述操作方法_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按图所示的装置进行电解实验 下列说法正确的是 ( )
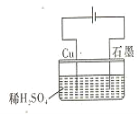
A.电解过程中,铜电极上有H2产生
B.电解初期,总反应方程式为:Cu+H2SO4 ![]() CuSO4+H2
CuSO4+H2
C.电解一段时间后,石墨电极上有O2产生
D.整个电解过程中,H+的浓度不断增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com