
����Ŀ��N2��H2��Ӧ����NH3�Ĺ����������仯������ͼ��ʾ������һ���̶��ݻ����ܱ������г���1 mol N2��3 mol H2��ʹ��ӦN2��3H2![]() 2NH3�ﵽƽ�⣬��÷�Ӧ�ų�����ΪQ1��
2NH3�ﵽƽ�⣬��÷�Ӧ�ų�����ΪQ1��
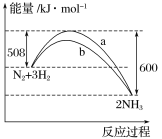
(1)�÷�Ӧ���Ȼ�ѧ����ʽΪ__________________________��
(2)Q1________92 kJ(���������������)��
(3)����a������b�У����˴�������________��
(4)������Ӧ�ﵽƽ��������¶�H2��ת����________(��������䡱��С��)��
(5)���¶����һ���������£���ͨ��2 mol N2��6 mol H2��Ӧ��ų�������ΪQ2 kJ����2Q1��Q2�Ĺ�ϵΪ: Q2 ______2Q1(��>������=������<��)��
���𰸡�N2(g)��3H2(g) ![]() 2NH3(g)����H= ��92 kJ��mol��1 �� ����b ��С >
2NH3(g)����H= ��92 kJ��mol��1 �� ����b ��С >
��������
(1)�÷�Ӧ����H= ��Ӧ���� ���������ܣ�����ʱ䣬��д�Ȼ�ѧ����ʽ��
(2)��Ϊ�÷�Ӧ�ǿ��淴Ӧ��1mol������ַ�Ӧ������������ȫ��Ӧ�꣬�ų������١�
(3)����b�ǽ����˷�Ӧ��ܡ�
(4)�����¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����������ƶ������ɵõ��𰸡�
(5)������Ϊ������ͬ��������װ1 mol N2��3 mol H2��Ӧ���ų�������Ϊ2Q1���ټ�ѹ��Ϊһ��������ƽ�������ƶ����ַ�Ӧ�ų����������ɵõ��𰸡�
(1)�÷�Ӧ����H= 508 kJ��mol��1��600 kJ��mol��1=��92 kJ��mol��1������Ȼ�ѧ����ʽΪN2(g)��3H2(g) ![]() 2NH3(g) ��H= ��92 kJ��mol��1���ʴ�Ϊ��N2(g)��3H2(g)
2NH3(g) ��H= ��92 kJ��mol��1���ʴ�Ϊ��N2(g)��3H2(g) ![]() 2NH3(g) ��H= ��92 kJ��mol��1��
2NH3(g) ��H= ��92 kJ��mol��1��
(2)��Ϊ�÷�Ӧ�ǿ��淴Ӧ��1mol������Ӧ����ȫ����˷ų�������Q1��92 kJ���ʴ�Ϊ������
(3)����b�ǽ����˷�Ӧ��ܣ����Ϊ���˴��������˴�����������b���ʴ�Ϊ������b��
(4)������Ӧ�ﵽƽ��������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����������ƶ���H2��ת���ʼ�С���ʴ�Ϊ����С��
(5)���¶����һ���������£���ͨ��2 mol N2��6 mol H2��Ӧ��ų�������ΪQ2 kJ������������Ϊ������ͬ��������װ1 mol N2��3 mol H2��Ӧ���ų�������Ϊ2Q1���ټ�ѹ��Ϊһ��������ƽ�������ƶ����ַ�Ӧ�ų����������2Q1��Q2�Ĺ�ϵΪ: Q2 >2Q1���ʴ�Ϊ��>��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л��� X(C4H6O5)�㷺����������ˮ���ڣ��������ѡ����ϡ�ɽ����Ϊ�࣬X ��̼���ṹ��֧��������ʽΪ C4H6O5��1.34gX ������������Һ��Ӧ�����ɱ�״���µ����� 0.336L��X�봼��������Ũ H2SO4 �ͼ��ȵ������¾���������ζ�IJ��X ��һ�������¿ɷ�����Ӧ����A��A![]() B
B![]() C(X��A��B��C ������̼ԭ����Ŀ��ͬ)�������й�˵���в���ȷ����( )
C(X��A��B��C ������̼ԭ����Ŀ��ͬ)�������й�˵���в���ȷ����( )
A.X �Ľṹ��ʽΪ HOOC��CHOH��CH2��COOH
B.A �ķ���ʽΪ C4H4O4
C.�� X�Ĺ��������ࡢ������ȫ��ͬ��ͬ���칹�廹�� 3 ��
D.C ����������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѡ���У�����ָ����Ŀ����Ŀǰ����ȵ��� �� ��
A.��������17gOH����1mol��OH
B.˫����Ŀ��1mol![]() ��4mol C2H4
��4mol C2H4
C.�����������³�ѹ��16g������4g����
D.������������72gCaO2��62g Na2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼͼ���У�������Ϊ����������ʵ�����������Ϊ����Һ�м��뷴Ӧ������ʵ���������Ӧ��ͼ������루1������4����Ӧ����
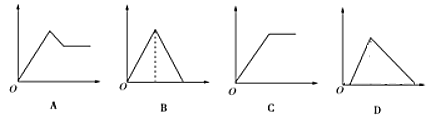
��Һ | �������� | ��Ӧ��ͼ�� |
��1������ʯ��ˮ | ͨ����CO2���� | ____ |
��2���Ȼ�����Һ | ���������ˮ | ____ |
��3��MgCl2��AlCl3�Ļ��Һ | ��μ���NaOH��Һ������ | ____ |
��4��������NaOH��NaAlO2��Һ | ��μ���ϡ���� | ____ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ� ��
A.14g��C2H4��N2��ɵĻ��������������������һ��Ϊ7.5NA
B.1molP4S3�� ��������P��S������ĿΪ9NA
��������P��S������ĿΪ9NA
C.1L0.1mol��L-1NaHSO3��Һ�����������ӵ���������0.1NA
D.11.2LCl2�����������ڹ��������·�Ӧ����HCl���ӵ�����Ϊ0.5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н���ʵ����̻���ʵ�ķ�Ӧ����ʽ����ȷ����
A. �����ռ�ʱ������ʹ����ͨʯӢ������SiO2+2NaOH![]() Na2SiO3+H2O
Na2SiO3+H2O
B. �ں����ҵĽ���Һ(����I-)�еμ�H2O2�õ�I2:2I-+ H2O2+2H+= I2+O2��+2H2O
C. ���ȵ���˿��ˮ�Ӵ��������γ�����ɫ�����ɫ�������㣺3Fe+ 4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
D. ��84����Һ������Ч�ɷ�NaClO�����������������Ҫ�ɷ����ᣩ���ʹ�÷ų�������ClO-+ Cl-+ 2H+= Cl2��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ѧϰ��ѧ����Ҫ���ߡ�����������ʾ���ʱ仯�Ļ�ѧ�����У�������ǣ� ��
A.������ʴʱ���ܷ�����������Ӧ��2H2O + O2+ 4e-= 4OH-
B.��ʾH2ȼ���ȵ��Ȼ�ѧ����ʽ��2H2��g��+O2��g��=2H2O��g������H=-483.6kJ/mol
C.����ˮ������ӷ���ʽ��CO32-+H2O![]() HCO3-+ OH-
HCO3-+ OH-
D.Ca(HCO3)2��Һ�м����������ʯ��ˮ��Ca2++HCO3��+OH��=CaCO3��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ѧϰ��ѧ����Ҫ���ߡ�����������ʾ���ʱ仯�Ļ�ѧ��������ȷ���ǣ� ��
A.K37ClO3��ŨHCl�ڼ�������������Cl2�Ļ�ѧ����ʽ: K37ClO3+6HCl=K37Cl+3Cl2��+3H2O
B.��ʾH2ȼ���ȵ��Ȼ�ѧ����ʽ: H2��g��+![]() O2��g��=H2O��g����H= -241��8kJ/mol
O2��g��=H2O��g����H= -241��8kJ/mol
C.��1~2mLFeCl3������Һ���뵽20ml��ˮ�������������ӷ���ʽ:Fe3++3H2O ![]() Fe��OH�� 3�����壩+3H+
Fe��OH�� 3�����壩+3H+
D.��Ba��OH�� 2��Һ�е�����������������: Ba2++OH-+H++SO42-=BaSO4��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���a L�ܱ������м���1molX�����2 molY���壬�������·�Ӧ��X(g) + 2Y(g)![]() 2Z(g) �˷�Ӧ�ﵽƽ��ı�־�ǣ� ��
2Z(g) �˷�Ӧ�ﵽƽ��ı�־�ǣ� ��
A.����Ӧ���淴Ӧ�����ʶ�Ϊ��
B.�����ڸ����ʵ�Ũ�Ȳ���ʱ��仯
C.������X��Y��Z��Ũ��֮��Ϊ1��2��2
D.��λʱ������0.1molXͬʱ����0.2molZ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com