
【题目】有两个相同带活塞的容器,向容器a中充入NO2(g)待颜色不再变化,再向容器b中充入溴蒸汽,使两容器的颜色和体积相等〔注意:同浓度的NO2和Br2蒸汽颜色相同,2NO2(g)![]() N2O4(g)(无色),迅速将两容器同时压缩(假设气体不液化),下列说法正确的是
N2O4(g)(无色),迅速将两容器同时压缩(假设气体不液化),下列说法正确的是
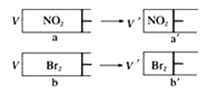
A.a→a′过程中,颜色突然加深,然后逐渐变浅,最终颜色比原来的浅
B.若对a和b以极慢的速度缓缓压缩,则a和b的颜色均慢慢加深,但在每一个相同的时间点,b的颜色总比a的深
C.假设容器和活塞均为无色,从容器左侧观察a和a′,a′的颜色比a浅
D.气体的物质的量:na一定大于nb′
【答案】B
【解析】
a→a′过程中,增大压强,2NO2N2O4平衡正向移动,有一定量的NO2转化成N2O4,但是新平衡时各气体物质的浓度均比旧平衡时大;b→b′过程中,溴蒸汽的物质的量不变,浓度增大,
A. a→a′过程中,开始时容器的容积瞬间减小,NO2的浓度瞬间增大,则颜色突然加深,2NO2N2O4平衡正向移动,NO2的浓度逐渐减小,则颜色又逐渐变浅,但是新平衡时各气体物质的浓度均比旧平衡时大,则最终颜色比原来的深,故A错误;
B. 在以极慢的速度缓缓压缩的过程中,a中2NO2N2O4平衡正向移动,有一定量的NO2转化成N2O4,而b→b′过程中,溴蒸汽的物质的量不变,但在每一个相同的时间点,溴蒸汽的浓度总是比NO2的浓度大,故b的颜色总比a的深,故B正确;
C. 由A项分析知,从容器左侧观察a和a′,a′的颜色更深,故C错误;
D. 起始时,两容器中气体的浓度和体积相等,即气体物质的量相等,b→b′过程中,溴蒸汽的物质的量不变,故气体的物质的量:na等于nb′,故D错误;
故选B。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
【题目】下列有关化学用语正确的是( )
A. 某元素基态原子的电子排布图![]()
B. NH4Cl电子式为[![]() :H]+Cl-
:H]+Cl-
C. Ca2+基态电子排布式为1s22s22p63s23p6
D. α羟基丙酸(乳酸)的比例模型为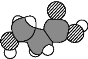
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,可用于制备丙烯、氢气等。
(1)MTO法由甲醇制备丙烯时的反应原理是:甲醇先脱水生成二甲醚,然后二甲醚与甲醇的平衡混合物脱水转化为含丙烯较多的低聚烯烃。某温度下,在密闭容器中加入CH3OH气体,发生脱水反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g),一段时间后测得各组分的浓度如表所示。
CH3OCH3(g)+H2O(g),一段时间后测得各组分的浓度如表所示。
物质 | CH3OH | CH3OCH3 | H2O |
5min浓度(mol·L-1) | 0.44 | 0.6 | 0.6 |
10min浓度mol·L-1) | 0.04 | 0.8 | 0.8 |
15min浓度(molL-1) | 0.04 | 0.8 | 0.8 |
该温度下,反应的平衡常数数值是___,CH3OH的平衡转化率是___。
(2)利用甲醇水蒸气重整制氢法是获得氢气的重要方法。反应原理如下:
反应i(主反应):CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)△H=+49kJmol-1
CO2(g)+3H2(g)△H=+49kJmol-1
反应ii(副反应):H2(g)+CO2(g)![]() CO(g)+H2O(g)△H=+41kJmol-1
CO(g)+H2O(g)△H=+41kJmol-1
①温度高于300℃则会同时发生CH3OH转化为CO和H2的副反应,该反应的热化学方程式是___。
②反应中,经常使用催化剂提高化学反应速率,但催化剂对反应具有选择性。一定条件下,测得CH3OH转化率及CO、CO2选择性随温度变化情况分别如图所示(CO、CO2的选择性:转化的CH3OH中生成CO、CO2的百分比)。

从图中可知,反应的适宜温度为___,随着温度的升高,催化剂对___(填“反应i”或“反应ii”)的选择性越低。
③TiO2纳米电极电化学还原法可将副产物CO2在酸性水溶液中电解生成甲醇,生成甲醇的电极反应式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素的单质X、Y、Z在通常状况下均为气态,并有如图转化关系(反应条件略去)。已知X、Y、Z均为双原子单质,X是空气中含量最多的气体,甲可使湿润的酚酞试纸变红,乙溶于水即得盐酸。请完成下列问题:

(1)X的电子式是_________________。
(2)写出甲和乙反应的化学方程式__________________。
(3)实验室可用如图所示的装置(缺少收集装置,夹持固定装置略去)制备并收集甲。

①在图中方框内绘出收集甲的仪器装置简图。_______________
②试管中的试剂是________________(填写化学式)。
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S催化分解过程中通入CO2、CH4会发生如下反应,下列说法不正确的是
A.CH4(g)+CO2(g)![]() 2H2(g)+2CO(g)压缩容器体积,平衡转化率将增大
2H2(g)+2CO(g)压缩容器体积,平衡转化率将增大
B.H2S(g)+CO2(g)![]() H2O(g)+COS(g)通入CO2,将促进反应的进行
H2O(g)+COS(g)通入CO2,将促进反应的进行
C.已知2H2S(g)+CH4(g)![]() 4H2(g)+CS2(g) △H>0,则该反应在高温下易自发
4H2(g)+CS2(g) △H>0,则该反应在高温下易自发
D.2H2S(g)![]() 2H2(g)+S(g) △H>0
2H2(g)+S(g) △H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图所示。
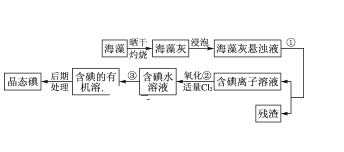
(1)指出提取碘的过程中有关的实验操作名称___、___。
(2)写出流程图中氧化②的离子反应议程式___。
(3)提取碘的过程中,可供选择的有机试剂是___。
A.酒精 B.四氯化碳 C.醋酸 D.水
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器,尚缺少的玻璃仪器是___。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出图中实验装置中的错误之处。
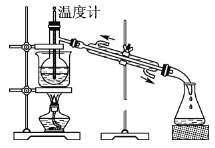
①____;
②____;
③____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一固体混合物,可能由K2CO3、NaNO2、FeCl3、KClO3、AgNO3混合而成,为检验它的成分,做了如下实验:取固体加入足量的稀硝酸中,搅拌充分反应,得到无色透明溶液,同时有黄绿色气体和白色沉淀生成![]() 已知NaNO2不能被稀硝酸氧化)。根据以上实验现象,你认为以下判断正确的是
已知NaNO2不能被稀硝酸氧化)。根据以上实验现象,你认为以下判断正确的是
A.一定含有KClO3、AgNO3、NaNO2,不能肯定是否含有氯化铁
B.一定含有KClO3,且在反应过程中被还原生成了两种还原产物
C.另取适量固体加水溶解,若出现白色沉淀,即可证明K2CO3的存在
D.将反应产生的气体通入少量澄清石灰水,若有无沉淀出现,即可证明K2CO3不存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题
(1)等pH、等体积的两份溶液A(盐酸)和B(CH3COOH)分別与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是_____(填写序号)。
①开始反应时的速率A>B ②参加反应的锌的物质的量A=B
③反应所需要的时间B>A ④A中有锌剩余
(2)已知,CH3COOH是常见的弱酸,现有常温下0.1molL-1的CH3COOH溶液。
①温度不变,加水稀释过程中,下列表达式的数据一定变小的是_____(填字母序号,下同),②若该溶液升高温度,下列表达式的数据增大的是_____。
A.c(H+) B.c(H+)·c(OH-)
C.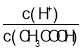 D.
D.![]()
(3)取0.10mol CH3COOH(冰醋酸)作导电性实验,测得其导电率随加入的水量变化如图所示:比较a、b点的相关性质(填“>”“<”或“=”):
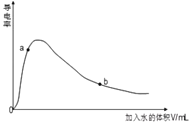
① n(H+):a_____b;
② c(CH3COO-):a_____b;
③完全中和时消耗NaOH的物质的量:a_____b;
(4)25℃时,部分物质的电离平衡常数如下表所示:
CH3COOH | H2CO3 | HCN |
1.7×10﹣5 | K1=4.3×10-7 K2=5.6×10﹣11 | 4.9×10﹣10 |
请回答下列问题:
① CH3COOH、H2CO3、HCN的酸性由强到弱的顺序为_________。
② 焦炉煤气中一般含有H2S和HCN气体,有的工厂在真空条件下,使用K2CO3溶液吸收煤气中的H2S和HCN气体,实现脱硫脱氰。请根据上述数据,尝试从理论上推测同为0.l molL-1的K2CO3溶液和HCN混合后,最可能发生的反应的离子方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4 ℃下,把质量A g摩尔质量为M g·mol-1的可溶性盐RCln 溶解在V mL水中,恰好形成该温度下的饱和溶液,密度为ρ g·cm-3,下列关系式错误的是
A. 溶质的质量分数ω=A/(A+V)×100%
B. 溶质的物质的量浓度c=1 000ρ A/(MA+MV) mol·L-1
C. 该温度下此盐的溶解度S=100A/V g
D. 1 mL该溶液中n(Cl-)=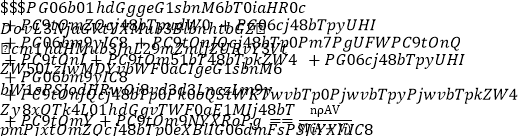 mol
mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com