
����Ŀ����.һ�������������Ժ�CO2������Ӧ:Fe(s)+CO2(g)![]() FeO(s)+CO(g)����H>0��
FeO(s)+CO(g)����H>0��
(1)���д�ʩ����ʹƽ��ʱ![]() �������____(�����)��
�������____(�����)��
A.�����¶� B.����ѹǿ C.����һ�������� D.�ټ���һЩ����
(2)��Ӧ�ﵽƽ���,�����������������ʱ,��ͨ��һ������CO2,ʹCO2��Ũ�ȳ�Ϊԭ����2��,��CO2��ת���ʽ�____(��������������С������������)��
��.��һ���¶��µ�ij�ݻ�������ܱ�������,�������л�ѧƽ��:C(s)+H2O(g)![]() CO(g)+H2(g),�Է����ͻش���������:
CO(g)+H2(g),�Է����ͻش���������:
(1)���϶��������淴Ӧ��һ���������Ѵﵽ��ѧƽ��״̬����____(ѡ�����)��
A.��ϵ��ѹǿ���ٷ����仯
B.v��(CO)=v��(H2O)
C.����n mol CO��ͬʱ����n mol H2
D.1 mol H��H�����ѵ�ͬʱ����2 mol H��O��
E.���������ܶ�
(2)���������ݻ��ɱ䣬������ѧƽ��״̬������Ӧ��ʼ����,�ﵽƽ���,��ƽ����ϵ��ѹ(��С�ݻ���������������),�������������ƽ����Է���������____(��������������С�����������)��
���𰸡� A ���� ABDE ���
��������������������ԭ����I.��1��A���˷�Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���COŨ������CO2Ũ�ȼ�С���˱�ֵ����A��ȷ��B����Ӧǰ������ϵ��֮����ȣ�����ѹǿ��ƽ�ⲻ�ƶ�����ֵ���䣬��B����C����Ӧǰ������ϵ��֮����ȣ�����Ƿ�Ӧ���壬ƽ�ⲻ�ƶ�����ֵ���䣬��C����D�������ǹ��壬Ũ����Ϊ������ƽ�ⲻ�ƶ�����ֵ���䣬��D����2��Fe��FeO�ǹ��壬CO2��CO������ϵ����ȣ����CO2Ũ�ȳ�Ϊԭ����2����ƽ�ⲻ�ƶ���CO2��ת���ʲ��䣻II.��1��A����Ӧǰ������ϵ��֮�Ͳ���ȣ����ѹǿ���䣬˵����Ӧ�ﵽƽ�⣬��A��ȷ��B���ò�ͬ���ʵĻ�ѧ��Ӧ���ʱ�ʾ�ﵽƽ�⣬��Ӧ������һ��һ�棬�һ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���B��ȷ��C������CO������H2����Ӧ����������Ӧ������У���C����D������ѡ��B�ķ�������D��ȷ��E��CΪ���壬������������������������䣬�����ܶȵĶ��壬����ܶȲ��䣬˵����Ӧ�ﵽƽ�⣬��E��ȷ����2����ΪCO��H2�����ʵ�����ȣ�����1mol�����ƽ��Ħ������Ϊ(28��2)/2g��mol��1=15g��mol��1��ˮ��Ħ������Ϊ18g��mol��1���ﵽƽ�������ѹǿ��ƽ��������Ӧ��Ӧ�ƶ�����ƽ��Ħ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����������ض�������һ���ܹ������������
A. ���н϶�Fe3+����Һ��Na+��SO42-��HS-��NH4+
B. c(OH-)=1mol/L����Һ��AlO2-��CH3COO-��K+��Ba2+
C. pH=1����Һ��K+��Fe2+��NO3-��Na+
D. ��Al�ܷų�H2����Һ��HCO3-��K+��Mg2+��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����16�֣���������G��һ�����ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫,���ķ���ʽΪC10H10O2���÷�����AΪԭ�Ϻϳ���������G��·�����£�
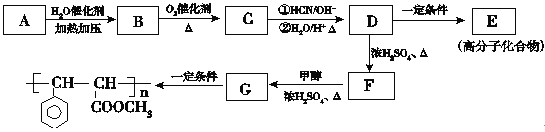
��֪��
��1��B�Ĺ����ŵ�����________��
��2��D��F�ķ�Ӧ������________��
��3�����������Ľṹ��ʽΪ_________��
��4��д��A�Ľṹ��ʽ___________��
��5��C��������Һ��Ӧ�Ļ�ѧ����ʽ________��
��6��Dת��ΪE�Ļ�ѧ����ʽ_________��
��7��д��![]() ����������������Һ��Ӧ�Ļ�ѧ����ʽ________��
����������������Һ��Ӧ�Ļ�ѧ����ʽ________��
��8��д����������������D��ͬ���칹��Ľṹ��ʽ_______��
��������������ȡ�����ұ����ϵ�һ�ȴ��������֣�
����FeCl3��Һ����ɫ
����NaOH��Һ�з�Ӧ���������3mol NaOH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���������FexO��1.52g�������������У���������Һ��ͨ���״����112mlCl2��ǡ��ȫ��ת����Fe3+��xֵΪ��
A.0.80B.0.85C.0.90D.0.93
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����14�֣���ѧʵ�鳣����ͼ��ʾװ����ȡ�����屽������ƿa��װ���Լ��DZ���������ۡ�����д���пհס�
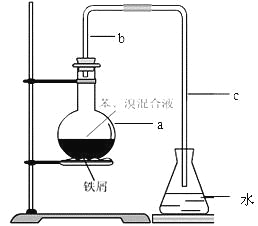
������b��������������һ�ǵ��������Ǽ��� �����ã�
��a�з�Ӧ�Ļ�ѧ����ʽΪ ��
����ʵ��õ����Ǵֱ���Ϊ�˳�ȥ���е��壬Ҫ�õ���һ�ֳ��ó��Ӳ��������� ���ᴿ�屽�ľ��岽���У�
��������ˮϴ�����ø���������10%NaOH��Һϴ����ˮϴ ��
��ȷ�IJ���˳��Ϊ�� ��
A���٢ڢۢܢ� | B���ڢܢݢۢ� | C���ܢڢۢ٢� | D���ڢܢ٢ݢ� |
��Ϊ֤�������巢������ȡ����Ӧ�����Ǽӳɷ�Ӧ������ˮ�м��� ������ʵ�鲻�����ܣ�Ϊ�˱����ڵ���a��b֮�����һʢ�� ��ϴ��ƿ��Ŀ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(ǰ����ÿ��2�֣�������ÿ��3�֣���13��)�����������ϳɰ��ǻ�ѧ��ҵ�м�Ϊ��Ҫ�ķ�Ӧ,���Ȼ�ѧ����ʽ�ɱ�ʾΪ:N2(g)+3H2(g)![]() 2NH3(g)����H=-92 kJ��mol-1����ش���������:
2NH3(g)����H=-92 kJ��mol-1����ش���������:
(1)ȡ1 mol N2(g)��3 mol H2(g)����һ�ܱ�������,�ڴ�������ʱ���з�Ӧ,��÷�Ӧ�ų�������___(����������������������С����)92 kJ,ԭ�� ��______________;���������,��H___(�������������С������������)��
(2)��֪:�ƻ�1 mol N��N����1 mol H��H����Ҫ���յ������ֱ�Ϊ:946 kJ��436 kJ,���ƻ�1 mol N��H����Ҫ���յ�����Ϊ_____kJ��
(3)N2H4����ΪNH3�����е�һ��H����NH2ȡ���IJ������������N2H4(g)Ϊȼ��,NO2Ϊ������,����N2��H2O(g)��
��֪:N2(g)+2O2(g)![]() 2NO2(g) ��H1=+67.7 kJ��mol-1
2NO2(g) ��H1=+67.7 kJ��mol-1
N2H4(g)+O2(g)![]() N2(g)+2H2O(g)��H2=-534 kJ��mol-1��
N2(g)+2H2O(g)��H2=-534 kJ��mol-1��
��:1 mol N2H4��NO2��ȫ��Ӧ���Ȼ�ѧ����ʽΪ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽���У����е��ǣ�������
A. ��ʳ�׳�ȥ��ˮƿ�е�ˮ��
B. ����������ӵ����еĵ���أ�KIO3��
C. ��Al2��SO4��3��Һ�мӹ���NaOH��Һ����Al��OH��3
D. ��ϡH2SO4��ˮ������ѿ����Һ��ֱ�Ӽ�������Cu��OH��2����Һ������ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2�Ǵ�����Ⱦ�����������Ҫԭ������ͼ��ʾװ�����Լ����չ����ŷŵķ����е�SO2���ֿ�������һ���������ᣬ����˵����ȷ����

A. a������b����
B. ��������������������������
C. �����¿��������������������һ������50%
D. ������ӦʽΪSO2��2H2O-2e-=SO42-��4H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��װ��(��)Ϊ������Fe-Ni���ɳ���أ�Fe+NiO2+2H2O![]() Fe(OH)2+Ni(OH)2��װ��(��)Ϊ���ʾ��ͼ�����պϿ���Kʱ��Y������Һ�ȱ�졣����˵����ȷ����
Fe(OH)2+Ni(OH)2��װ��(��)Ϊ���ʾ��ͼ�����պϿ���Kʱ��Y������Һ�ȱ�졣����˵����ȷ����

A. �պ�Kʱ��X�ĵ缫��ӦʽΪ��2H++2e-= H2��
B. �պ�Kʱ��A�缫��ӦʽΪ��NiO2+2e-+2H+= Ni(OH)2
C. ��װ��(��)���ʱ��B�����뷴Ӧ�����ʱ�����
D. ��װ��(��)���ʱ��OH- ͨ�������ӽ���Ĥ������A�缫
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com