
2SO2(g)+ O2(g)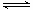 2SO3(g) △H = a kJ·mol-1,反应过程的能量变化如图所示。已知1mol
SO2(g)完全转化为1mol SO3(g)放热99 kJ。请回答:
2SO3(g) △H = a kJ·mol-1,反应过程的能量变化如图所示。已知1mol
SO2(g)完全转化为1mol SO3(g)放热99 kJ。请回答:
(1)图中A点表示_______________________,a=__________ 。
(2) Ea的大小对该反应的△H _______(填“有” 或“无”)影响。该反应常用V2O5作催化剂,加入V2O5会使图中B点_________(填“升高”、“降低”或“不变”)。
(3)已知单质硫的标准燃烧热为296kJ·mol-1,写出反应的热化学方程式:________________________ ____,常温常压下,由单质硫和氧气经两步反应,若生成1mol SO3(g),放出的总热量为___ ___ 。
(1)反应物总能量;-198;(2)无;减小;(3)S(s)+O2=SO2(g)△H=-296kJ•mol-1;-1185。
【解析】
试题分析:(1)因图中A表示反应物总能量;因1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1,所以2molSO2(g)氧化为2molSO3的△H=-198kJ•mol-1,则2SO2(g)+O2(g)=2SO3(g)△H=-198KJ•mol-1。(2)因物质的活化能的大小与反应热无关;加入催化剂能降低物质的活化能,则Ea减小。(3)因燃烧热概念要求必须是lmol物质完全燃烧,则热化学方程式为:S(s)+O2=SO2(g)△H=-296kJ•mol-1;因单质硫的燃烧热为296KJ•mol-1,则S(s)+O2(g)=SO2(g)△H=-296KJ•mol-1,而 1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1,则SO2(g)+1/2O2(g)=SO3(g)△H=-99kJ•mol-1,由盖斯定律可得:S(s)+3/2O2(g)=SO3(g)△H=-296KJ•mol-1+(-99kJ•mol-1)=-395KJ•mol-1,所以S(s)生成3molSO3(g)的△H为-395KJ•mol-1×3=-1185 KJ•mol-1。
考点:热化学方程式;吸热反应和放热反应;催化剂的作用。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (2012?淄博一模)硫及其化合物在国民生产中占有重要的地位.
(2012?淄博一模)硫及其化合物在国民生产中占有重要的地位.| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
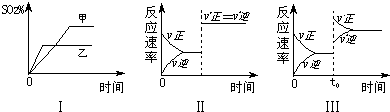
| A、图Ⅰ表示温度对化学平衡的影响,且甲的温度较高 | B、图Ⅱ表示t0时刻使用催化剂对反应速率的影响 | C、图Ⅱ表示t0时刻通入氦气对反应速率的影响 | D、图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |
查看答案和解析>>
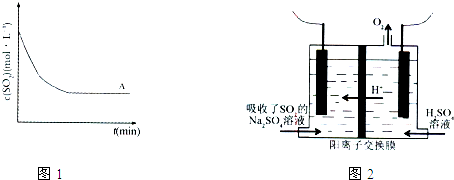
科目:高中化学 来源: 题型:阅读理解
| 方法1 | 用氨水将SO2转化为(NH4)2SO3,再氧化成(NH4)2SO4 |
| 方法2 | 用活性炭吸附法处理SO2 |
| 方法3 | 用Na2SO4溶液吸收SO2,再进行电解得到S单质 |
| t(min) 浓度(mol?L-1) |
0min | 1min | 2min | 3min | 4min | 5min | 6min |
| c(SO2) | 0.054 | 0.034 | 0.018 | 0.010 | 0.008 | 0.006 | 0.006 |
| c(O2) | 0.032 | 0.022 | 0.014 | 0.010 | 0.009 | 0.008 | 0.008 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com