
【题目】下列图示与对应的叙述相符的是

A.由图甲可以判断:若T1>T2,反应A(g)+ B(g)![]() 2C(g)的△H<0
2C(g)的△H<0
B.图乙表示压强对可逆反应2A(g)+2 B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.根据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH溶液,调节pH≈4
D.图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,溶液pH随加入盐酸体积的变化
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据下列图示所得推论正确的是
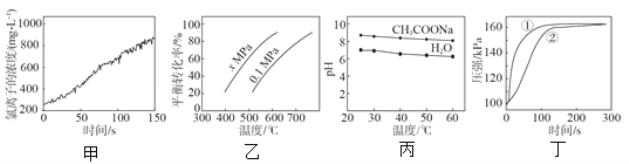
A.甲是新制氯水光照过程中氯离子浓度的变化曲线,推断次氯酸分解生成了 HCl 和 O2
B.乙是 C4H10(g)![]() C4H8(g) + H2(g)的平衡转化率与温度和压强的关系曲线,推断该反应的H>0、x>0.1
C4H8(g) + H2(g)的平衡转化率与温度和压强的关系曲线,推断该反应的H>0、x>0.1
C.丁是 0.03g 镁条分别与 2 mL 2 mol/L 盐酸和醋酸反应过程中密闭容器内气体压强随时间的变化曲线,推断①代表盐酸与镁条的反应
D.丙是 0.5 mol/L CH3COONa 溶液及水的 pH 随温度的变化曲线,说明随温度升高,CH3COONa 溶液中 c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)海水资源的利用具有广阔前景。海水中主要离子的含量如下:
成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
Cl- | 18980 | Ca2+ | 400 |
Na+ | 10560 |
| 142 |
| 2560 | Br- | 64 |
Mg2+ | 1272 |
电渗析法淡化海水示意图如图所示,其中阴(阳) 离子交换膜仅允许阴(阳)离子通过。
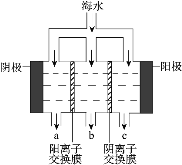
①电解氯化钠溶液的离子方程式_____。
②电解过程中阴极区碱性明显增强,用平衡移动原理 解释原因_____。 在阴极附近产生少量白色沉淀,其成分有_________和CaCO3。
③淡水的出口为_________(填“a”、“b”或“c”);a 出口物质为_____(填化学式)。
④若用下面燃料电池为电源电解 100mL1molL-1 氯化钠溶液,当电池消耗0.00025 molO2 时,常温下,所得溶液的 pH 为__________(忽略反应前后溶液体积变化)
(2)如图Ⅰ是氢氧燃料电池(电解质为 KOH 溶液)的结构示意图,
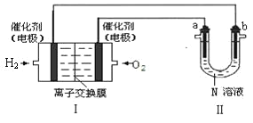
①Ⅰ中通入O2的一端为电池的_____极。 通入H2的一端的电极反应式_________
②若在Ⅱ中实现锌片上镀铜,则 b 的电极材料是_____,N 溶液为_____溶液。
③若在Ⅱ中实现 Cu+H2SO4= CuSO4+H2↑,则a 极的反应式是_____,N 溶液为 _____溶液。
(3)工业上用 Na2SO3 溶液吸收 SO2,过程中往往得到 Na2SO3 和 NaHSO3的混合溶液,溶液 pH 随 n(![]() ):n(
):n(![]() ) 变化关系如下表:
) 变化关系如下表:
n( | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
当吸收液的 pH 降至约为 6 时,送至电解槽再生。再生示意图如下,结合图示回答:

①![]() 在阳极放电的电极反应式是_____。
在阳极放电的电极反应式是_____。
②当阴极室中溶液 pH升至 8 以上时,吸收液再生并循环利用。简述再生原理:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属腐蚀与防护的说法中正确的是( )
A.牺牲阳极的阴极保护法是一种基于电解池原理的金属防护法
B.钢铁的析氢腐蚀和吸氧腐蚀的负极反应式相同
C.镀锌铁制品镀层受损后形成原电池,锌作负极,比破损前更耐腐蚀
D.将变黑后的银器(表面被氧化为Ag2S)放入盛有食盐溶液的铝质容器中,黑色褪去是因为生成了AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图象对应的叙述中,错误的是( )
A. 图A表示常温下,将铜粉加入到一定量浓硝酸中,生成气体的体积与所加铜粉的质量之间的关系
图A表示常温下,将铜粉加入到一定量浓硝酸中,生成气体的体积与所加铜粉的质量之间的关系
B.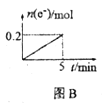 图B表示用惰性电极电解一定浓度的硫酸铜溶液,若通电5min后,加入0.1mol的氢氧化铜溶解,刚好恢复到通电前的浓度,则电解过程中转移的电子的物质的量
图B表示用惰性电极电解一定浓度的硫酸铜溶液,若通电5min后,加入0.1mol的氢氧化铜溶解,刚好恢复到通电前的浓度,则电解过程中转移的电子的物质的量
C. 图C表示在恒温恒容的密闭容器中,反应NH2COONH4(s)2NH3(g)+CO2(g)达平衡后,t1时缩小容器体积,t2时再达平衡时CO2的浓度变化
图C表示在恒温恒容的密闭容器中,反应NH2COONH4(s)2NH3(g)+CO2(g)达平衡后,t1时缩小容器体积,t2时再达平衡时CO2的浓度变化
D. 图D表示一定条件,在水溶液中1molCl-、ClOx-(x=1、2、3、4)的能量(kJ)相对大小由此可知,B→A+C反应的热化学方程式为:3ClO-(aq)=ClO3-(aq)+2Cl-(aq) △H=-117kJmol-1
图D表示一定条件,在水溶液中1molCl-、ClOx-(x=1、2、3、4)的能量(kJ)相对大小由此可知,B→A+C反应的热化学方程式为:3ClO-(aq)=ClO3-(aq)+2Cl-(aq) △H=-117kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生设计了三个实验方案,用以检验淀粉的水解产物。
方案甲:淀粉液![]() 水解液
水解液![]() 中和液
中和液![]() 溶液变蓝
溶液变蓝
结论:淀粉没有水解
方案乙:淀粉液![]() 水解液
水解液![]() 无银镜现象
无银镜现象
结论:淀粉完全没有水解
方案丙:淀粉液![]() 水解液
水解液![]() 中和液
中和液![]() 有银镜出现
有银镜出现
结论:淀粉已经水解
根据上述操作、现象,首先回答结论是否正确,然后简要说明理由。
(1)方案甲:_________;
(2)方案乙:________;
(3)方案丙:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g) △H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
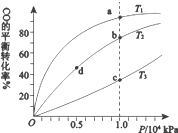
A.温度:T1>T2>T3
B.正反应速率:v(b)>v(d) v(a)>v(c)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量:M(b)>M(d) M(a)<M(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质a、b、c、d均为中学化学中的常见单质或化合物,它们之间的转化关系如右图所示(部分产物已略去),下列各组物质中,通过一步反应就能实现图示转化的是
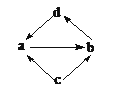
选项 | a | b | c | d |
A | SO2 | SO3 | S | H2SO4 |
B | Na2O | Na2O2 | Na | NaOH |
C | CO | CO2 | C | H2CO3 |
D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图装置制备乙烯,下列有关说法错误的是
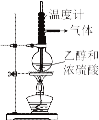
A.圆底烧瓶中应加入碎瓷片防止暴沸
B.烧瓶中应先加入乙醇,再缓慢加入浓硫酸
C.实验时,加热迅速升温至 170℃,提高乙烯的产率
D.将产生的气体直接通到溴水中,检验是否有乙烯生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com