
【题目】氨在生产生活中应用广泛。
(1) NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,工业上可通过反应:NH3(g)+Cl2(g)=NH2Cl(g) + HCl(g)制备氯胺,已知部分化学键的键能如下表所示(假定不同物质中同种化学键的键能一样), 则上述反应的H=__________kJ·mol—1
化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
键能/(kJ/mol) | a | b | c | d |
(2)氨气是重要的化工产品。目前工业合成氨的原理是: N2(g)+3H2(g) ![]() 2NH3(g)。在恒温恒压装置中进行工业合成氨反应,下列说法正确的是__________。
2NH3(g)。在恒温恒压装置中进行工业合成氨反应,下列说法正确的是__________。
a.气体压强不再变化时,表明该反应已达平衡状态
b.气体密度不再变化时,表明该反应已达平衡状态
c.平衡后,压缩容器,会生成更多NH3
d.平衡后,向装置中通入一定量Ar, 平衡不移动
(3)现向三个体积均为5L,温度分别恒定为T1、 T2、T3的恒容密闭容器I、II、 III中,分别充入1 mol N2和3 molH2发生反应: N2(g)+3H2(g) ![]() 2NH3(g) H1=-93 kJ·mol—1,当反应均进行到2min时H2的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。
2NH3(g) H1=-93 kJ·mol—1,当反应均进行到2min时H2的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。
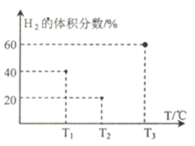
①2min时三个容器中的反应达到化学平衡状态的是_____容器.(填“I”、“II”或“III”)。
②0~2 min内容器I中用NH3表示的化学反应速率v(NH3)=____。 (保留两位有效数字)
③2 min时容器II中v正______ v逆。 (填“<”、 “>”或“=”)
④当三个容器中的反应均达到平衡状态时,平衡常数最小的是容器______(填容器序号),它的数值为____(保留两位有效数字)。
(4)氨在高温下可将一些固体金属氧化物还原为固态或液态金属单质,本身被氧化为N2。在不同温度下,氨气还原四种金属氧化物达到平衡后,气体中![]() 与温度(T)的关系如图所示。下列说法正确的是______(填字母)。
与温度(T)的关系如图所示。下列说法正确的是______(填字母)。
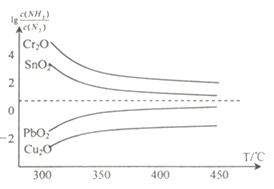
A. NH3还原PbO2的反应△H>0
B.工业冶炼这四种金属时,NH3冶炼金属铬(Cr)的还原效率最低
C.实验室还原出金属铜(Cu)时,325°C 下NH3的利用率比425°C下NH3的利用率更大
D.通过延长反应管的长度来增加金属氧化物和NH3的接触面积,可以减少尾气中NH3的量
【答案】a+b-c-d bc Ⅲ 0.064molL1min 1 > III 2.1 L2mol2 BC
【解析】
(1)反应的焓变等于反应物的键能之和减去生成物的键能之和;
(2)a.在恒温恒压装置中气体压强始终没有变化;
b.反应中,由质量守恒定律可知气体质量不变,该反应是一个气体体积减小的可逆反应,容器的体积会减小,气体密度增大;
c.该反应是一个气体体积减小的可逆反应,平衡后,压缩容器,容器的压强增大,平衡向正反应方向移动;
d.在恒温恒压装置中合成氨反应达到平衡后,向装置中通入一定量Ar,容器的压强减小,平衡向逆反应方向移动;
(3)①若未达平衡,温度越高反应速率越快,相同时间内氢气的含量越低;
②依据题意建立三段式求解可得;
③若未达平衡,温度越高反应速率越快,相同时间内氢气的含量越低,2min时,氢气的含量Ⅲ最大,则II没有达到平衡;
④合成氨反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,则当三个容器中的反应均达到平衡状态时,平衡常数最小的是容器Ⅲ,依据题意建立三段式求解可得;
(4)![]() 的值越大,说明冶炼金属的还原效率越低,NH3的利用率越大。
的值越大,说明冶炼金属的还原效率越低,NH3的利用率越大。
(1)反应的焓变等于反应物的键能之和减去生成物的键能之和,则反应的H=[3E(N-H)+E(Cl-Cl)]—[2 E(N-H)+E(N-Cl)+E(H-Cl)]=(a+b-c-d)kJ·mol—1,故答案为:a+b-c-d;
(2)a.在恒温恒压装置中气体压强始终没有变化,气体压强不再变化不能表明该反应已达平衡状态,故错误;
b.反应中,由质量守恒定律可知气体质量不变,该反应是一个气体体积减小的可逆反应,容器的体积会减小,气体密度增大,则气体密度不再变化能表明该反应已达平衡状态,故正确;
c.该反应是一个气体体积减小的可逆反应,平衡后,压缩容器,容器的压强增大,平衡向正反应方向移动,NH3的量增大,故正确;
d.在恒温恒压装置中合成氨反应达到平衡后,向装置中通入一定量Ar,容器的压强减小,平衡向逆反应方向移动,故错误;
bc正确,故答案为:bc;
(3)①若未达平衡,温度越高反应速率越快,相同时间内氢气的含量越低,2min时,氢气的含量Ⅲ最大,则Ⅲ到达平衡,故答案为:Ⅲ到达平衡;
②设0~2 min内容器I中氨气的转化率为x,由题意建立如下三段式:
由氢气百分含量为40%可得![]() ×100%=40%,解得x=
×100%=40%,解得x=![]() ,则化学反应速率v(NH3)=
,则化学反应速率v(NH3)= ![]() ≈0.064 molL1min 1,故答案为:0.064 molL1min 1;
≈0.064 molL1min 1,故答案为:0.064 molL1min 1;
③若未达平衡,温度越高反应速率越快,相同时间内氢气的含量越低,2min时,氢气的含量Ⅲ最大,则II没有达到平衡,则v正>v逆,故答案为:>;
④合成氨反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,则当三个容器中的反应均达到平衡状态时,平衡常数最小的是容器Ⅲ,设0~2 min内容器中氨气的转化率为x,由题意建立如下三段式:

由氢气百分含量为60%可得![]() ×100%=60%,解得x=
×100%=60%,解得x=![]() ,则平衡常数K=
,则平衡常数K=![]() ≈2.1L2mol2,故答案为:2.1L2mol2;
≈2.1L2mol2,故答案为:2.1L2mol2;
(4)A.由图可知,NH3还原PbO2时,升高温度,![]() 增大,说明平衡向逆反应方向移动,NH3还原PbO2的反应为放热反应,△H<0,故错误;
增大,说明平衡向逆反应方向移动,NH3还原PbO2的反应为放热反应,△H<0,故错误;
B.相同温度时,![]() 的值越大,说明冶炼金属的还原效率越低,由图可知,相同温度时,NH3冶炼金属铬(Cr)的
的值越大,说明冶炼金属的还原效率越低,由图可知,相同温度时,NH3冶炼金属铬(Cr)的![]() 最大,则还原效率最低,故正确;
最大,则还原效率最低,故正确;
C.![]() 的值越大,说明NH3的利用率越大,由图可知,还原出金属铜(Cu)时,温度升高,
的值越大,说明NH3的利用率越大,由图可知,还原出金属铜(Cu)时,温度升高,![]() 增大,则325°C 下NH3的利用率比425°C下NH3的利用率更大,故正确;
增大,则325°C 下NH3的利用率比425°C下NH3的利用率更大,故正确;
D.、通过延长反应管的长度不能增加金属氧化物的表面积,不能增大金属氧化物和NH3的接触面积,故D错误;
BC正确,故答案为:BC。


科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如右图所示。下列说法正确的是

A.铁是阳极,电极反应为Fe-2e-+2OH-![]() Fe(OH)2
Fe(OH)2
B.电解一段时间后,镍电极附近溶液的pH减小
C.若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42-
D.每制得1mol Na2FeO4,理论上可以产生67.2L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜单质及其化合物在很多领域有重要的用途.
I.如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和![]() 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
(1)超细铜粉的某制备方法如图所示,![]() 中所含的化学键有 ______ .
中所含的化学键有 ______ .
![]()
(2)氯化亚铜![]() 的制备过程是:向
的制备过程是:向![]() 溶液中通入一定量
溶液中通入一定量![]() ,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
II.波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.已知![]() 的部分结构可表示如下:
的部分结构可表示如下:

(1)写出铜原子价电子层的电子排布式 ______ ,与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有 ______ ![]() 填元素符号
填元素符号![]() .
.
(2)请在上图中把![]() 结构中的化学键表示出来._____________
结构中的化学键表示出来._____________
(3)![]() 晶体中配位体是 ______ ,杂化轨道类型是
晶体中配位体是 ______ ,杂化轨道类型是![]() 杂化的原子是 ______ .
杂化的原子是 ______ .
(4)金属晶体Cu中原子的堆积方式如下图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如下图丙所示.
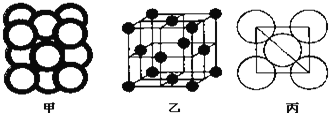
已知![]() 代表阿伏加德罗常数,Cu的相对原子质量为M,Cu单质晶体的密度为d
代表阿伏加德罗常数,Cu的相对原子质量为M,Cu单质晶体的密度为d![]() 该晶体的空间利用率是 ______ ,Cu原子半径的表达式为 ______
该晶体的空间利用率是 ______ ,Cu原子半径的表达式为 ______ ![]() 用含
用含![]() 、M、d的代数式表示
、M、d的代数式表示![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,相关坐标图错误的是
A | B | C | D |
向盐酸中滴入NaAlO2溶液 | NaHSO4溶液中逐滴加入 | 将铜粉加入到一定量浓硝酸中 | 将铁粉加入到一定量氯化铁溶液中 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物I是一种常用的植物调味油,常用脂肪烃A和芳香烃D按如下路线合成:

已知①RCHO+CH3CHO![]() RCH=CHO+H2O
RCH=CHO+H2O
②通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:
(1) A的名称是_______,H含有的官能团名称是________。
(2)②的反应条件是_______________,⑦的反应类型是_______________。
(3) I的结构简式是____________________。
(4)④的化学方程式是_______________________________。
(5)L是I的同分异构体且含有相同的官能团,其结构中苯环上只有两个处于对位的取代基,则L共有_____种 (不考虑立体异构)。
(6)参照上述合成路线,设计以C为原料制备保水树脂![]() ,的合成路线(无机试剂任选)__________________
,的合成路线(无机试剂任选)__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置的说法中正确的是
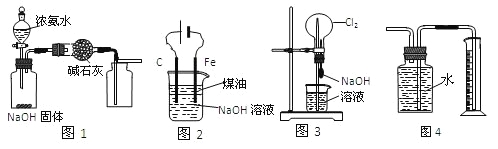
A. 用图1装置制取干燥纯净的NH3
B. 用图2装置制备Fe(OH)2并能较长时间观察其颜色
C. 用图3装置可以完成“喷泉”实验
D. 用图4装置测量Cu与浓硝酸反应产生气体的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用滴有酚酞和氯化钠溶液湿润的滤纸分别做甲、乙两个实验,下列判断错误的是( )
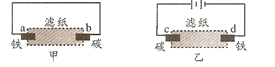
A.b极附近有气泡冒出B.d极附近出现红色
C.a、c极上都发生氧化反应D.甲中铁棒比乙中铁棒更易腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2=-58 kJ/mol
CH3OH(g)+H2O(g) △H2=-58 kJ/mol
③CO2(g)+H2(g)![]() CO(g)+H2O(g) △H3=+41 kJ/mol
CO(g)+H2O(g) △H3=+41 kJ/mol
回答下列问题:
(1)CO2的电子式是 。
(2)△H1= kJ/mol,①反应正向的熵变△S 0(填>、<或=)。
(3)在容积为2L的密闭容器中,充入一定量CO2和H2合成甲醇(上述②反应),在其他条件不变时,温度T1、T2对反应的影响图像如图,下列说法正确的是__________(填序号)
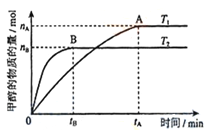
①温度为T1时,从反应到平衡,生成甲醇的平均速率为:v(CH3OH)=nA/tA mol/(L·min)
②当v(CH3OH) = v(H2O)时,说明反应达到平衡
③混合气体的平均相对分子质量A点大于B点
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)与n(CH3OH)比值增大
(4)在T1温度时,将2molCO2和6molH2充入2L密闭容器中,充分反应(上述②反应)达到平衡后,若CO2转化率为50%,,则容器内的压强与起始压强之比为__________;T1温度,反应CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)的平衡常数数值为__________。
CO2(g)+3H2(g)的平衡常数数值为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com