
【题目】A是植物秸秆的主要成分,以A为原料在一定条件下可获得多种有机物,它们的相互转化关系如图所示。已知F是一种最简单的烯烃。请回答:

(1)F→C的反应类型是___。
(2)D的官能团名称为___。
(3)C+E→G的化学方程式是___。
(4)下列说法正确的是__。
A.D能被氧化成E,但不能被还原成C
B.实验室制备G时可用浓硫酸作催化剂和吸水剂
C.B、C、E三种物质可以用新制氢氧化铜悬浊液鉴别
D.相同质量的B、G完全燃烧生成水的质量相等
E.SO2气体与F均能使溴水褪色,且原理相同
【答案】加成反应 醛基 C2H5OH+CH3COOH![]() CH3COOC2H5+H2O BC
CH3COOC2H5+H2O BC
【解析】
A是植物秸秆的主要成分,即纤维素,由“酒化酶”可知,B为葡萄糖,C为乙醇,D为乙醛,E为乙酸,G为乙酸乙酯,“F是一种最简单的烯烃”,则F为乙烯,据此分析。
(1)F→C为乙烯制乙醇的反应,方程式为![]() ,则反应类型是加成反应,故答案为:加成反应;
,则反应类型是加成反应,故答案为:加成反应;
(2)D为乙醛,官能团名称为醛基;
(3)C+E→G是乙醇与乙酸发生酯化反应生成乙酸乙酯和水,反应的化学方程式是C2H5OH+CH3COOH![]() CH3COOC2H5+H2O;
CH3COOC2H5+H2O;
(4)A.C为乙醇,D为乙醛,E为乙酸,乙醛能被氧化成乙酸,也能被还原成乙醇,选项A错误;
B.实验室制备乙酸乙酯时,浓硫酸的作用是催化剂和吸水剂,选项B正确;
C.B为葡萄糖,E为乙酸,葡萄糖含醛基,能与银氨溶液反应形成银镜,而乙酸不含醛基,不能发生银镜反应,选项C错误;
D.B为葡萄糖(![]() ),G为乙酸乙酯(
),G为乙酸乙酯(![]() ),二者最简式不同,故相同质量的时候生成水的量不同,选项D错误;
),二者最简式不同,故相同质量的时候生成水的量不同,选项D错误;
E.SO2气体与F均能使溴水褪色,前者与有色物质发生化合反应而褪色,后者因发生氧化还原反应而褪色,原理不相同,选项E错误;
答案选BC。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】化学是一门实验为基础的科学。请回答下列问题:
(1)利用如图装置可验证浓、稀硝酸氧化性强弱,请完成 实验操作,回答相关问题:
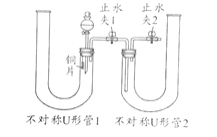
①实验操作过程:固定铜片,打开分液漏斗活塞及止水夹2,从不对称U形管1、2长管口处分别注入稀硝酸、浓硝酸,液面与双孔橡皮塞接触,然后,关闭分液漏斗玻璃活塞、止水夹1、2。此后可观察到现象______;然后打开止水夹1,会发现不对称U形管2中长导管口无色气泡变红棕色,浓硝酸逐渐变黄(说明稀硝酸不能氧化这种无色气体而浓硝酸可以)。
②请用一个化学方程式体现该实验验证浓、稀硝酸氧化性强弱的原理_________。
(2)利用如图装置可以验证非金属性的变化规律。
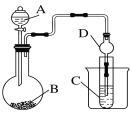
①干燥管D的作用是__________。
②实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B中所装药品分别为________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为______________________。
③若要证明非金属性:Cl > C >Si,则A中加入试剂____________、B中加Na2CO3、C中加入试剂______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一块11.0 g的铁铝合金,加入一定量的稀硫酸后合金完全溶解,然后加H2O2到溶液中无Fe2+存在,加热除去多余的H2O2,当加入200 mL 6 molL﹣1NaOH溶液时沉淀量最多,且所得沉淀质量为26.3 g,下列说法不正确的是
A.该合金中铁的质量为5.6 g
B.合金与稀硫酸反应共生成0.45 mol H2
C.该合金与足量氢氧化钠反应,转移的电子数为0.6 NA
D.所加的稀硫酸中含0.6 mol H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
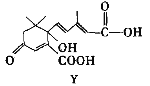
【题目】利用下图所示的有机物X可生产S-诱抗素Y。下列说法正确的是( )
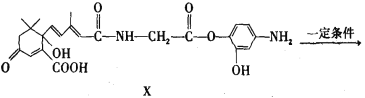
A. X可以发生氧化、取代、酯化、加聚、缩聚反应,并能与盐酸反应生成有机盐
B. Y既可以与FeCl3溶液发生显色反应,又可使酸性KMnO4溶液褪色
C. 1mol X与足量NaOH溶液反应,最多消耗4mol NaOH
D. 有机物分子中若某一个碳原子连接4个不同的原子或基团,这种碳原子称为“手性碳原子”,则在X结构中有2个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组选用酸性高锰酸钾溶液和草酸(H2C2O4)溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:[实验内容及记录]
已知:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
实验 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
_mol·L-1H2C2O4溶液 | H2O | 0.05 mol·L-1KMnO4溶液 | 3 mol·L-1稀硫酸 | ||
1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
2 | 2.0 | 2.0 | 4.0 | 2.0 | 5.2 |
3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
请回答:
(1)[实验原理]_____________(写离子方程式)。
(2)为完成实验目的,H2C2O4溶液的物质的量浓度不低于________。
(3)根据上表中的实验数据,可以得到的结论是_________。
(4)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设。并继续进行实验探究。

①该小组同学提出的假设是__________。
②请你帮助该小组同学完成实验方案。
实验 编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量MnSO4 | 室温下溶液颜色褪至无色所需时间/min | |||
__mol·L-1 H2C2O4溶液 | H2O | 0.05 mol·L-1 KMnO4溶液 | 3 mol·L-1 稀硫酸 | |||
4 | 3.0 | 1.0 | 4.0 | 2.0 | 0.1 g | t |
若该小组同学提出的假设成立,应观察到的现象_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W和X的最高价氧化物的水化物之间可以相互反应生盐和水,该反应的离子方程式为___。
(2)W与Y可形成化合物W2Y,该化合物的电子式为___。
(3)比较Y、Z气态氢化物的稳定性 > (用化学式表示)___。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为___。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > (用离子符号表示)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下常压下,1g固态碳与水蒸气恰好完全反应,反应生成气体CO和H2,吸收10.94kJ热量,此反应的热化学方程式为___。
(2)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-Q1kJ·mol-1,
②2H2(g)+O2(g)=2H2O(g) ΔH2=-Q2kJ·mol-1,
③2H2(g)+O2(g)=2H2O(l) ΔH3=-Q3kJ·mol-1。
常温下,取体积比4∶1的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为___kJ。
(3)以H2为燃料可制成氢氧燃料电池。已知:2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1,某氢氧燃料电池释放228.8kJ电能时,生成1mol液态水,该电池的能量转化率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烷、甲烷、乙醛的混合气体在同温同压下和CO2的密度相同,则三种气体的体积比可能是( )
①2:1:4 ②5:2:1 ③2:5:1 ④6:3:2 ⑤4:2:3
A. ①②B. ②③C. ③④⑤D. ①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G是周期表中短周期的七种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 其一种单质可吸收紫外线,是地球的保护伞 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
G | G是形成化合物种类最多的元素 |
(1)B元素符号为___,G的元素名称为___,它的一种同位素可测定文物年代,这种同位素的符号是___。
(2)A与C以原子个数比为1:1形成的一种化合物,其所属化合物类型为___(填“离子化合物”或“共价化合物”),包含的化学键有__(填“离子键”、“极性共价键”或“非极性共价键”)。
(3)F常温下可以形成两种用途广泛的氢化物,它们的电子式分别为__和__,并用电子式表示出其最简单气态氢化物的形成过程___。
(4)D在元素周期表中的位置__,D与E相比非金属性较强的是__(填元素名称),请从原子结构的角度解释原因:__。
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com