
【题目】W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W和X的最高价氧化物的水化物之间可以相互反应生盐和水,该反应的离子方程式为___。
(2)W与Y可形成化合物W2Y,该化合物的电子式为___。
(3)比较Y、Z气态氢化物的稳定性 > (用化学式表示)___。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为___。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > (用离子符号表示)___。
【答案】Al(OH)3+OH-=AlO2-+2H2O ![]() HCl>H2S SO2+Cl2+2H2O=H2SO4+2HCl S2->Cl->Na+>Al3+
HCl>H2S SO2+Cl2+2H2O=H2SO4+2HCl S2->Cl->Na+>Al3+
【解析】
(1)W、X的最高价氧化物对应的水化物可以反应,由于W、X是金属元素,说明他们的最高价氧化物对应水化物的反应是氢氧化物之间的反应,所以W是Na,X是Al;
(2)Na与Y可形成化合物Na2Y,说明Y是S元素;
(3)Z是Cl元素,非金属性Cl>S;
(4)将二氧化硫通入氯水中发生氧化还原反应生成硫酸和氯化氢,据此书写反应的化学方程式;
(5)简单离子的离子半径,电子层数越多,半径越大,层数相同时,核电荷越多半径越小。
(1)W、X的最高价氧化物对应的水化物可以反应,由于W、X是金属元素,说明他们的最高价氧化物对应水化物的反应是氢氧化物之间的反应,所以W是Na,X是Al,氢氧化钠和氢氧化铝反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)Na与Y可形成化合物Na2Y,说明Y是S元素,硫化钠的电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)Z是Cl元素,非金属性Cl>S,所以气态氢化物的稳定性HCl>H2S,故答案为:HCl>H2S;
(4)将二氧化硫通入氯水中发生氧化还原反应生成硫酸和氯化氢,反应的化学方程式为:Cl2+SO2+2H2O=H2SO4+2HCl,故答案为:Cl2+SO2+2H2O=H2SO4+2HCl;
(5)简单离子的离子半径,电子层数越多,半径越大,层数相同时,核电荷越多半径越小,Na、Al、S、Cl元素的简单离子的半径由大到小的顺序为:S2->Cl->Na+>Al3+,故答案为:S2->Cl->Na+>Al3+。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】(8分)向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式_____________。
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用图中的曲线表示是________(填序号).

(4)若向装有Ba(OH)2溶液烧杯里缓缓滴入KAl(SO4)2溶液至Ba2+恰好完全反应.则反应的离子方程式是 _________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】POCl3常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:
I.制备PCl3
(1)实验室用高锰酸钾和浓盐酸反应制氯气。发生装置可以是图中的____(填字母代号)。
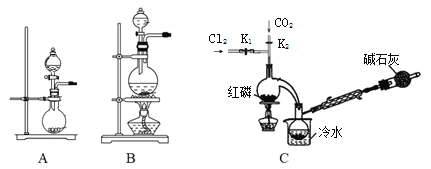
(2)检查装置C气密性并装入药品后,先关闭K1,打开K2通入干燥的CO2,一段时间后,关闭K2,加热曲颈瓶同时打开K1通入干燥氯气,反应立即进行。图中碱石灰的作用是______________。
II.实验室制备POCl3。
采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如图:
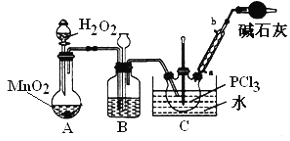
资料:①Ag++SCN﹣=AgSCN↓,Ksp(AgCl)>Ksp(AgSCN);
②PCl3和POCl3的相关信息如下表:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | ﹣112.0 | 76.0 | 137.5 | 两者互溶,均为无色液体,遇水均剧烈反应生成含氧酸和氯化氢 |
POCl3 | 2.0 | 106.0 | 153.5 |
(3)POCl3在潮湿空气中会剧烈“发烟”,反应的化学方程式为___________________________________。
(4)反应温度要控制在60~65℃,原因是:_________________________________。
(5)通过佛尔哈德法可以测定产品中Cl元素含量,实验步骤如下:
a、准确称取15.0 g POCl3产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00 mL溶液。
b、取10.00 mL溶液于锥形瓶中,加入10.00 mL 3.2 molL﹣1 AgNO3标准溶液。
c、加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
d、以NH4Fe (SO4) 2为指示剂,用0.2 molL﹣1 NH4SCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去l0.00 mL NH4SCN溶液。
①步骤d中达到滴定终点的现象是__________________________________________。
②产品中Cl元素的质量分数为______________(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸,又称草酸,通常在空气中易被氧化而变质。其两分子结晶水(H2C2O4·2H2O)却能在空气中稳定存在。在分析化学中常用H2C2O4·2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是
A.草酸是二元弱酸,其电离方程式为H2C2O4![]() 2H++C2O
2H++C2O![]()
B.草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂
C.乙二酸可通过乙烯经过加成、水解、氧化再氧化制得
D.将浓H2SO4滴加到乙二酸上使之脱水分解,分解产物是CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是植物秸秆的主要成分,以A为原料在一定条件下可获得多种有机物,它们的相互转化关系如图所示。已知F是一种最简单的烯烃。请回答:

(1)F→C的反应类型是___。
(2)D的官能团名称为___。
(3)C+E→G的化学方程式是___。
(4)下列说法正确的是__。
A.D能被氧化成E,但不能被还原成C
B.实验室制备G时可用浓硫酸作催化剂和吸水剂
C.B、C、E三种物质可以用新制氢氧化铜悬浊液鉴别
D.相同质量的B、G完全燃烧生成水的质量相等
E.SO2气体与F均能使溴水褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有几种有机物的键线式结构如图:
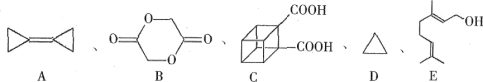
回答下列问题:
(1)有机物B所含官能团的名称是____。
(2)C的官能团位置异构体有___种。
(3)E的分子式为____。
(4)A与溴的四氯化碳反应,其产物的结构简式为____,该反应类型是____。
(5)在镍,80℃作用下,D与氢气反应生成丙烷。写出化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中不正确的是( )
A. 标况下,22.4L C2H2 中所含的 π 键数和 18g 冰中所含的氢键数均为 2NA
B. 双原子或多原子形成的气体单质中,一定有 σ 键,可能有 π 键
C. NH4+与 H3O + 均为 10 电子粒子,它们互为等电子体
D. 一个 P4S3 分子(结构如图)中含有三个非极性共价键

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推的思维方法在化学学习和研究中有时会产生错误的结论,因此类比推出的结论最终要经过实践的检验才能决定其正确与否。下列类推结论中正确的是( )
A.Mg失火不能用CO2灭火;Na失火也不能用CO2灭火
B.Fe3O4可写成FeO·Fe2O3;Pb3O4也可写成PbO·Pb2O3
C.Cu与Cl2直接化合生成CuCl2;Cu与S直接化合也能得到CuS
D.CO2通入到硝酸钡溶液中不能生成沉淀;SO2通入到硝酸钡溶液中也不能生成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出)
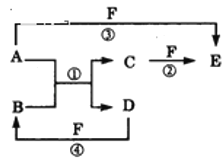
(1)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,③与④两个反应中都有红棕色气体生成,反应④的离子方程式是__,用电子式表示C的形成过程__,六种物质中所有元素的原子半径由大到小的顺序为__(用元素符号表示)。
(2)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则C的化学式为__,E的结构式为__,A、D、F所对应元素的气态氢化物的稳定性,由强到弱的顺序是__(用化学式表示),反应①的化学方程式是__。
(3)若B、C、F都是气态单质,且B为黄绿色,③和④两个反应中都有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,反应①的化学方程式是__,在反应中若有3mol电子转移,则生成C的物质的量为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com