
【题目】A、B、C、D、E、F、G是周期表中短周期的七种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 其一种单质可吸收紫外线,是地球的保护伞 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
G | G是形成化合物种类最多的元素 |
(1)B元素符号为___,G的元素名称为___,它的一种同位素可测定文物年代,这种同位素的符号是___。
(2)A与C以原子个数比为1:1形成的一种化合物,其所属化合物类型为___(填“离子化合物”或“共价化合物”),包含的化学键有__(填“离子键”、“极性共价键”或“非极性共价键”)。
(3)F常温下可以形成两种用途广泛的氢化物,它们的电子式分别为__和__,并用电子式表示出其最简单气态氢化物的形成过程___。
(4)D在元素周期表中的位置__,D与E相比非金属性较强的是__(填元素名称),请从原子结构的角度解释原因:__。
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:___。
【答案】Al 碳 ![]() C 离子化合物 离子键和非极性共价键
C 离子化合物 离子键和非极性共价键 ![]()
![]()
![]() 第三周期第VIA族 氯 氯与硫电子层数相同,氯原子半径小于硫,氯对最外层电子的吸引能力强,所以氯得电子能力强,即非金属性氯大于硫 4KClO3
第三周期第VIA族 氯 氯与硫电子层数相同,氯原子半径小于硫,氯对最外层电子的吸引能力强,所以氯得电子能力强,即非金属性氯大于硫 4KClO3![]() KCl+3KClO4
KCl+3KClO4
【解析】
由题干信息,A、B、C、D、E、F、G是周期表中短周期元素,A的一种单质可吸收紫外线,是地球的保护伞,该单质是O3,则A是O元素,B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的,则B为Al元素,C与B同周期,且是所在周期中原子半径最大的(稀有气体除外),则C为Na元素,D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味,则D为S元素,E与D同周期,且在该周期中原子半径最小,则E为Cl元素,F的氢化物和最高价氧化物的水化物反应生成一种离子化合物,则F为N元素,G是形成化合物种类最多的元素,则G是C元素,据此分析解答。
(1)根据上述分析可知,B为Al元素,元素符号为Al,G为C元素,元素名称为碳,![]() C可用于测定文物年代,故答案为:Al;碳;
C可用于测定文物年代,故答案为:Al;碳;![]() C;
C;
(2)O与Na以原子个数比为1:1形成的一种化合物为Na2O2,Na+和O22-形成离子键,O22-中O原子和O原子之间形成非极性共价键,属于离子化合物,故答案为:离子化合物;离子键和非极性共价键;
(3)N在常温下可形成两种用途广泛的氢化物为NH3和N2H4,均属于共价化合物,电子式分别为![]() 和
和![]() ,最简单的气态氢化物为NH3,其形成过程可表示为
,最简单的气态氢化物为NH3,其形成过程可表示为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;![]() ;
;
(4)D为S元素,位于元素周期表的第三周期第ⅥA族,E为Cl元素,由于氯与硫电子层数相同,氯原子半径小于硫,氯对最外层电子的吸引能力强,所以氯得电子能力强,则非金属性Cl>S,故答案为:第三周期第ⅥA族;氯;氯与硫电子层数相同,氯原子半径小于硫,氯对最外层电子的吸引能力强,所以氯得电子能力强,即非金属性氯大于硫;
(5)根据题干信息可知,KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1,则两种盐为氯化钾和高氯酸钾,反应方程式为4KClO3![]() KCl+3KClO4,故答案为:4KClO3
KCl+3KClO4,故答案为:4KClO3![]() KCl+3KClO4。
KCl+3KClO4。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A是植物秸秆的主要成分,以A为原料在一定条件下可获得多种有机物,它们的相互转化关系如图所示。已知F是一种最简单的烯烃。请回答:

(1)F→C的反应类型是___。
(2)D的官能团名称为___。
(3)C+E→G的化学方程式是___。
(4)下列说法正确的是__。
A.D能被氧化成E,但不能被还原成C
B.实验室制备G时可用浓硫酸作催化剂和吸水剂
C.B、C、E三种物质可以用新制氢氧化铜悬浊液鉴别
D.相同质量的B、G完全燃烧生成水的质量相等
E.SO2气体与F均能使溴水褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是制取氯气并以氯气为原料进行特定反应的装置,请回答下列问题:
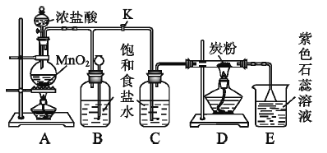
(1)A是制取氯气的发生装置,发生反应的离子方程式为_________。
(2)实验开始时,先点燃A处的酒精灯,打开旋塞K,让![]() 充满整个装置,再点燃D处的酒精灯,
充满整个装置,再点燃D处的酒精灯,![]() 通过C瓶后再进入D(D装置的硬质玻璃管内盛有炭粉)发生氧化还原反应其产物为
通过C瓶后再进入D(D装置的硬质玻璃管内盛有炭粉)发生氧化还原反应其产物为![]() 和
和![]() 。D中发生反应的化学方程式为_______,装置C的作用是_________。
。D中发生反应的化学方程式为_______,装置C的作用是_________。
(3)E处溶液的颜色由紫色变为红色,再变为无色,请解释溶液由红色变为无色的原因_______,若将E处烧杯中的溶液改为硝酸银溶液,发生反应的离子方程式为________。
(4)D处反应完毕后关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有![]() 产生,此时B中出现的现象是_________。
产生,此时B中出现的现象是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl﹣、![]() 、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH﹣等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③C.①②③②④D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷的分子结构可简写成键线式结构![]() ,有机物A的键线式结构为
,有机物A的键线式结构为![]() ,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
A. B的结构可能有3种,其中一种名称为2,2,3-三甲基-2-戊烯
B. 用系统命名法命名有机物A,名称为2,2,3-三甲基戊烷
C. 有机物A的分子式为C8H18
D. 有机物A的一氯取代物只有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出)
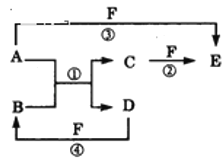
(1)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,③与④两个反应中都有红棕色气体生成,反应④的离子方程式是__,用电子式表示C的形成过程__,六种物质中所有元素的原子半径由大到小的顺序为__(用元素符号表示)。
(2)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则C的化学式为__,E的结构式为__,A、D、F所对应元素的气态氢化物的稳定性,由强到弱的顺序是__(用化学式表示),反应①的化学方程式是__。
(3)若B、C、F都是气态单质,且B为黄绿色,③和④两个反应中都有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,反应①的化学方程式是__,在反应中若有3mol电子转移,则生成C的物质的量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究铝片与Na2CO3溶液的反应,下列说法不正确的是( )
|
| |
无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验为H2和CO2) |
A.对比Ⅰ、Ⅲ,说明Na2CO3溶液能破坏铝表面的保护膜
B.Na2CO3溶液中存在平衡:CO32-+H2O![]() HCO3- +OH-
HCO3- +OH-
C.加热和H2逸出对CO32-水解平衡移动方向的影响是相反的
D.推测出现白色浑浊的原因:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】印刷铜制电路板的腐蚀液选取和回收再利用一直是研究的热点。
(1)应用传统蚀刻液(HCl-FeCl3)
①蚀刻铜板主要反应的离子方程式为_____。
②腐蚀结束后,通过以下两步可分离出铜,并实现FeCl3溶液再生。
![]()
步骤I所加试剂和操作分别为______。可实现步骤II转化的物质或方法是____(填一种即可)。
(2)应用酸性蚀刻液(HCl-H2O2),产生的蚀刻废液处理方法如图:
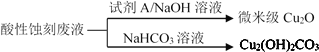
①蚀刻铜板主要反应的离子方程式为_____。
②回收微米级Cu2O过程中,加入的试剂A是____(填字母)。
a.Fe粉 b.葡萄糖 c. NaCl固体 d.酸性KMnO4溶液
③回收Cu2(OH)2CO3的过程中需控制反应的温度,当温度高于80℃时,产品颜色发暗,其原因可能是_____。
(3)应用碱性蚀刻液(NH3H2O–NH4Cl) 蚀刻铜板,会有Cu(NH3)4Cl2和水生成。蚀刻铜板主要反应的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为![]() ,下列说法错误的是( )
,下列说法错误的是( )
A.1mol苹果酸可与2molNaOH发生中和反应
B.一定条件下,苹果酸与乙酸或乙醇均能发生酯化反应
C.![]() 与苹果酸互为同分异构体
与苹果酸互为同分异构体
D.1mol苹果酸与足量金属Na反应生成1.5molH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com