
【题目】某有机物0.3克完全燃烧后生成224毫升(标准状况)二氧化碳和0.18克水。已知该物质的蒸气对氢气的相对密度为30,试求:
(1)有机物的分子式___________
(2)试写出该有机物可能的结构简式并命名____________________。
【答案】C2H4O2 CH3COOH 乙酸 HCOOCH3 甲酸甲酯
【解析】
有机物的蒸气密度是相同条件下氢气的30倍,则其相对分子质量为30×2=60,根据原子守恒计算有机物分子中N(C)、N(H),再结合相对分子质量计算有机物分子中N(O),据此确定有机物分子式;根据分子式确定其可能的结构。
(1)有机物的蒸气密度是相同条件下氢气的30倍,则其相对分子质量为30×2=60,该有机物0.3g完全燃烧后,生成224mLCO2 (标准状况下)和0.18gH2O;0.3g有机物的物质的量=![]() =0.005mol,n(CO2)=
=0.005mol,n(CO2)= ![]() =0.01mol;0.18gH2O的物质的量为
=0.01mol;0.18gH2O的物质的量为![]() =0.01mol,根据原子守恒,可以知道有机物分子中N(C)=
=0.01mol,根据原子守恒,可以知道有机物分子中N(C)=![]() =2;N(H)=
=2;N(H)=![]() =4,则有机物分子中N(O)=
=4,则有机物分子中N(O)= ![]() =2,故有机物分子式为C2H4O2;
=2,故有机物分子式为C2H4O2;
答:该有机物分子式为C2H4O2;
(2)有机物分子式为C2H4O2,则该有机物的结构简式为CH3COOH,乙酸;HCOOCH3,甲酸甲酯;
答: 该有机物可能的结构简式及命名:CH3COOH,乙酸;HCOOCH3,甲酸甲酯。


科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)CH3OH(g)。
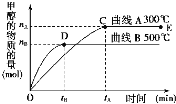
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=__________,升高温度,K值__________(填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=______________。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是__________(填字母序号)。
a.氢气的浓度减小 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,11.2LNO2完全溶于水,转移电子数为0.5NA
B.20gD2O和HTO两种水的组合中含有的中子数为10NA
C.一定温度下,1molH2和足量碘蒸气反应产生的H-I键数目为2NA
D.标准状况下,22.4L的HF中含有的原子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.在中和热测定实验中,为准确测得反应前后的温差,应将已分别测得温度的氢氧化钠溶液与盐酸在隔热的容器中快速混合,并不断搅拌,用温度计测量混合液的最高温度
B.往海带灰的浸泡液中加入过量的氯水,保证![]() 完全氧化为
完全氧化为![]()
C.将溴乙烷与氢氧化钾混合液加热,再滴加硝酸银溶液,观察有淡黄色沉淀生成,可证明溴乙烷中含有溴
D.润洗酸式滴定管时应从滴定管上口加入![]() 所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复
所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复![]() 次
次
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1 L FeCl3与CuCl2的混合溶液(其中Cu2+浓度为0.05 mol·L-1)中加入一定量的Fe粉,充分反应后过滤,剩余固体质量为6.0 g,向滤液中加入足量的AgNO3溶液,生成57.4 g沉淀。下列说法正确的是
A.剩余固体为CuB.加入Fe粉的质量为8.4 g
C.原溶液中Fe3+浓度为0.3 mol·L-1D.反应后溶液中Fe2+浓度为0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式中,不能正确表达反应颜色变化的是
A. 向CuSO4溶液中加入足量Zn粉,溶液蓝色消失Zn+CuSO4![]() Cu+ZnSO4
Cu+ZnSO4
B. 澄清的石灰水久置后出现白色固体Ca(OH)2+CO2![]() CaCO3↓+H2O
CaCO3↓+H2O
C. Na2O2在空气中放置后由淡黄色变为白色2Na2O2![]() 2Na2O+O2↑
2Na2O+O2↑
D. 向Mg(OH)2悬浊液中滴加足量FeCl3溶液出现红褐色沉淀3Mg(OH)2+2FeCl3![]() 2Fe(OH)3+3MgCl2
2Fe(OH)3+3MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为进行某些实验的探究,某兴趣小组设计了如下装置。

(1)为探究浓硫酸与木炭反应的全部产物,分液漏斗中盛浓硫酸,圆底烧瓶中放木炭。
①装置B中试剂的名称是________。
②装置C、D、E中所盛放的试剂分别是品红、酸性KMnO4溶液和澄清的石灰水。C装置的作用是________,确认产物中含有CO2的实验现象是________。
(2)为了制取无水氯化铜,上述装置中的分液漏斗中盛浓盐酸,圆底烧瓶中放MnO2,B中放铜粉并在玻璃管下添加酒精灯,且将B装置平移至D与E之间。
①此时C、D中依次加入的试剂分别是________。
②若E中为NaOH溶液用于尾气吸收,常温下发生反应的离子方程式为________。
③实验结束时,应首先熄灭装置B下面的酒精灯,其目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地环保部门将收集到的一定量酸雨试样分成甲、乙、丙、丁四份,进行如图所示的实验探究。
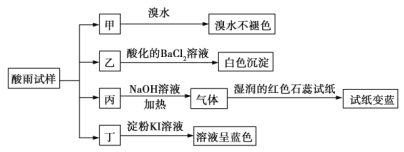
已知酸雨试样中可能含有下表所示的某些离子:
阳离子 |
|
阴离子 |
|
请回答下列问题:
(1)![]() 是______,
是______,![]() 是______。
是______。
(2)可能存在的阴离子是______,能证明该阴离子是否存在的简单实验操作为______。
(3)写出丁试样中滴加淀粉![]() 溶液所发生反应的离子方程式:______。
溶液所发生反应的离子方程式:______。
(4)某次降雨收集到![]() 雨水,向雨水中滴加
雨水,向雨水中滴加![]() 的
的![]() 溶液,充分反应后测得溶液中
溶液,充分反应后测得溶液中![]() ,再向该溶液中加入足量的
,再向该溶液中加入足量的![]() 溶液,经过滤、蒸干、称重,测得沉淀的质量为
溶液,经过滤、蒸干、称重,测得沉淀的质量为![]() 。假设雨水的酸性仅由
。假设雨水的酸性仅由![]() 和
和![]() 的排放所致,则排放到空气中的
的排放所致,则排放到空气中的![]() 和
和![]() 的物质的量之比约为______(不考虑
的物质的量之比约为______(不考虑![]() 的相互反应)。
的相互反应)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com