
【题目】高铁酸盐在水溶液中有四种含铁型体,25℃时,它们的物质的量分数随PH的变化如图所示。下列叙述错误的是
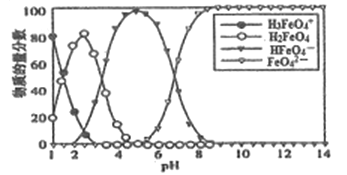
A. 已知H3FeO4+的电离平衡常数分别为:K1=2.5×10-2,K2=4.8×10-4、K3=5.0×10-8.当pH=4时,溶渡中c(HFeO4-)/c(H2FeO4)=1.2
B. 向pH=5的高铁酸盐溶液中加入KOH溶液,离子方程式为HFeO4-+OH-=FeO42-+H2O
C. PH=2时,溶液中主要含铁型体浓度的大小关系为c(H2FeO4)>c(H3FeO4+)>c(HFeO4-)
D. 为获得尽可能纯净的高铁酸盐,应控制PH≥9
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法,不正确的是( )
A. 制作光纤产品可用晶体硅
B. 纸浆漂白可用二氧化硫
C. 游泳池消毒可用漂粉精
D. 人工降雨可用干冰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图中的曲线是表示其他条件一定时,2NO+O2![]() 2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是
2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是

A. a点 B. b点 C. c点 D. d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应 A(g) + 2B(g) ![]() 2C(g) ΔH<0,在一定条件下达到平衡,若改变条件,将变化结果(“增大”、“减小”或“不变”)填入空格。
2C(g) ΔH<0,在一定条件下达到平衡,若改变条件,将变化结果(“增大”、“减小”或“不变”)填入空格。
(1)升高温度,B的转化率_____________,v(正)____________,v(逆)____________。
(2)保持温度和压强不变,加入惰性气体,则C的物质的量_____________,A的转化率_____________。
(3) 保持温度和体积不变,加入惰性气体,A的转化率_____________。
(4)若温度和体积不变,反应从开始到平衡,容器内气体的密度_____________,压强____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的方法是( )
A.在一定条件下通入H2B.通入足量酸性高锰酸钾溶液中
C.通入足量溴水中D.分别进行燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如下图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如下图所示,回答下列问题。
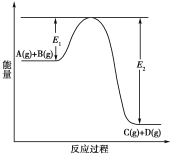
(1)该反应是________反应(填“吸热”或“放热”)。
(2)当反应达到平衡时,升高温度,A的转化率________(填“增大”、“减小”或“不变”)
(3)反应体系中加入催化剂对反应热是否有影响?___________________________________(填“有”、或“无”)
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1________,E2________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次增大的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A. 原子半径:W>Z>Y>X>M
B. 常见气态氢化物的稳定性:X<Y<Z
C. 1 mol WM溶于足量水中完全反应,共转移2 mol电子
D. 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,欲使CH3COONa溶液中c(CH3COO-)/c(Na+)的比值增大,可在溶液中加入下列物质中正确的是①固体NaOH ②固体KOH ③固体NaHS ④固体CH3COONa ⑤冰醋酸 ⑥加水
A. ②③④⑤ B. ②④⑤ C. ②⑤⑥ D. ①⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com