
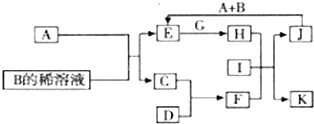
 A-LΪ��ѧ��ѧ�������ʣ�����Ҫת����ϵ����ͼ��ʾ�����в���ˮ����ȥ������֪AΪ�������ʣ�C��Dͨ��״����Ϊ���嵥�ʣ�B��F��Ϊ��Ҫ�Ļ�����Ʒ��0.05mol/LB����ҺpH=1��F���д̼�����ζ�����壬��һ����Fͨ��B��ϡ��Һ�п��Եõ�������K��L��G��I�ֱ�����ͬ������Ԫ����ɣ�ͨ��״���¾�Ϊ��ɫҺ�壮
A-LΪ��ѧ��ѧ�������ʣ�����Ҫת����ϵ����ͼ��ʾ�����в���ˮ����ȥ������֪AΪ�������ʣ�C��Dͨ��״����Ϊ���嵥�ʣ�B��F��Ϊ��Ҫ�Ļ�����Ʒ��0.05mol/LB����ҺpH=1��F���д̼�����ζ�����壬��һ����Fͨ��B��ϡ��Һ�п��Եõ�������K��L��G��I�ֱ�����ͬ������Ԫ����ɣ�ͨ��״���¾�Ϊ��ɫҺ�壮| G |
| G |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����е�C��SO2�е�S����ȡ����sp2�ӻ����� |
| B��N2H4�е�N��HClO�е�O����ȡ����sp3�ӻ����� |
| C����ϩ�����ӳɷ�ӦʱCԭ���ӻ����Ͳ��ᷢ���仯 |
| D��CS2��C2H2�е�C����ȡ����sp�ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��5.6 g���ֱ������������ᡢ������Ӧ������ת��������Ϊ0.3NA |
| B��14g��ϩ����ϩ�Ļ�����庬��C-H��Ϊ2NA |
| C����״���£�4.48L��ˮ��D2O���к��е�������Ϊ2NA |
| D����FeI2��Һ��ͨ������Cl2������1 mol Fe2+������ʱ����ת�Ƶĵ��ӵ���ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1mol I2��g����2mol H2����2L�ܱ������У���һ���¶��·�����Ӧ��I2��g��+H2 ��g��?2HI��g������H��0������ƽ�⣮HI�����ʵ�������w��HI����ʱ��仯��ͼ���ߣ�����ʾ��
��1mol I2��g����2mol H2����2L�ܱ������У���һ���¶��·�����Ӧ��I2��g��+H2 ��g��?2HI��g������H��0������ƽ�⣮HI�����ʵ�������w��HI����ʱ��仯��ͼ���ߣ�����ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��M��N��Q�������ʵ�Ũ��һ����� |
| B��M��Nȫ�������Q |
| C����Ӧ����������Ũ�ȶ����ֲ��� |
| D����Ӧ�Ѿ�ֹͣ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��A��B��SO2��ת������ͬ |
| B��B�еķ�Ӧ���ʱ�A�п� |
| C��A��SO2��ת���ʱ�B�и� |
| D����A��B�н��ټ���ͬ���������ƽ�ⲻ�ƶ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com