
【题目】下列说法不正确的是
A.浓度均为①![]() 的
的![]() ②
②![]() ③
③![]() ④
④![]() 溶液中
溶液中![]() 的大小顺序为③>①>②>④
的大小顺序为③>①>②>④
B.浓度均为![]() 的
的![]() 溶液与NaClO溶液,溶液中阴、阳离子的总浓度前者大于后者
溶液与NaClO溶液,溶液中阴、阳离子的总浓度前者大于后者
C.![]() 为一元弱酸,在
为一元弱酸,在![]() 水溶液中存在:
水溶液中存在:![]()
D.![]() 的
的![]() 溶液中:
溶液中:![]()
【答案】A
【解析】
A. 浓度均为![]() 的
的![]()
![]()
![]()
![]() 溶液,在这四种溶液中,亚铁离子抑制铵根离子水解、氢离子抑制铵根离子水解,但氢离子抑制程度大于亚铁离子,醋酸根离子、碳酸根离子都促进氨根离子水解,且碳酸根离子促进能力强于醋酸根离子,但
溶液,在这四种溶液中,亚铁离子抑制铵根离子水解、氢离子抑制铵根离子水解,但氢离子抑制程度大于亚铁离子,醋酸根离子、碳酸根离子都促进氨根离子水解,且碳酸根离子促进能力强于醋酸根离子,但![]() 中铵根离子浓度高,所以这四种溶液中铵根离子浓度大小顺序是:
中铵根离子浓度高,所以这四种溶液中铵根离子浓度大小顺序是:![]() ,故A错误;
,故A错误;
B. 等物质的量浓度的![]() 溶液与NaClO溶液,阳离子的总浓度都等于钠离子和氢离子的浓度和,钠离子浓度相等,又因为酸性比较:
溶液与NaClO溶液,阳离子的总浓度都等于钠离子和氢离子的浓度和,钠离子浓度相等,又因为酸性比较:![]() 强于HClO,所以次氯酸钠的碱性强,氢离子浓度小,故所含离子总浓度前者大于后者,故B正确;
强于HClO,所以次氯酸钠的碱性强,氢离子浓度小,故所含离子总浓度前者大于后者,故B正确;
C. ![]() 为一元弱酸,在
为一元弱酸,在![]() 水溶液中,
水溶液中,![]() 部分水解生成
部分水解生成![]() ,依据物料守恒得:
,依据物料守恒得:![]() ,故C正确;
,故C正确;
D. 碳酸氢根离子部分电离生成碳酸根离子,部分水解生成碳酸,依据物料守恒可知:碳酸根离子、碳酸氢根离子、碳酸分子中所有碳原子浓度之和等于![]() ,即
,即![]() ,故D正确;
,故D正确;
综上所述,答案为A。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用铁矿石(主要成分为Fe2O3,还有SiO2、Al2O3等杂质)提取Fe2O3。操作过程如下:
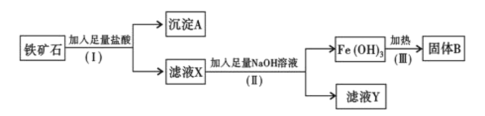
(1)I和II步骤中分离溶液和沉淀的操作名称_____;
(2)沉淀A中主要含有__________,固体B是____________;
(3)写出II步骤中生成Fe(OH)3的离子方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行反应:CO(g)+2H2(g)![]() CH3OH(g),下列事实能说明此反应已达到平衡状态的是( )
CH3OH(g),下列事实能说明此反应已达到平衡状态的是( )
A.容器内气体密度保持不变
B.用CO、H2、CH3OH表示反应的速率之比为1:2:1
C.单位时间内生成nmolCO的同时生成2nmolH2
D.混合气体的平均相对分子质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象与对应的说法正确的是![]()
A. 向NaOH溶液中加水稀释
向NaOH溶液中加水稀释
B. 等质量的Al、Zn与足量的稀硫酸反应
等质量的Al、Zn与足量的稀硫酸反应
C. 向稀硫酸中加入
向稀硫酸中加入![]() 溶液
溶液
D. 恒温下,适量蒸发饱和NaCl溶液的水分
恒温下,适量蒸发饱和NaCl溶液的水分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为前四周期原子序数依次增大的五种元素。A原子半径是周期表中原子半径最小的;B可以和A形成两种常见的液态化合物甲和乙,且原子个数之比分别是1:1和1:2;C、 D为同周期元素,C是所属周期的主族元素中电负性最小的;D的单质晶体是分子晶体,原子最外层有两个未成对电子;E位于周期表的ds区,E元素原子最外层有一个未成对电子。回答下列问题:
(1)E2+的简化电子排布式是__________;甲和乙沸点较高的是___________(填化学式);
(2)D与B形成常见的具有还原性的阴离子立体构型是三角锥形;则D显最高正价时与B形成的常见化合物的中心原子的杂化类型是_________
(3)同时由A、B、C、D四种元素组成的两种盐M和W,写出这两种盐溶液反应的离子方程式___________
(4)由B、D、E三种元素组成常见盐溶液丙,向丙溶液加入过量NaOH溶液可生成[E(OH)4]2-,不考虑空间构型,[E(OH)4]2-的结构可用示意图表示为__________
(5)根据周期表对角线规则,铍和铝的性质有相似性,则书写铍单质和C的最高正价氧化物对应水化物溶液发生反应的离子方程式是___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得滴定曲线如图。下列说法不正确的是( )

A. 在曲线上任一点均存在:c(Na+)c(OH-) = c(CH3COO-)c(H+)
B. 点①所示溶液中:c(CH3COO-)+2c(OH-) = c(CH3COOH)+2c(H+)
C. 点②所示溶液中:c(Na+) = c(CH3COO-)
D. 点③所示溶液中:c(Na+) > c(OH-) > c(CH3COO-) > c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列叙述正确的是( )

A. A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3和NaHCO3
B. B曲线中消耗盐酸0<v(HCl)<25mL时发生的离子反应为:OH-+H+=H2O H++CO32-=HCO3-
C. B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为224mL
D. 原NaOH溶液的物质的量浓度为1.0mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.H2SO4溶液与氢氧化钠反应:OH-+H+=H2O
B.铝与NaOH溶液反应:Al+2OH-= ![]() +H2↑
+H2↑
C.AlCl3溶液与氨水反应:AlCl3+3OH-=Al(OH)3↓+3Cl-
D.Cl2与氢氧化钠溶液反应:Cl2+2OH-=2ClO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+ 4B(g)![]() C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
A. vA=0.15mol/(L·min) B. vB=0.6 mol/(L·min)
C. vC=0.4 mol/(L·min) D. vD=0.01 mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com