
����Ŀ������˶�Ա����ɵ��ܡ�������Ŀʱ���á�þ�ۡ����֣�������Ч����ij�֡�þ�ۡ��п��ܺ���Mg��MgO��Mg(OH)2��MgCO3�е�һ�ֻ����ֹ��壬ʵ��С�����ɷ�չ����̽����
��֪��MgO+2HCl=MgCl2+H2O MgCO3+2HCl=MgCl2+H2O+CO2��
��1��̽����þ�ۡ����Ƿ���Mg��MgCO3
��ȡ������Ʒ����ͼ��ʾ����ʵ�顣�۲쵽a�Թ��������ݲ�����b�Թ��в���������������ʯ��ˮ����ǣ���֤����þ�ۡ���һ������______��

��Ϊ֤����þ�ۡ����Ƿ���Mg��С����ȼ�ŵ�ľ������ͼ��b�Թܿ��Ϸ���ľ��Ϩ�𡣵�ͬѧ��ָ������ʵ�鲻�ܴ��ʵ��Ŀ�ģ���Ҫ��ͼ�еij���ʯ��ˮ�滻��ŨNaOH��Һ��Ŀ����______________��С�������ĺ��ʵ�鷽���ظ�����ʵ�飬�۲쵽b�Թ�������������֤����þ�ۡ���______________��
��2��̽����þ�ۡ����Ƿ���MgO��Mg(OH)2
��ʵ����̡�
��.��MgO��Mg(OH)2��MgCO3���ֹ���ֱ�������ʵ�顣�ֱ�ȡ0.5g���ֹ����ĩ��ÿ��ȡ��������ͼ2��ʾ��

��μ�����ͬ��������������ϡ����ֱ����ĩǡ����ʧ�����±��м�¼���ĵ�ͬŨ��ϡ���������������������ͬһ�����²ⶨ���ұ�����С�����1λ��
MgO | Mg(OH)2 | MgCO3 | |
����ϡ�������� /mL | 10.4 | 7.2 | 5.0 |
Mg(OH)2�����ᷢ���кͷ�Ӧ�Ļ�ѧ����ʽΪ_____________��
��.ȡ��þ�ۡ���Ʒ0.5 g����������ϡ��������ĩǡ���ܽ⡣��ʱ����ϡ��������ԼΪ5.3 mL��
��ʵ����������ۡ�
��þ�ۡ���ֻ����MgCO3��������____________________________________��
��ʵ�鷴˼��
Ϊȷ����þ�ۡ��ľ���ɷ֣�ͬѧ����Ϊ����Ҫ��������ʵ�飺�ֱ�ȡ0.5 g��þ�ۡ���0.5 g_________����������ϡ���ᣬ�ⶨ���ɵ���������ֱ�Ϊ119mL��140mL���ɴ˿�֪��þ�ۡ��к���MgCO3����������Ϊ___________��
���𰸡���1����MgCO3�����Ѷ�����̼ȫ�����գ�û��Mg��
��2��Mg(OH)2 + 2HCl = MgCl2 + 2H2O��0.5g��þ��������ϡ����������0.5gMgCO3����ϡ������������ȣ�MgCO3��85%��
��������
�����������1���� ��������뵽��þ�ۡ��е�������a�Թ��������ݲ�����b�Թ��г���ʯ��ˮ����ǣ�֤��������CO2��һ���ж�����̼���������Ƶķ�Ӧ��������һ������MgCO3������Ϊ������̼��������ã����ȳ���������̼������Ҫ��ͼ�еij���ʯ��ˮ�滻����������Ũ��Һ����֤���Ƿ����������ɣ�����۲쵽b�Թ����������������Ʋ⡰þ�ۡ���һ��������þ��������ͼ�еij���ʯ��ˮ�滻��ŨNaOH��Һ��Ŀ�����Ѷ�����̼ȫ�����գ�ͨ��ʵ��֤�� ��þ�ۡ�����Mg��������2����ʵ����̡����ݸ��ֽⷴӦ����д�ص㡰�����ϣ������ϡ�����Mg(OH)2�����ᷢ���кͷ�Ӧ�����κ�ˮ�Ļ�ѧ����ʽΪMg(OH)2+2HCl�TMgCl2+2H2O����ʵ����������ۡ����ݱ����е����ݺ͡�ȡ��þ�ۡ���Ʒ0.5g����������ϡ��������ĩǡ���ܽ⣮��ʱ����ϡ��������ԼΪ5.3mL�������Ʋ⡰þ�ۡ���ֻ����MgCO3��������0.5g MgCO3���ĵ����������0.5g��þ�ۡ����ĵ������������ȣ���ʵ�鷴˼��Ϊȷ����þ�ۡ��ľ���ɷ֣�ͬѧ����Ϊ����Ҫ��������ʵ�飺�ֱ�ȡ0.5g��þ�ۡ���0.5g MgCO3����������ϡ���ᣬ�ⶨ���ɵ���������ֱ�Ϊ119mL��140mL����MgCO3������Ϊx����x��0.5g=119ml��140ml�����x=0.425g����(0.425g��0.5g)��100%=85%���ɴ˿�֪��þ�ۡ��к���MgCO3����������Ϊ85%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������7�����ʣ���NaHCO3��CH3COOH��BaSO4����HF����C2H5OH����Al����ʳ��ˮ.��������ǿ����ʵ��� ������ţ���ͬ�������ܸ����ᷴӦ���ܸ�NaOH��Һ��Ӧ���� ��
II������һƿŨ��Ϊ0.2mol/L��ij����Һ������Ϊ���ᡢ���ᡢ�����е�һ�֣�Ϊ��ȷ��������Һ����ɽ���ʵ�飺ȡ20.00mL������Һ����μ���0.2mol/L������������Һ��ǡ�÷�Ӧ��ȫʱ�����Һ���Ϊ20.00mL�����û�ѧ����ش�
��1����������� ��
��2����pH��ֽ��÷�Ӧ��������Һ�ʼ��ԣ����ݴ�����˵��������ҺΪ �������ӷ���ʽ˵����Һ�ʼ��Ե�ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����������������������ֳ�����������д�ڿհ״���
�ٰ�п������ϡ������ʱ��������ų��� ��
��ʢ��Ũ������ձ����ڷ���һ��ʱ����������ӡ� ��
���ò�����պŨ�������ֽ��ʱ��ֽ��ڡ� ��
�ܰ�ľ̿�����ȵ�Ũ������ʱ��������ų��� ��
���ڳ����¿�����������������ʢװ���Ũ���ᡣ ___ ��
��2��ʵ������ȡ�����Ļ�ѧ����ʽ: ��
��3��ͭ��ϡ���ᷴӦ�����ӷ���ʽ: ��
��4��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ: ��
��5������������Һ�������Һ���ȷ��������ӷ���ʽ: ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��������Ӽ������й��ۼ����ǣ� ��
A��NaCl B��Ca��OH��2 C��H2O D��CH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ѧ�о��IJ�ʢʱ�ڣ���ѧ���о����֣������������ڵ������ӣ��ɽ���1������ת��Ϊ�������������ɻ�(O2�D)��������������һϵ�����ɻ���һ������������������ھ���һ�������Ļ�����ϵͳ(������ø�Ϳ�������)���ܽ�������ת��Ϊ���Խϵ͵����ʣ���������ܵ����������������ǰ�(NH2OH)�����ķ������Լ��������ϵͳ��O2�D������ԭ����O2�D���ǰ���Ӧ����NO2�D��һ�ֹ������NO2�D�ڶ�����������������������£����ɷۺ��ż��Ⱦ�ϣ���Ⱦ��������530nm�����������գ���������ֵ��c(NO2�D)�����ȣ��Ӷ��ɼ������Ʒ�е�O2�D������ijʵ���������Ϸ�������������Һ�У�c(NO2�D) ��2.500��10-3 molL-1��
��1���뽫�ⶨԭ���йص����ӷ���ʽȱ�ٵ����ʲ�����������ƽ��
![]() NH2OH ��
NH2OH ��![]() O2�D ��
O2�D ��![]() H����
H����![]() NO2�D ��
NO2�D ��![]() ��
��![]() H2O��
H2O��
��2���������Ʒ��c(O2�D ) �� ��
��3�������ǰ��������ⶨO2�Dʱ���������ɵĹ���������Ϊ������ѡ������K2Cr2O7��Һ���ж�����������д����Ӧ�����ӷ���ʽ ��
��4��NO2�D���������ԣ����л�ԭ�ԡ�NaNO2��������ѪҺʱ���ܽ�Ѫ�쵰���е�Fe2+������Fe3+��������Ѫ�쵰��ת��Ϊ����Ѫ�쵰�ף�ʧȥЯ�����ܣ������ж����������������и����Լ����ܼ���NO2�D���� ��
A��FeCl2 KSCN B��KMnO4 H2SO4
C��AgNO3 HNO3 D��KI��������Һ
��5��ij�о���ѧϰС�飬Ϊ�о��⻯ѧ�����������ɣ���һ����ʵ�����У������������Ҫ�ɷ�ΪRH(��)��NO��NO2��O3��PAN(CH3COOONO2)���������ʵ����Ũ����ʱ�����ʧ����¼����ͼ������ͼ�����ݣ������ж�������������������� ��

A��NO����ʧ�����ʱ�RH�� B��NO������NO2
C��RH��NO2��������PAN��O3 D��O3������PAN
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z���ֶ�����Ԫ�طֱ��ڲ�ͬ�����ڡ���֪Xԭ�Ӻ�Yԭ��������������ͬ��Zԭ�Ӵ����ֻ���������ӣ�X��Z�����γ����ӻ�����X2Z��Y��Z�����γɹ��ۻ�����Y2Z��
��1��д��Ԫ�ط�����X______��Y______��Z______��
��2��Y���ʵĵ���ʽ��_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л������������صĽṹ����������
��1��������� �͵Ŀռ�ṹ������Ȳ����� �ͽṹ��
��2��������FeCl3��Һ���� ɫ����������Ũ���Ṳ�Ȼ�� ɫ�������������� ɫ����Щ���Գ����������ʵļ�������
��3�����ɵ����ʵİ����Ἰ������![]() -�����ᡣ����R����ʾ������
-�����ᡣ����R����ʾ������![]() -������Ľṹͨʽ�ɱ�ʾΪ �������������������һ�������������������һ�ֶ��ģ��÷�Ӧ�Ļ�ѧ����ʽΪ ��
-������Ľṹͨʽ�ɱ�ʾΪ �������������������һ�������������������һ�ֶ��ģ��÷�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ0.1 mol��L��1 NaOH��Һ450 mL��0.5 mol��L��1������Һ500mL��������������Һ����������ش��������⣺
(1)��ͼ��ʾ��������������Һ�϶�����Ҫ������__________(�����)������������Һ�����õ��IJ�����������____________(����������)��
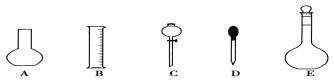
(2)���ݼ�����������ƽ��ȡNaOH������Ϊ�� g����ʵ����������������ȷ��������ʱ���ӿ̶��ߣ���������ҺŨ����__________0.1 mol��L��1(������������������������С����)��
(3)�ɼ���֪��������������Ϊ98%���ܶ�Ϊ1.84 g��cm��3��Ũ��������Ϊ__��__mL(����������һλС��)�����ʵ������15 mL��20 mL��50 mL��Ͳ��Ӧѡ��__��__mL��Ͳ��á����ƹ������������ձ��н�Ũ�������ϡ�ͣ�ϡ��ʱ���������ǽ�Ũ�������ձ��ڻ�������ˮ�У����ò��������Ͻ��衣
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com