
【题目】对于下列事实的解释错误的是( )
A.在蔗糖中加入浓硫酸后岀现发黑现象,说明浓硫酸具有吸水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C.氨溶于水的喷泉实验,说明氨气极易溶于水
D.向碘水中滴加CCl4,振荡静置分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中;
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡;
③在50~60℃下发生反应,直至反应结束;
④除去混合酸后,粗产品依次用蒸馏水和5%![]() 溶液洗涤,最后再用蒸馏水洗涤;
溶液洗涤,最后再用蒸馏水洗涤;
⑤将用无水![]() 干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
请回答下列问题:
(1)配制一定比例的浓硫酸与浓硝酸的混合酸时,操作的注意事项是_______________________________。
(2)步骤③中,为了使反应在50~60℃下进行,常用的方法是___________________________________。
(3)步骤④中洗涤粗硝基苯应使用的仪器是___________________________________________________。
(4)步骤④中粗产品用5%![]() 溶液洗涤的目的是___________________________________________。
溶液洗涤的目的是___________________________________________。
(5)纯硝基苯是无色、密度比水_______________________________(填“小”或“大”)的油状液体,它具有________味。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸松油酯是松油醇的酯化产物,具有甜香气味,广泛应用于日用和食用香精中。乙酸松油酯的结构简式如图甲所示,下列说法正确的是
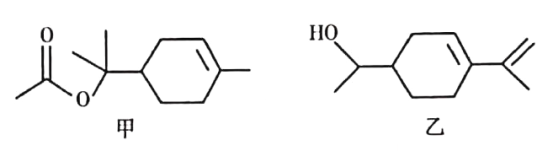
A. 乙酸松油酯的分子式为C12H22O2
B. 乙酸松油酯的水解产物松油醇与图乙所示物质互为同分异构体
C. 乙酸松油酯既易溶于水、也易溶于乙醇或油脂
D. 乙酸松油酯能使Br2的CCl4溶液或酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮(水中以NH3和NH4+形式存在的氮)含量是环境水体污染的一项重要指标,其氧化过程会造成水体中溶解氧浓度降低,导致水质下降,影响水生动植物的生长。
(1)水中NH3和NH4+两者的浓度比取决于水体的pH和水温。当pH偏高时,___比例较高,原因是___(请用离子方程式表示)。
(2)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH充分反应后,再向水中通入空气,可增大NH3的脱除率,用平衡移动原理解释其原因:___。
(3)在微生物作用下,蛋白质在水中分解产生的NH3能够被O2氧化生成亚硝酸(HNO2)。
___NH3+__O2→__HNO2+__________
①请将上述化学方程式补充完整,并配平。
②反应中氧化剂与还原剂的物质的量之比为___。
③若反应中有0.6mol电子发生转移,生成亚硝酸的质量为___。
(4)水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示。DO的测定原理如下:
①2Mn2++O2+4OH-→2MnO(OH)2↓
②MnO(OH)2+2I-+4H+→Mn2++I2+3H2O
③2S2O32-+I2→S4O62-+2I-
某小组同学取100.00mL水样经反应①和②后,取出20.00mL溶液,以淀粉作指示剂,用amol/LNa2S2O3溶液进行滴定,终点现象为___;滴定消耗Na2S2O3溶液bmL,水样的DO=____mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A~E能发生如图所示一系列变化,则下列说法错误的是

A. A分子中所有原子均在同一平面内
B. A→B所用试剂为![]()
C. 分子式为![]() 的酯有3种
的酯有3种
D. 等物质的量的B、D分别与足量钠反应生成气体的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.用铜作电极电解硫酸铜溶液: 2Cu2+ + 2H2O ![]() 2Cu+ O2↑+4H+
2Cu+ O2↑+4H+
B.用银氨溶液检验乙醛中的醛基: CH3CHO+2Ag(NH3)2++2OH-![]() CH3COO-+NH4++3NH3+2Ag↓+H2O
CH3COO-+NH4++3NH3+2Ag↓+H2O
C.苯酚钠溶液中通入少量的CO2: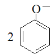 +H2O
+H2O![]()
![]() +CO32-
+CO32-
D.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e-= 4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜在自然界中常以多种形态存在,现以孔雀石矿石[成分为Cu2(OH)2CO3、CuFeS2、SiO2、Fe2O3等]为原料生产主产品胆矾和副产品铁红的工艺流程如图:

(1)气体1的成分除H2O(g)外,还有CO2、SO2,写出步骤①中发生氧化还原反应的化学方程式为 _______________,若反应生成1mol SO2,则反应中转移的电子数为___________mol。滤液1的主要成分为__________(写化学式)
(2)目前工业生产中步骤③酸浸的百分率为70%,为进一步提高酸浸的百分率可采取的措施有_________________(答出两点)。
(3)步骤④调pH所用试剂为_____________ (写化学式)
(4)常温下滤液3的pH=4,Ksp[Fe(OH) 3]=4×10-38,则滤液3中c(Fe3+)=___________。
(5)步骤⑤操作为_______________________________________________________.。
(6)假设使用孔雀石矿石质量为m kg,步骤③酸浸的百分率为70%,经滤渣2所得铁红的质量为n kg,则:
①铁红的用途之一为________,
②孔雀石矿石中铁元素的含量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以乙醇为原料制备少量1,2—二溴乙烷的相关装置如图所示。下列说法正确的是( )

A.用装置甲制取乙烯,加热混合液使温度缓慢上升至170℃
B.用装置乙净化乙烯,瓶中盛放的试剂可以是KMnO4酸性溶液
C.用装置丙制备1,2—二溴乙烷,冰水浴、液溴液面上加少量水等措施均可减少Br2的挥发
D.用装置丁净化尾气,可除去尾气中的Br2和未反应的乙烯气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其中Y与Z为金属元素,四种元素的简单离子的电子层结构均相同。p、q是它们中的部分元素组成的化合物,r是W的单质,s是Z的单质。这些物质间的转化关系如图所示。下列说法不正确的是

A.原子半径:Y>Z>W>X
B.q属于离子化合物
C.一定条件下,r与s能发生化合反应生成p
D.p能与盐酸反应,但不能与氢氧化钠溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com