
【题目】在体积一定的密闭容器中![]() 和3mol
和3mol![]() 发生反应:
发生反应:![]()
![]()
![]() 。下列有关说法正确的是
。下列有关说法正确的是
A.降低温度可以加快反应速率
B.向容器中再加入![]() 可以加快反应速率
可以加快反应速率
C.达到化学反应限度时,生成2mol![]()
D.达到化学平衡时![]() 、
、![]() 、
、![]() 的物质的量之比为1:3:2
的物质的量之比为1:3:2
科目:高中化学 来源: 题型:
【题目】2mol金属钠和1mol氯气反应的能量关系如图所示,下列说法不正确的( )
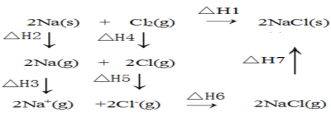
A.△H2+△H3+△H4+△H5+△H6+△H7=△H1
B.△H4的值数值上和Cl-Cl共价键的键能相等
C.△H5<0,在相同条件下,2Br(g)的△H5′<△H5
D.△H7<0,且该过程形成离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:![]() ,下图中的曲线是不同温度下的平衡转化率曲线,图中有a、b、c三点,则下列说法正确的是
,下图中的曲线是不同温度下的平衡转化率曲线,图中有a、b、c三点,则下列说法正确的是
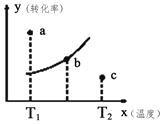
A.该反应是放热反应
B.b点时有![]()
C.![]() 温度下,若由a点达到平衡,可以采取增大压强的方法
温度下,若由a点达到平衡,可以采取增大压强的方法
D.c点![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是一种重要的化工产品,2SO2+O2![]() 2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
A.只要选择适宜的条件,SO2和O2就能全部转化为SO3
B.该反应达到平衡后,反应就完全停止了,即正逆反应速率均为零
C.如果反应前充入由18O原子组成的O2,反应达到平衡状态时,18O只存在于O2和SO3中
D.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g)△H<0,在恒容的密闭容器中,下列有关说法不正确的是
2N2(g)+3H2O(g)△H<0,在恒容的密闭容器中,下列有关说法不正确的是![]()
A.平衡时,其他条件不变,升高温度可使该反应的平衡常数减小
B.平衡时,其他条件不变,增加![]() 的浓度,废气中氮氧化物的转化率增大
的浓度,废气中氮氧化物的转化率增大
C.单位时间内消耗NO和![]() 的物质的量比为1:1时,反应达到平衡
的物质的量比为1:1时,反应达到平衡
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在漂白液(次氯酸钠溶液)中:Ag+、K+、NO3-、SO32-
B.中性溶液:K+、NO3-、Br-、Fe3+
C.![]() =1012的溶液中,NH4+、Ca2+、Cl-、NO3-
=1012的溶液中,NH4+、Ca2+、Cl-、NO3-
D.由水电离的c(H+)=1×10-10mol/L的溶液中:K+、Na+、HCO3-、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲烷制氢是一种廉价的制氢方法。有关的热化学方程式如下:
![]() ;
;![]() ①
①
![]() ;
;![]() ②
②
①下列说法正确的是 ______。
A.![]()
B.当反应①中![]() 时,表明该反应达平衡状态
时,表明该反应达平衡状态
C.其它条件不变时,增大体系压强,反应①②中甲烷的转化率均增大
D.为维持恒定温度![]() 不考虑热量损失
不考虑热量损失![]() ,某反应器中同时发生反应①与②时,消耗甲烷的物质的量之比为6:1
,某反应器中同时发生反应①与②时,消耗甲烷的物质的量之比为6:1
②某温度下,在100L反应器中充入甲烷和水蒸汽的物质的量分别为100mol和300mol时,假定只发生反应![]() 当甲烷的转化率为
当甲烷的转化率为![]() 时,此时平衡常数为 ______。
时,此时平衡常数为 ______。
(2)蓝液是由![]() 、
、![]() 及NaOH配成的,在加热条件下,通过三步反应使铁表面生成一层致密的
及NaOH配成的,在加热条件下,通过三步反应使铁表面生成一层致密的![]() :
:
![]()
![]()
![]() ①
①
![]()
![]()
![]() ②
②
以及第三步生成四氧化三铁,请补充第三步反应的方程式并配平: ______。
①为了使铝表面形成较厚的氧化膜,工业上常用电解硫酸溶液的方法,在阳极上生成氧化铝,写出此时阳极的电极反应: ______。
②将固体草酸锰![]() 放在一个可以称出质量的容器里加热,固体质量随温度的变化关系如图所示
放在一个可以称出质量的容器里加热,固体质量随温度的变化关系如图所示![]() 质量单位为
质量单位为![]() :则
:则![]() 时,剩余固体的成分为 ______(填化学式);在
时,剩余固体的成分为 ______(填化学式);在![]() ,剩余固体的成分为 ______(填化学式)。
,剩余固体的成分为 ______(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
A. 溶液的pH增大
B. CH3COOH电离度增大
C. 溶液的导电能力减弱
D. 溶液中c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将pH和体积均相同的HCl和CH3COOH溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
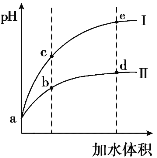
A.曲线II代表HCl的稀释过程
B.溶液中水的电离程度:b点>c点
C.从b点到d点,溶液中![]() 保持不变
保持不变
D.该温度下,b点Kw的数值比e点大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com