
【题目】TiCl3是烯烃定向聚合的催化剂、TiCl4可用于制备金属Ti。
nCH3CH=CH2![]()
TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
(1)Ti3+的基态核外电子排布式为__________。
(2)丙烯分子中,碳原子轨道杂化类型为______和____。
(3)Mg、Al、Cl第一电离能由大到小的顺序是___________。
(4)写出一种由第2周期元素组成的且与CO互为等电子体的阴离子的电子式________。
(5)TiCl3浓溶液中加入无水乙醚,并通入HCl至饱和,在乙醚层得到绿色的异构体,结构式分别是[Ti(H2O)6]Cl3、[Ti(H2O)5Cl]Cl2·H2O。1mol[Ti(H2O)6]Cl3中含有σ键的数目为______。

(6)钛酸锶具有超导性、热敏性及光敏性等优点,该晶体的晶胞中Sr位于晶胞的顶点,O位于晶胞的面心,Ti原子填充在O原子构成的正八面体空隙的中心位置,据此推测,钛酸锶的化学式为_________。
【答案】[Ar] 3d1 sp2 sp3 Cl>Mg>Al ![]() 18NA SrTiO3
18NA SrTiO3
【解析】
(1)Ti是22号元素,电子排布式为[Ar]3d24s2,Ti3+的基态核外电子排布式为[Ar]3d1。
(2)丙烯分子中,第2、3个碳原子有三个价键即为sp2杂化,第1个碳原子有四个价键即为sp3杂化。
(3)铜周期电离能呈增大趋势,但第IIA族大于第IIIA族,第VA族大于第VIIA族,因此Mg、Al、Cl第一电离能由大到小的顺序是Cl>Mg>Al。
(4)根据N = O或C2 = O,与CO互为等电子体的阴离子为CN或C22,再写其电子式。
(5)一个水有2个 σ键,1mol[Ti(H2O)6]Cl3中含有σ键的数目为(2×6 + 6)NA =18NA。
(6)该晶体的晶胞中Sr位于晶胞的顶点即![]() 个,O位于晶胞的面心即
个,O位于晶胞的面心即![]() 个,Ti原子填充在O原子构成的正八面体空隙的中心位置即1个,因此钛酸锶的化学式为SrTiO3。
个,Ti原子填充在O原子构成的正八面体空隙的中心位置即1个,因此钛酸锶的化学式为SrTiO3。
(1)Ti是22号元素,电子排布式为[Ar]3d24s2,Ti3+的基态核外电子排布式为[Ar]3d1,故答案为:[Ar]3d1。
(2)丙烯分子中,第2、3个碳原子有三个价键即为sp2杂化,第1个碳原子有四个价键即为sp3杂化,故答案为:sp2;sp3。
(3)铜周期电离能呈增大趋势,但第IIA族大于第IIIA族,第VA族大于第VIIA族,因此Mg、Al、Cl第一电离能由大到小的顺序是Cl>Mg>Al,故答案为:Cl > Mg > Al。
(4)根据N = O或C2 = O,与CO互为等电子体的阴离子为CN或C22,其电子式为![]() ,故答案为:
,故答案为:![]() 。
。
(5)一个水有2个 σ键,1mol[Ti(H2O)6]Cl3中含有σ键的数目为(2×6 + 6)NA =18NA,故答案为:18NA。
(6)该晶体的晶胞中Sr位于晶胞的顶点即![]() 个,O位于晶胞的面心即
个,O位于晶胞的面心即![]() 个,Ti原子填充在O原子构成的正八面体空隙的中心位置即1个,因此钛酸锶的化学式为SrTiO3,故答案为:SrTiO3。
个,Ti原子填充在O原子构成的正八面体空隙的中心位置即1个,因此钛酸锶的化学式为SrTiO3,故答案为:SrTiO3。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:
【题目】用下列实验装置(部分夹持装置略去)进行相应的实验,能达到实验目的的是 ( )
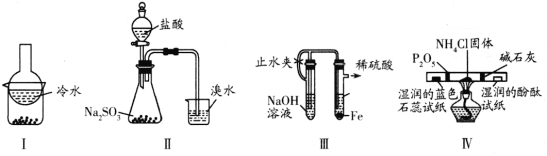
A. 加热装置I中的烧杯分离I2和高锰酸钾固体
B. 用装置II验证二氧化硫的漂白性
C. 用装置III制备氢氧化亚铁沉淀
D. 用装置IV检验氯化铵受热分解生成的两种气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种重要的有机合成中间体,它的合成路线如图:
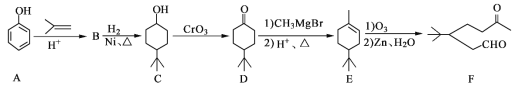
(1)化合物F中含氧官能团的名称是______和______,由A生成B的化学反应类型是______;
(2)写出化合物B的结构简式:______;
(3)写出化合物C与乙酸反应生成酯的化学方程式:______;
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化合物的结构简式:______(任写一种);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定温度时:![]() 。当生成2mol SO3时,放出热量197kJ,在相同温度和压强下,向密容器中通入3mol SO2和1molO2,达到平衡时放出热量Q,则下列关系式中正确的是
。当生成2mol SO3时,放出热量197kJ,在相同温度和压强下,向密容器中通入3mol SO2和1molO2,达到平衡时放出热量Q,则下列关系式中正确的是
A.Q=197 kJB.Q<197×2 kJC.Q<197 kJD.Q>197 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,H2X溶液中逐滴滴加NaOH溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列说法正确的是( )
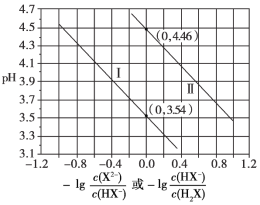
A.H2X的电离方程式为:H2X![]() 2H++X2-
2H++X2-
B.pH与-lg![]() 的变化关系是曲线Ⅰ
的变化关系是曲线Ⅰ
C.常温下,水解反应X2-+H2O![]() HX-+OH-的化学平衡常数为10-9.54
HX-+OH-的化学平衡常数为10-9.54
D.NaHX溶液中离子浓度由大到小顺序:c(Na+)>c(HX-)>c(X2-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性或碱性溶液中铝均可与NO![]() 发生氧化还原反应,转化关系如图:
发生氧化还原反应,转化关系如图:
已知:气体D和A溶液反应生成白色沉淀,气体D和F反应可生成盐。
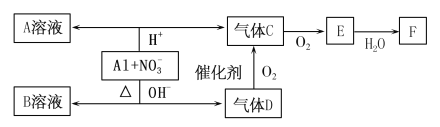
请回答下列问题:
(1)写出铝在碱性条件下与NO![]() 反应的离子方程式_________。
反应的离子方程式_________。
(2)在酸性条件下,被还原的NO![]() 与Al的物质的量之比是_______。
与Al的物质的量之比是_______。
(3)C、E排入大气中会造成大气污染,在催化剂存在下,D可以将C和E都转化为无毒的气态单质,请写出D和C反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁做电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是

A.铁是阳极,电极反应为Fe-6e-+4H2O===FeO42-+8H+
B.镍电极上的电极反应为2H2O+2e-==H2↑+2OH-
C.若隔膜为阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低、阴极区pH升高,最终溶液pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1,反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是( )
COS(g)+H2(g) K=0.1,反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是( )
A.升高温度,H2S浓度增加,表明该反应是吸热反应
B.通入CO后,平衡常数增大
C.反应前H2S物质的量为7mol
D.CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式正确的是( )
选项 | 已知条件 | 热化学方程式 |
A | H2的燃烧热为a kJ·mol-1 | H2+Cl2 |
B | 1 mol SO2、0.5 mol O2完全反应,放出热量98.3 kJ | 2SO2(g)+O2(g) ΔH=-98.3 kJ·mol-1 |
C | H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1 | H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6 kJ·mol-1 |
D | 31 g白磷比31 g红磷能量多b kJ | P4(白磷,s)=4P(红磷,s)ΔH=-4b kJ·mol-1 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com