
������ˮ�п��ܴ��ڵ���ƽ�⡢�ε�ˮ��ƽ��ͳ������ܽ�ƽ�⣬���Ƕ��ɿ�����ѧƽ�⡣�������ѧ��֪ʶ�ش��±��Dz�ͬ�¶���ˮ�����ӻ����ݣ�
| �¶� / �� | 25 | t1 | t2 |
| ˮ�����ӻ����� | 1��10��14 | �� | 1��10��12 |
(1)�� (2)4��1��10��10 ���� (3)9:11(2��)
���������������1��ˮ��������ʣ����ڵ���ƽ�⡣�����������ȵģ����ȴٽ�ˮ�ĵ��룬˭�����ӻ����������������25��t1��t2�������1��10��14��
��2��25��ʱ��ijHCl��Һ��c(HCl)��1��10��4 mol��L��1������Ԫ����ǿ�ᣬ��ȫ���룬��˸���Һ��������Ũ����1��10��4 mol��L��1��������Һ��pH��4����ʱc��H+��H2O������Һ��OH��Ũ�ȣ������� ��1��10��10mol/L����ˮϡ��1000������������Խ��ͣ����������Լ��ԣ�������ϡ�ͺ���Һ��pH��7��
��1��10��10mol/L����ˮϡ��1000������������Խ��ͣ����������Լ��ԣ�������ϡ�ͺ���Һ��pH��7��
��3��t2��ʱ��ˮ�����ӻ�������1��10��12����ʱpH��11��������������Һ��Ũ����0.1mol/L��V1 L����Һ��pH��1��ϡ����V2 L��ϣ����Ϻ���Һ�����Ϊԭ����Һ���֮�ͣ������û����Һ��pH��2����˵����Ӧ�������ǹ����ģ��� ��0.01����V1��V2��9:11��
��0.01����V1��V2��9:11��
���㣺����ˮ�ĵ��롢ˮ�����ӻ�������pH�ļ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ش��йصζ������е�������⡣
��1������֪Ũ�ȵ�����������Һ�ζ�δ֪Ũ�ȵ����ᣬ�ζ�������ͼ��ʾ��
����ͼ��A��pH��Χʹ�õ�ָʾ����________��
C��pH��Χʹ�õ�ָʾ����________��
�����й��������к͵ζ������еIJ�������ȷ����________������ţ���
| A���ü�ʽ�ζ�����ȡ��֪Ũ�ȵ��ռ���Һ |
| B���ζ��ܺ���ƿ�������ô�װҺ��ϴ |
| C���ζ�������ʼ��ע����ƿ����Һ��ɫ�仯 |
| D����ƿ�еĴ���Һ������Ͳ��ȡ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ijѧ��������֪���ʵ���Ũ�ȵĴ������ⶨδ֪���ʵ���Ũ�ȵ�����������Һʱ��ѡ���ʵ���ָʾ��������д���пհף�
��1���ñ�����ζ����������������Һʱ��������ѡ����ѡ����ǡ����һ��________��
| | ��ƿ����Һ | �ζ�������Һ | ѡ��ָʾ�� | ѡ�õζ��� |
| A | �� | �� | ʯ�� | ���ң� |
| B | �� | �� | ���� | ���ף� |
| C | �� | �� | ��̪ | ���ף� |
| D | �� | �� | ʯ�� | ���ң� |
| | ������������ | 0.100mol/L�������� | |
| �ζ����� | ��Һ�������ml�� | �ζ�ǰ�Ŀ̶ȣ�ml�� | �ζ���Ŀ̶ȣ�ml�� |
| ��һ�� | 25.00 | 0.00 | 24.98 |
| �ڶ��� | 25.00 | 1.56 | 27.86 |
| ������ | 25.00 | 0.22 | 25.24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
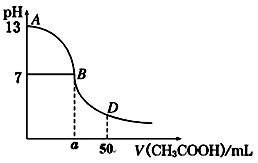
��1����������pH=12��NaCN��Һ�У���ˮ�����c(OH��)Ϊ mol?L��1��
��2��Ũ��Ϊ0.1mol?L��1�����и����ʵ���Һ�У�c(NH4+)�ɴ�С��˳����___������ţ���
��NH4Cl ��NH4HSO4 ��NH3?H2O ��CH3COONH4
��3��ij��Ԫ�ᣨ��ѧʽ��H2A��ʾ����ˮ�еĵ��뷽��ʽ�ǣ�
H2A=H+ +HA����HA�� H+ +A2����
H+ +A2����
����Na2A��Һ��____�ԣ�NaHA��Һ�� �ԣ�����ԡ��������ԡ����ԡ�����
������0.1mo1?L��1Na2A����Һ�����и�������Ũ���ɴ�С��˳���ǣ� ������ţ���
| A��c(Na+)>c(A2��)>c(OH��)>c(HA��)>c(H+) |
| B��c(Na+)> c(OH��)>c(HA��)> >c(A2��) > c(H+) |
| C��c(Na+)> c(H+)> c(A2��)> c(OH��)>c(HA��) |
| D��c(A2��)>c(Na+)> c(OH��) > c(H+)>c(HA��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
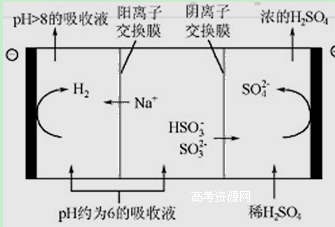
(8��)������������ֿ�ʼ��Ű�ҹ��ֵ���������SO2����ɿ�����Ⱦ����Ҫԭ�������Ƽ�ѭ�����ɳ�ȥSO2��
��1���Ƽ�ѭ�����У�����ҺΪNa2SO3��Һ�������շ�Ӧ�����ӷ���ʽ��
��2����֪H2SO3�ĵ��볣��Ϊ K1��1��54��10-2 , K2��1��02��10-7, H2CO3�ĵ��볣��Ϊ K1��4��30��10-7, K2�� 5��60��10-11,�����������Թ������_____________��
A��CO32- HSO3�� B��HCO3�� HSO3��
C��SO32- HCO3�� D��H2SO3 HCO3��
��3������Һ����SO2�Ĺ����У�pH��n(SO3²��):n(HSO3��)�仯��ϵ���±�:
| n(SO3²��):n(HSO3��) | 91 ��9 | 1 ��1 | 1 ��91 |
| pH | 8��2 | 7��2 | 6��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����pH��2�Ĵ�����Һ��pH��2�������ң���������в���������⣺
(1)ȡ10 mL�ļ���Һ������������ˮ������ĵ���ƽ��________(����������ҡ�����)�ƶ�����ȡ10 mL�ļ���Һ������������ˮ�����ƹ���(����������ǰ����Һ������ֲ���)���������������Һ��[H��]/[CH3COOH]�ı�ֵ��________(���������С������ȷ����)��
(2)��ͬ�����£�ȡ������ļס�������Һ����ϡ��100����ϡ�ͺ����Һ����pH��С��ϵΪ��pH(��)________pH(��)��(����ڡ�����С�ڡ����ڡ�����ͬ)
(3)��ȡ25 mL�ļס�������Һ���ֱ��õ�Ũ�ȵ�NaOHϡ��Һ�к���pH��7�������ĵ�NaOH��Һ�������С��ϵΪ��V(��)________V(��)��
(4)ȡ25 mL�ļ���Һ����������pH��12��NaOH��Һ����Ӧ����Һ��[Na��]��[CH3COO��]�Ĵ�С��ϵΪ��[Na��]________[CH3COO��]��
(5)ȡ25 mL������Һ����������pH��12�İ�ˮ����Ӧ����Һ�е�����Ϊ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������0. 1 mol/L�����¼�����Һ����H2SO4��Һ��NaHSO4��Һ��CH3COOH��Һ��HCl��Һ��HCN��Һ��NH3��H2O���������¼�����Һ�ĵ����(���Ѿ������ռԭ���ܵİٷ���)���±�(��֪H2SO4�ĵ�һ����������ȫ��)���ش���������:
| ��H2SO4��ҺHSO4- | ��NaHSO4��ҺHSO4- | ��CH3COOH | ��HCl��Һ |
| 10% | 29% | 1.33% | 100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
Ϊ��֤��������������ʣ��ס��ҡ����������˷ֱ�ѡ�������Լ�����ʵ�飺
0.01mol/L������Һ��0.1mol/L��������Һ��pH=3�����ᡢpH=3�Ĵ��ᡢ�����ƾ��塢�Ȼ��ƾ��塢���ȡ�pH��ֽ������ˮ��
��1������pH��ֽ���0.10mol/L�Ĵ�����ҺpH=4�����϶�������������ʣ�����Ϊ��һ������ȷ�𣿣����ȷ������ȷ����
��2����ȡ��10ml0.10mol/L�Ĵ�����Һ����pH��ֽ�����pH=a��Ȼ��������ˮϡ�͵�1000mL������pH��ֽ�ⶨ��pH=b��Ҫȷ��������������ʣ���a��bӦ������Ĺ�ϵ�� ���á���ʽ������ʽ����ʾ��
��3����ȡ��10ml0.10mol/L������Һ�����������Һ���Ժ�ɫ���ټ�������ƾ��壬��ɫ���ɫ������Ϊ��һ�����ܷ�֤��������������ʣ�����ܡ����ܡ��� ��
��4������pH��ֽ���ⶨ0.1mol/L��������Һ��pHֵ������0.1mol/L��������Һ��pHֵΪ14�����϶�������������ʣ�����Ϊ��һ������ȷ�𣿣����ȷ������ȷ���� ��
��5���콫pH=3��������ᣬ��ȡ10ml��������ˮϡ�͵�ԭ����100����Ȼ����pH��ֽ�ⶨ����Һ��pH������ı仯С�����϶�������������ʣ�����Ϊ��һ������ȷ�𣿣����ȷ������ȷ���� ��
��6������pH=3��������ᣬ�ֱ������Ӧ�����ι��壬�����PH�仯�����϶�������������ʣ�����Ϊ��һ������ȷ�𣿣����ȷ������ȷ���� ��
��7����ȡpH=3������ʹ��ᣬ�ֱ�ϡ�͵�ԭ����100����Ȼ�������ȫһ����п��������ų�H2�����ʿ죬���϶�������������ʣ�����Ϊ��һ������ȷ�𣿣����ȷ������ȷ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�����£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH�����±���
| ʵ���� | HA���ʵ���Ũ��(mol��L-1) | NaOH���ʵ���Ũ��(mol��L-1) | �����Һ��pH |
| �� | 0.1 | 0.1 | pH��9 |
| �� | c | 0.2 | pH��7 |
| �� | 0.2 | 0.1 | pH��7 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com