
����Ŀ������һ�����ȼ������ۺ���������ĩ�Ļ����ڸ�����ʹ֮��ַ�Ӧ������Ӧ��Ĺ����Ϊ���ȷݣ���������ʵ�飨����Ũ��ʱ�ٶ���Һ���û�б仯����
��������һ�ݹ����м���100mL 2.0mol/L��NaOH��Һ������ʹ���ַ�Ӧ����ˣ������Һ��c��OH-����1mol/L��
������һ�ݹ����м���140mL 4��0 mol/L��HCl��Һ��ʹ����ȫ���ܽ⣬��÷�Ӧ��������Һ��ֻ��H+��Fe2+��Al3+������������c��H+��=1mol/L��
��1��д�������ȷ�Ӧ�Ļ�ѧ����ʽ��_______________________________
д��ʵ��ٷ��������ӷ���ʽ��_________________________________��
��2��������ȼ������۵�����Ϊ___________________________��
��3��������ȼ�����������ĩ������Ϊ__________________________________��
���𰸡� 2Al+Fe2O3![]() 2Fe+Al2O3 Al2O3+2OH-=AlO2-+2H2O��2Al+2H2O+2OH-=2AlO2-+3H2�� 5.4g 9.6g
2Fe+Al2O3 Al2O3+2OH-=AlO2-+2H2O��2Al+2H2O+2OH-=2AlO2-+3H2�� 5.4g 9.6g
����������1�����ȷ�Ӧ�������������ڸ��������·�Ӧ������������������Ӧ�Ļ�ѧ����ʽΪ��2Al+Fe2O3![]() 2Fe+Al2O3��ʵ������ȷ�Ӧ��Ļ�����������������ã�����ֻ����������δ��Ӧ�������������Ʒ�Ӧ�����������ӷ���ʽ�У�Al2O3+2OH-=AlO2-+2H2O��2Al+2H2O+2OH-=2AlO2-+3H2����ʵ�������ȥn(NaOH)��100mL��(2.0mol/L��1.0mol/L)��0.1mol��������Al����Al2O3����NaOH��Һ��Ӧ������NaAlO2�����ȼ�����n(Al)��n(NaOH)��2��0.2mol��m(Al)��5.4g��ʵ���������Һ�У����ݡ�����غ㡱��n(H+)��2��n(Fe2+)��3��n(Al3+)��n(Cl��)����n(Fe2+)��
2Fe+Al2O3��ʵ������ȷ�Ӧ��Ļ�����������������ã�����ֻ����������δ��Ӧ�������������Ʒ�Ӧ�����������ӷ���ʽ�У�Al2O3+2OH-=AlO2-+2H2O��2Al+2H2O+2OH-=2AlO2-+3H2����ʵ�������ȥn(NaOH)��100mL��(2.0mol/L��1.0mol/L)��0.1mol��������Al����Al2O3����NaOH��Һ��Ӧ������NaAlO2�����ȼ�����n(Al)��n(NaOH)��2��0.2mol��m(Al)��5.4g��ʵ���������Һ�У����ݡ�����غ㡱��n(H+)��2��n(Fe2+)��3��n(Al3+)��n(Cl��)����n(Fe2+)��![]() ��0.06mol�����ȼ���n(Fe2O3)��n(Fe2+)��
��0.06mol�����ȼ���n(Fe2O3)��n(Fe2+)��![]() ��2��0.06mol��m(Fe2O3)��9.6g��
��2��0.06mol��m(Fe2O3)��9.6g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50mL0.50molL��1������50mL0.55molL��1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȣ��ش��������⣺ 
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��
��2����ʵ������У���ͬѧ��Ҫ�ⶨ����¼��ʵ��������������ţ���
A.�����Ũ��
B.������¶�
C.����������Һ��Ũ��
D.����������Һ���¶�
E.ˮ�ı�����
F.��Ӧ������Һ����ֹ�¶�
��3���кͷ�Ӧ������ʵ���¶�ƽ������3.4�森��֪�кͺ����ɵ���Һ�ı�����Ϊ4.18J/��g�棩���������Һ���ܶȾ�Ϊ1g/cm3 �� ͨ������ɵ��к��ȡ�H=
��4��ʵ���и���60mL0.50molL��1�����50mL0.55molL��1NaOH��Һ���з�Ӧ����������ȷ��ʵ�������ȣ����ų������������ȡ�����ȡ����������к��������ȡ�����ȡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������У�����ȷ������ ��
A. ����������С���и��ʣ�����Ӧ�Ż�ú����
B. ����ƿʹ��ǰ��Ҫ��©
C. ��ͷ�ιܵμ�Һ��ʱһ�������������Ͽ��в�
D. ��������ƽ������ֽ����4.20 g �ռ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ����1��C��s��+O2��g���TCO2��g����H=��393.5kJ/mol
��2��CO��g��+ ![]() O2��g���TCO2��g����H=��283.0kJ/mol
O2��g���TCO2��g����H=��283.0kJ/mol
��Ӧ��C��s��+ ![]() O2��g���TCO��g���ġ�H �ǣ� ��
O2��g���TCO��g���ġ�H �ǣ� ��
A.��221 kJ/mol
B.��110.5 kJ/mol
C.+110.5 kJ/mol
D.+221 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӹ����������仯�������������������е����÷����˾�ı䡣
��1���Ŵ��й��Ĵ���֮һ��ָ����������Ȼ��ʯ�Ƴɵģ�����Ҫ�ɷ���(����ĸ���)��
a��Fe b��FeO c��Fe3O4 d��Fe2O3
��2������������Ҫ��ѧ�ɷ�Ϊ��SiO2Լ45%��Fe2O3Լ40%��Al2O3Լ10%��MgOԼ5%���ø÷�����ȡҩ�ø��ϡ������������Ĺ�����������(���ֲ�����������)��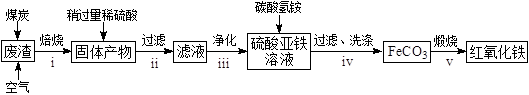
�ش��������⣺
���ڲ���i�в������ж������������
���ڲ���iii�����У�Ҫ��ȥ������֮һΪAl3+��������ʱKsp[Al(OH)3]=1.0��1032 �� ��ʱ�����Ͻ�Al3+������ȫ������Һ��pHΪ��
�۲���iv�У�����FeCO3�����ӷ���ʽ����
��3���Ȼ�����Һ��Ϊ��ѧ�Լ��еġ������֡������Ȼ�ͭ���Ȼ����Ļ����Һ�м�������ͭ��ĩ�����������д���ó����Ļ�ѧʽ������ƽ���ƶ���ԭ������ϱ�Ҫ�����ӷ���ʽ���Դ���������������
��4���ٹ��϶��������ɫȾ����³ʿ���ĺϳɷ������£�
���ֽⷴӦii�����ӷ���ʽ����
����������³ʿ���ϳ�ԭ���ɼ��ʳƷ���Ƿ�CN �� �������£�![]()
����ֽ������֤��ʳƷ�к���CN �� ����ͼ��ʱ��ֽ��FeSO4��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʪ���KI������ֽ�Ӵ�ij���������ɫ���������п�����()
��Cl2��NO2��H2S��SO2��HCl��������
A.�٢ۢ�
B.�٢ڢ�
C.�٢ڢ�
D.�ڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����5mol��L-1����10mLϡ�͵�200mL����ȡ��5mL����5mL��Һ�����ʵ���Ũ���ǣ� ��
A. 0.05mol��L-1B. 0.25mol��L-1C. 0.1mol��L-1D. 0.5mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ��װ�ú�����ʵ�鲽�裬������ȡ�������屽�������飮��֪�Ҵ���һ���������������ᷴӦ���Ʊ������飺
C2H5OH+HBr��C2H5Br+H2O
��Ҫʵ�鲽�����£������Ӻ�װ�ã����װ�õ������ԣ�������ƿ�м���һ�����ı���Һ�壮����ƿ�м����Ҵ���ŨH2SO4�Ļ��Һ���Ը��ڽ������ܿڴ����۽�Aװ���еĴ���˿С�����²�����Һ�У��ܵ�ȼBװ���еľƾ��ƣ���С������ƿ����10min��
����д���пհף�
��1��д����ȡ�屽�Ļ�ѧ����ʽ�� ��
��2��������й۲쵽�������ǣ� ��
��3��Cװ����U�ι��ڲ�������ˮ��ס�ܵ������ǣ� ��
��4����Ӧ��Ϻ�U�ι��ڵ������ǣ� �� ����������ʱ���õ�����Ҫ�����������ǣ�ֻ��һ�֣� ��
��5��ʵ�����������ƿ�Ļ�����з�������ƻ�ɫ���屽��������ɫ��ԭ�������к������ѧʽ�������õ���ɫ���屽�ķ����������Լ��Ͳ������ƣ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com