
���º��������£����������в��ǿ��淴Ӧ2A��g��+3B��s��⇌2C��g���ﵽƽ��ı�־���ǣ�������
��C������������C�ķֽ�������ȣ�
�ڵ�λʱ������amol A��ͬʱ����1.5amol B��
�۸���ֵ�Ũ�Ȳ��ٱ仯��
�ܻ��������ܶȲ��ٱ仯��
�ݻ���������ѹǿ���ٱ仯��
�����������ʵ������ٱ仯��
��������ƽ��Ħ���������ٱ仯��
��A��B��C�ķ�����Ŀ��Ϊ2��3��2��
| �� | A�� | �ݢޢ� | B�� | �ڢݢ� | C�� | �٢ۢ� | D�� | �ڢܢ� |
| ��ѧƽ��״̬���жϣ�. | |
| ר�⣺ | ��ѧƽ��ר�⣮ |
| ������ | ��ѧ��Ӧ�ﵽƽ��״̬�ı�־�ǣ�����ֵ�����Ũ�ȣ����ٱ仯���淴Ӧ������Ӧ������ȣ�������Щ�ҳ����жϴﵽƽ��״̬��ѡ� |
| ��� | �⣺��C������������C�ķֽ�������ȣ����淴Ӧ������ȣ��ﵽ�˻�ѧƽ�⣬�ʢٲ���ѡ�� �ڵ�λʱ������amol A�������淴Ӧ���ʣ�ͬʱ����1.5amol B����������Ӧ���ʣ������ʵ����ı仯֮�ȵ��ڻ�ѧ������֮�ȣ�����淴Ӧ������Ӧ������ȣ��ﵽ�˻�ѧƽ�⣬�ʢڲ���ѡ�� ��A��B��C��Ũ�Ȳ��ٱ仯���ﵽ��ƽ��״̬���ʢ۲���ѡ�� ������BΪ���壬��˷�Ӧǰ������������仯�������������������䣬�����ܶȱ仯����˻��������ܶȲ��ٱ仯˵���ﵽƽ��״̬���ʢܲ���ѡ�� ��Ӧǰ������Ļ�ѧ��������ȣ�����ں��º���������ѹǿ��һ��ֵ������������ѹǿ���ٱ仯����˵���ﵽƽ��״̬���ʢݿ�ѡ�� ��Ӧǰ������Ļ�ѧ��������ȣ������������ʶ��Դ˷�Ӧ���ڵ����ʵ����ķ�Ӧ����˻����������ʵ������ٱ仯����˵���ﵽƽ��״̬���ʢ�ѡ�� �߷�Ӧǰ������Ļ�ѧ��������ȣ����ʵ������䣬����BΪ���壬��˷�Ӧǰ������������仯����˻�������ƽ��Ħ������Ϊ�Ա仯��ֵ������������ƽ��Ħ���������ٱ仯˵���ﵽƽ��״̬���ʢ߲���ѡ�� ��A��B��C�ķ�����Ŀ��Ϊ2��3��2���Ȳ���˵������ֵ�Ũ�Ȳ��ٱ仯���ֲ����淴Ӧ������Ӧ������ȣ���˲���˵���ﵽ��ѧƽ��״̬���ʢ��ѡ�� ��ѡ��A�� |
| ������ | ���⿼���˻�ѧƽ��״̬���жϣ����淴Ӧ������ȣ������Ũ�Ȳ��ٱ仯���ﵽƽ��״̬�������Ѷ��еȣ���һ���仯�ġ��������ٱ仯ʱ��˵���ﵽ�˻�ѧƽ��״̬�� |


 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��H2(g)��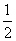 O2(g)===H2O(g)��
O2(g)===H2O(g)��
��H����Q1 kJ��mol��1
2H2(g)��O2(g)===2H2O(l)����H����Q2 kJ��mol��1
�������ж���ȷ���� (����)
A��2Q1��O2������B��Q1��2Q2 C��2Q1��Q2 D.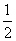 Q2��Q1
Q2��Q1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ݻ�Ϊ1 L���ܱ������У���CO��ˮ�����Ļ��������ȵ�800 ��ʱ��
������ƽ��CO(g)��H2O(g) 
 CO2(g)��H2(g)����K��1������2 mol CO
CO2(g)��H2(g)����K��1������2 mol CO
��10 mol H2O(g)���ϲ����ȵ�800 �棬��CO��ת����Ϊ(����)
A��16.7% B��50% C��66.7% D��83.3%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ� ��
A����100 mL 3 mol/L��H2SO4��100 mL ˮ��ϣ���������ʵ���Ũ�ȱ�Ϊ1.5 mol/L
B����200 mL 3 mol/L��BaCl2��Һ��100 mL 3 mol/L��KCl��Һ��Ϻ���Һ�е�c(Cl-)��Ȼ��3 mol/L
C����100 g 20%��NaCl��Һ��100 g H2O��Ϻ�NaCl��Һ������������10%
D����100 mL 1 mol/L��NaOH��Һȡ��10 mL��NaOH��Һ��Ũ�ȼ�С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ� ��
A���������ǵ���ʵı�����������ˮ��Һ���ۻ�״̬���ܷ����
B��ǿ�������������ʵı�����������ˮ��Һ�����Եļ���
C���ᡢ���������ڵ���ʣ����������ﶼ�Ƿǵ����
D��������ǿ�ᡢǿ��ʹ��ζ���ǿ����ʣ����������ﶼ�Ƿǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NH3•H2O⇌NH4++OH���γɵ�ƽ���У�ҪʹNH3•H2O�ĵ���̶ȼ�c��OH���������ɲ�ȡ�Ĵ�ʩ�ǣ�������
| �� | A�� | ͨ��HCl | B�� | ������NaOH���� |
| �� | C�� | �������Ȼ�粒��� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�£�H2N��NH2����һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯��ͼ��ʾ����֪����1mol��ѧ�������������kJ����N��NΪ942��O=OΪ500��N��NΪ154�������1molN��H�������������kJ���ǣ�������
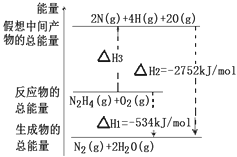
| �� | A�� | 194 | B�� | 391 | C�� | 516 | D�� | 658 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ�뽺�������ص���
A�����ð�Ĥ��ȥ������Һ�е�����NaCl
B���ƺ��뺣�������γ�ɳ��
C����ֲ���͵���ˮ������������γ���ˮ�����
D��һ��ƽ�й���ͨ����������Һ���Ӳ�����Կ���һ��������ͨ·
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ɫ����ǿ������Һ�п��Դ����������������( )
A.Na+��NO3-��Mg2+��Cl- B.Na+��CO32-��NO3-��Ca2+
C.K+��Cl-��SO42-��Cu2+ D.Ba2+��Cl-��K+��SO42-
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com