
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。
X | Y | ||||
Z | W | Q | |||
(1)Q的原子结构示意图是________。
(2)Y、Z、W形成简单离子,其离子半径关系为________(用离子符号表示)。
(3)用有关离子方程式表示Q、W元素的非金属性强弱______________
(4)Y的氢化物分子中含有18个电子,该分子中的共价键类型_____________________________。
(5)W的最高价氧化物对应的水化物的浓溶液与Cu反应的化学方程式为________________________。
【答案】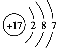 S2->O2->Al3+ S2-+Cl2===2Cl-+S↓ 极性共价键、非极性共价键 Cu+2H2SO4(浓)
S2->O2->Al3+ S2-+Cl2===2Cl-+S↓ 极性共价键、非极性共价键 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
【解析】
由图可知X、Y、Z、W、Q分别是N、O、Al、S、Cl,依据这些元素单质和化合物性质可解。
(1) Cl的原子结构示意图是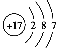 ;
;
(2) O、Al、S形成简单离子,S2-有三层电子,O2-和Al3+均有两层电子,但是O的核电荷数小,所以其离子半径关系为S2->O2->Al3+;
(3)氧化性氯气大于硫,表示S、Cl元素的非金属性强弱有关离子方程式:S2-+Cl2===2Cl-+S↓;
(4) O的氢化物分子中含有18个电子为H2O2,该分子中的共价键类型为极性共价键和非极性共价键;
(5) S的最高价氧化物对应的水化物的浓溶液为浓硫酸,与Cu反应的化学方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】分子式为C9H12的苯的同系物,已知苯环上只有一个取代基,下列说法中正确的是 ( )
A. 该有机物能发生加成反应,但不能发生取代反应
B. 该有机物不能使酸性高锰酸钾溶液和溴水褪色
C. 该有机物分子中的所有原子不可能在同一平面上
D. 该有机物的一溴代物最多有5种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是人体健康必需的一种微量元素。已知Se的原子结构示意图为: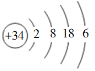 。下列说法不正确的是
。下列说法不正确的是
A. 该原子的质量数为34B. 该元素处于第四周期第ⅥA族
C. SeO2既有氧化性又有还原性D. 酸性:HBrO4 > H2SeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制备合成氨原料气过程中存在反应: CO(g)+H2O(g) ![]() CO2(g)+ H2(g)+ 41.0kJ,下列判断正确的是( )
CO2(g)+ H2(g)+ 41.0kJ,下列判断正确的是( )
A. 该反应的正反应是吸热反应
B. 反应物总能量小于生成物总能量
C. 反应中生成1 mol H2(g)放出41.0kJ热量
D. 反应中消耗1体积CO(g)放出41.0kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列情况中,会对人体健康造成较大危害的是 ( )
A.用SO2漂白食品B.用小苏打发酵面团制作馒头
C.用食醋清洗热水瓶胆内壁附着的水垢D.用ClO2对自来水进行杀菌消毒。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3的反应
C. Fe(SCN)3溶液中加入固体KSCN后颜色变深
D. 由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4) 是有机合成的重要还原剂。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质) 为原料制备铝氢化钠的一种工艺流程如下:
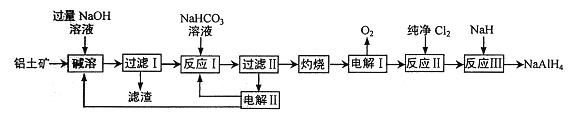
注: SiO2在“碱溶”时转化为铝硅酸钠(Na2Al2SixO8) 沉淀。
(1)铝硅酸钠(Na2Al2SixO8) 可以用氧化物的形式表示其组成,形式为________。
(2) “过滤I”中滤渣主要成分有________(写名称)。向“过滤I”所得滤液中加入NaHCO3溶液,反应的离子方程式为_______________、______________。
(3) “电解I”的另一产物在1000℃时可与N2反应制备AlN,在这种产物中添加少量NH4Cl固体并充分混合,有利于AlN 的制备,其主要原因是__________________。
(4)“电解II”是电解Na2CO3溶液,原理如图所示。
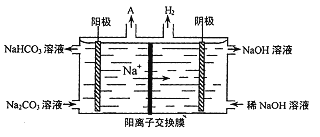
阳极的电极反应式为_________________。
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为_____________,每产生1mol 气体转移电子数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)![]() pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
①m+n>p ②x点表示的正反应速率大于逆反应速率
③x点比y点时的反应速率慢 ④n>p
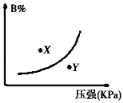
A. ①② B. ②④ C. ②③ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶须是由高纯度单晶生长而成的微纳米级的短纤维,工业应用的晶须主要是在人工控制条件下合成。
碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域。制取碳酸镁晶须的步骤如图:
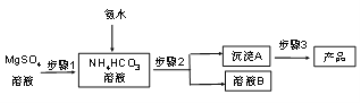
完成下列填空:
(1)步骤1必须将反应的温度控制在50℃,较好的加热方法是_______________________;氨水、硫酸镁、碳酸氢铵三者反应,除生成MgCO3·nH2O沉淀外,同时生成的产物还有______________________________________。
(2)步骤2是__________、洗涤,检验沉淀A已洗涤干净的方法是_____________________。
为测定碳酸镁晶须产品中n的值,某兴趣小组设计了如下装置,并进行了三次实验。(不考虑稀盐酸的挥发性)
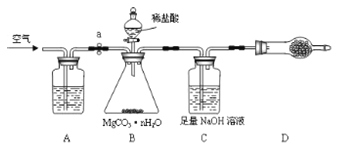
(3)装置A中盛放的溶液是_____________。装置D中盛放的固体是___________________,其作用是_________________________________。
(4)若三次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为__________________(用含a的代数式表达)。
(5)下列选项中,会造成实验结果偏大的是____________。 (选填序号)
①实验开始,未先通空气,即称量装置C; ②B中反应结束后,没有继续通空气;
③缺少装置A; ④缺少装置D;
⑤装置B中稀盐酸的滴加速率过快; ⑥装置C中的NaOH溶液浓度过大。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com