
����Ŀ����ѧ������ָ��ʹ���������������������ԭ�����������Ƽ��ı���������һ�����ķ�������������(NaH2PO2)����ѧ��������Ҫԭ������ҵ���Ʊ�NaH2PO2��H2O������������

�ش���������:
����������(NaH2PO2)�Ǵ�����(H3PO2)������NaOH��Һ��Ӧ�IJ�����NaH2PO2����_______(��������������ʽ��������ʽ�������� NaH2PO2����Ԫ���Ļ��ϼ�Ϊ___________��
(2)����Ӧ���м����黯��������������Ŀ����________________
(3)�ڷ�Ӧ���з��������Ӧ�����а���(P4)��Ca(OH)2��Ӧ���ɴ������Ƽ�������Ļ�ѧ����ʽΪ_________________________
(4)������ͨ��CO2��Ŀ����______________������X�Ļ�ѧʽΪ_____________
(5)������ĸҺ�е����ʳ�NaH2PO2�⣬���е�һ����Ҫ�ɷ�Ϊ_____________
(6)��PH3�ķ�������NaClO��NaOH�������Һ��������ת��Ϊ���������÷�Ӧ�����ӷ���ʽΪ____________
(7)ij������Ͷ���ԭ�ϰ���Ϊ1240 kg���������黯��Ӧ������80%�İ���ת��Ϊ�������Ƽ������������������������ʧ�����������յõ���ƷNaH2PO2��H2O������ӦΪ__________kg(NaH2PO2��H2O����Է�������Ϊ106)
���𰸡� ���� +1 �ӿ췴Ӧ���� 2P4+3Ca(OH)2+6H2O=3Ca(H2PO2)2+2PH3�� ��Ca(H2PO2)2 ת��ΪNaH2PO2 CaCO3 Na2HPO3 PH3+4ClO-+3OH-=PO43-+4Cl-+3H2O 2544
�����������⿼�黯ѧ�������̣��漰����ѧ��Ӧԭ����֪ʶ�����ã���1�����������Ǵ��������������������Ʒ�Ӧ�IJ����˴������������Σ�����Na�ԣ�1�ۣ����ԣ�1�ۣ����ԣ�2�ۣ��������ϼ۵Ĵ�����Ϊ0��P�Ļ��ϼ��ǣ�1�ۣ���2�������Ŀ�������ӽӴ���������ٷ�Ӧ���ʣ���3������P4��Ca(OH)2��Ca(H2PO2)2��PH3��P4��Ca(H2PO2)2��P�Ļ��ϼ���0����1�ۣ�����1�ۣ�������2�ۣ�P4��PH3��P�Ļ��ϼ���0����3�ۣ�����3�ۣ���С������Ϊ6����Ca(H2PO2)2ϵ��Ϊ3��PH3��ϵ��Ϊ2������ԭ���غ㣬��Ӧ����ʽΪ2P4��3Ca(OH)2=3Ca(H2PO2)2��2PH3����4��CO2��NaOH��Ӧ����Na2CO3��̼���������ˮ��ͨ��CO2��Ŀ���dz�ȥCa2��������Ca(H2PO2)2 ת��ΪNaH2PO2 ��������XΪCaCO3����5����������ͼ��ĸҺ�л�����NH2HPO3����6������ClO��������������PH3������PO43����PH3��ClO����PO43����Cl����P�Ļ��ϼ��ɣ�3�ۡ���5�ۣ����ϼ�����8�ۣ�Cl�ɣ�1�ۡ���1�ۣ�����2�ۣ���С������Ϊ8��PH3��4ClO����PO43����4Cl���������Ǽ��ԣ�����ѭ��Ӧǰ�����������������ȣ���PH3��4ClO����3OH��=PO43����4Cl��+3H2O����7������������Ӧ��������ϵʽ��2P4��3Ca(H2PO2)2��6NaH2PO2��H2O��m(NaH2PO2��H2O)=1240��80%��6��106/(31��4��2)kg=2544kg��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�о��������ϳɰ���Ӧ��T��ʱ�����ݻ�Ϊ2 L����������ͨ��4 mol N2��12mol H2����Ӧ���£� N2(g)+3H2(g) ![]() 2NH3(g) ��H=-92.0kJmol-1����ؼ����������£�
2NH3(g) ��H=-92.0kJmol-1����ؼ����������£�
N��N | H-H | N-H | |
��������( kJ/mol) | 946 | 436 | X |
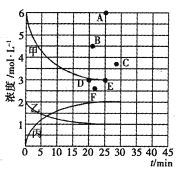
��25minʱ��Ӧ�ﵽƽ�⣬������Ũ����ʱ��仯��������ͼ�мס��ҡ������ش��������⣺
(1)0-25min�ڣ���Ӧ��ƽ������v(H2)Ϊ_________������X=_________________��
(2)T��ʱ���÷�Ӧ��ƽ�ⳣ��K=_____________ ���������������
(3)T��ʱ������ʼ����8mol N2��24 mol H2����Ӧ�մﵽƽ��ʱ����ʾc( H2)����ͼ����Ӧ�ĵ�Ϊ_____������ĸ����
(4)��úΪ��Ҫԭ�ϵĺϳɰ���ҵ�У�ԭ����������������������ã�
��C(s) +H2O(g)![]() CO(g) +H2(g) ��H1
CO(g) +H2(g) ��H1
��CO(g) +H2O(g)![]() CO2(g) +H2(g) ��H2
CO2(g) +H2(g) ��H2
����֪CO��H2��ȼ���ȷֱ�Ϊ283 kJ��mol-l��285.8kJ��mol-l��H2O( g) =H2O(1) ��H =-44kJ��mol-l ���H2=_______________��
(5)�����������������Ҫԭ�ϣ���������£�
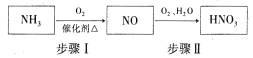
д������I�Ļ�ѧ����ʽ��_________________��
(6)��ͼ�ǿ�ѧ����������õ�ⷨ���³�ѹ���ɵ����������ϳɰ���ʾ��ͼ��
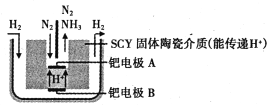
��ͼ��֪���ٵ缫B�ǵ��ص�________����������������������ٵ缫A�ϵĵ缫��ӦʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵ����ʺ�Ӧ�ö���ȷ���ǣ� ��
A.MgO��Al2O3�۵�ߣ��������������ͻ����
B.�����Լ��ԣ����ü�ʯ�һ���ˮCaCl2����
C.��������ǿ���ԣ������ڵ�̲���
D.ͭ�Ļ�Ա����������ں��������װͭ���Լ������ָ�ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʯ���۵����ʯī��ԭ������� �� ��
A.ʯī�л��з��»���
B.ʯī�ۻ�ҲҪ�ƻ����ۼ����Ҽ�������
C.ʯī���ȶ��Ը���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ı�����ȷ���ǣ� ��
A. ԭ�Ӻ�����10�����ӵ���ԭ�ӣ�![]() O
O
B. ��ԭ�ӵĽṹʾ��ͼ��![]()
C. Fe3+�����������Ų�ʽΪ��3s23p63d5
D. ��̬ͭԭ�ӵ���Χ�����Ų�ͼ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ѻ��Ҵ���ͬ���칹�壬�����ɲ��û�ѧ�������������������м����в��ܶԶ��߽��м������
A. ���ý����ƻ��߽����� B. ���ú������
C. �������� D. ���ú˴Ź�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH3CH=CH��C��N������̼ԭ�ӵ��ӻ�����Ϊ�� ��
A. sp�ӻ�B. sp2�ӻ�C. sp3��sp2�ӻ�D. sp��sp3��sp2�ӻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C����װ�ö�������ȡ�屽������A����������Ʊ�װ�ã�B��C�ǸĽ����װ�ã�����ϸ�������Ա�����װ�ã�Ȼ��ش��������⣺

��1��д������װ���ж������ķ�Ӧ�Ļ�ѧ����ʽ��__________��___________��
��2��װ��A��C�о������˳��������ܣ���������_____________________________��
��3��װ��B��C�Ϻõؽ����װ��A�д��ڵļ�ҩƷ�ͼ�ʱ�ܷ��ì�ܣ������˲�����װ��A����һ������ʵ��������ɵIJ��������________________________________��
��4��װ��B�в�����ϴ��ƿ����װ�ã���������_______________________��
��5��װ��B��Ҳ�����������Ե�ȱ�㣬ʹʵ���Ч�����û����������С�������ȱ����
___________________________��________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ����ͭ�����ҪƷ��֮һ��ͳ�Ļ�ұ������Դ���ۺ����á����������ȷ�����������ѡ���ͭ���ʪ��ұ��Ŀǰ�����ⶼ����̽���Ρ����������������뷨��һ�ֽ�Ϊ�����ʪ��ұ��������������������ͼ��ʾ��
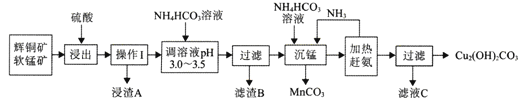
��֪��
�� ��ͭ�����Ҫ�ɷ���Cu2S,���н϶��Fe2O3��SiO2�ȡ�
�� ���̿����Ҫ�ɷ���MnO2�����н϶��SiO2�ȡ�
�� ����ʱ������һ�ַǽ������ʡ�
�� �����£�Kap[Fe(OH)3]=4.0��10-38mol/L��Kap[Fe(OH)2]=8.0��10-16mol/L
���������գ�
(l������ǰ��Ҫ�Ƚ���ʯ���飬��Ŀ����__________��
(2��дɽ����ʱ��Ҫ��Ӧ�����ӷ���ʽ_____________��
(3������A����Ҫ�ɷ�Ϊ_______������ҺpH 3.0-3.5��Ŀ���dz�ȥ______���ӣ������£��������ӵ�Ũ��Ϊ4.0��10-8mol/L������Һ��pH=__________��
(4) ��ҵ�Ͽɽ�MnCO3����300��������������ȡ���нϺô����ܵ�MnO2����MnCO3�ڿ�����������ȡMnO2�Ļ�ѧ����ʽΪ_________________��
(5������ҺC����ȡ���ᰱ����IJ���Ϊ_______��_______�����ˡ�ϴ�ӡ��ɲ١�
(6�����ұ����ͭ����ȣ���ͼ�з���ұ����ͭ����ŵ���________��_____�����о�����2����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com