
【题目】利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是 ( ) 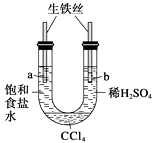
A.a管发生吸氧腐蚀,b管发生析氢腐蚀
B.一段时间后,a管液面高于b管液面
C.a处溶液的pH增大,b处溶液的pH减小
D.a、b两处具有相同的电极反应式:Fe-2e-= Fe2+
【答案】C
【解析】
A.U型管左边装置是中性溶液,所以发生吸氧腐蚀,右边装置是酸性溶液发生析氢腐蚀,故A不符合题意;
B.左边装置发生吸氧腐蚀时,氧气和水反应导致气体压强减小,右边装置发生析氢腐蚀,生成氢气导致气体压强增大,所以右边的液体向左边移动,所以一段时间后,a管液面高于b管液面,故B不符合题意;
C.a处铁失电子生成亚铁离子,氧气得电子和水反应生成氢氧根离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁沉淀,所以a处pH不变;b处溶液变成硫酸亚铁溶液,溶液的pH值变大,故C符合题意;
D.a、b两处构成的原电池中,铁都作负极,所以负极上具有相同的电极反应式:Fe-2e-=Fe2+ , 故D不符合题意;
故选C。四氯化碳隔开了U型管两端,且装置是密封体系。a管发生铁的吸氧腐蚀,b管发生铁的析氢腐蚀。分析腐蚀原理解题即可。


科目:高中化学 来源: 题型:
【题目】软锰矿(主要成分是MnO2)与浓盐酸混合加热,产生了氯气。某学生使用这一原理设计如图所示的实验装置,并且利用制得的氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:

(1)A仪器的名称是__________
(2)漂白粉将在U形管中产生,其化学方程式是____________________。
(3)此实验结果所得Ca(ClO)2产率太低,经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是______________________________。
②试判断另一个副反应(写出此反应方程式):____________________。
(4)漂粉精同盐酸作用产生氯气:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,该反应中每生成1molCl2,转移电子的物质的量为__________mol。
(5)有效氯是漂粉精中有效Ca(ClO)2的含量大小的标志。已知:有效氯=(漂粉精加盐酸所释放出的氯气的质量/漂粉精的质量)![]() 100%,该漂粉精的有效氯为65%,则该漂粉精中Ca(ClO)2的质量分数为__________(保留一位小数)
100%,该漂粉精的有效氯为65%,则该漂粉精中Ca(ClO)2的质量分数为__________(保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,以制取乙酸乙酯。
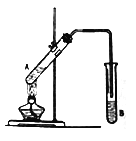
(1)试管A中的液体由以下试剂混合而成:①2mL乙醇;②3mL浓硫酸;③2mL 乙酸。一般况下,这三种试剂的加入顺序是:先加入________(填序号,下同),再加入_________,最后加入③。
(2)为防止试管A中的液体在实验时发生暴沸,在加热前还应加入碎瓷片。若加热后发现未加入碎瓷片,应采取的补救措施是:_________________________________________________________。
(3)试管B中盛放的试剂是___________________;反应结束后,分离B中的液体混合物需要用到的玻璃仪器主要是_____________。试管B中的导管末端不伸入液面下方的目的是_______________。
(4)试管 A中CH3COOH与C2H518OH反应的化学方程式为:___________________________________。
(5)该实验中用30gCH3COOH与46gC2H5OH反应,如果实际得到的乙酸乙酯的质量是26.4g,该实验中乙酸乙酯的产率是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列化学方程式或离子方程式。
(1)利用铝热反应焊接钢轨的化学方程式为_________________________。
(2)实验室利用二氧化锰和浓盐酸制取氧气的化学方程式为__________________。
(3)乙醇与金属钠反应的化学方程式为___________________________。
(4)苯与浓硫酸和浓硝酸混合液共热制取硝基苯的化学方程式为__________________。
(5)氯化铝溶液与氨水制备氢氧化铝的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米材料一直是人们研究的重要课题,例如纳米级Fe粉表面积大,具有超强的磁性,高效催化性等优良的性质。
I、实验室采用气相还原法制备纳米级Fe,其流程如图所示:
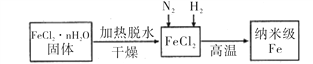
(1)纳米级Fe和稀盐酸反应的离子方程式为_______________________________。
(2)如何将FeCl2·nH2O固体加热脱水制得无水FeCl2 _____________________________________(用简要文字描述)。
(3)生成纳米级Fe的化学方程式为______________________________________。
II、查阅资料:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570℃时生成FeO,高于570℃时生成Fe3O4。甲同学用如图甲装置所示进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。

(4)甲装置中纳米级Fe粉与水蒸气反应的化学方程式是 ______________________。
(5)甲装置中仪器a的名称为_______________________。
(6)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
实验步骤 | 实验操作 | 实验现象 |
I | 将反应后得到的黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
II | 向实验I得到的溶液中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
根据以上实验,乙同学认为该条件下反应的固体产物为FeO。
丙同学认为乙同学的结论不正确,他的理由是______(用简要文字描述)。
(7)丁同学称取5.60gFe粉,用乙装反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88g,则丁同学实验后的固体物质中氧化物的质量分数为________(结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B3N3H6与C6H6是等电子体,则下列说法不正确的是( )
A. B3N3H6能发生加成反应和取代反应 B. B3N3H6具有碱性
C. B3N3H6各原子在同一平面上 D. B3N3H6不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 分子式为C3H6Cl2的有机物有4种同分异构体(不考虑立体异构)
B. ![]() 和
和![]() 互为同系物
互为同系物
C. 乙炔和溴的四氯化碳溶液反应生成1,2-二溴乙烷
D. 甲苯分子中所有原子都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式书写正确的是( )
A.CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l) ΔH=+725.76 kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=+725.76 kJ·mol-1
B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1451.52 kJ·mol-1
C.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-725.76 kJ·mol-1
D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=+1451.52 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2、CO、CH4、CH3OH等都是重要的能源,也是重要为化工原料。
(1)已知25℃,1.01×105Pa时,8.0g CH4完全燃烧生成二氧化碳气体和液态水放出444.8kJ热量。写出该反应的热化学反应方程式:___________________________________________。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,工业上可以用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
CH3OH(g) + H2O(g)。经测得CO2和CH3OH(g)的物质的量随时间变化如图所示。
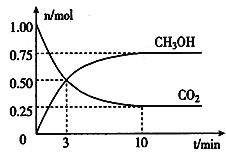
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________________。
②达到平衡时,H2的转化率为__________。
③该反应的平衡常数K=___________________(表达式)。
④下列措施不能提高反应速率的是__________。
A.升高温度 B.加入催化剂 C.增大压强 D.及时分离出CH3OH
(3)工业上也用CO和H2为原料制备CH3OH,反应方程式为:CO(g) + 2H2(g)![]() CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是______。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1 mol CO,同时生成1 mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com