
【题目】下列实验方案能达到实验目的的是
A | B | C | D | |
实验方案 |
置于光亮处 |
|
|
|
实验目的 | 验证甲烷与氯气发生化学反应 | 中和热的测定 | 验证乙炔的还原性 | 验证铁钉发生析氢腐蚀 |
A.AB.BC.CD.D
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案科目:高中化学 来源: 题型:
【题目】钴酸锂(LiCoO2)可用作锂离子电池的电极材料。以红土镍矿为原料制备LiCoO2的工艺流程如图:
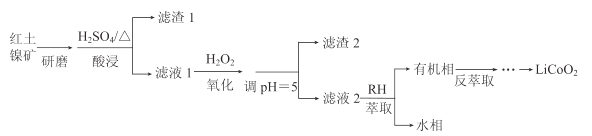
已知:①红土镍矿的主要成分有Fe2O3、FeO、SiO2、Al2O3、CoO、NiO等。
②20℃时,生成氢氧化物沉淀的pH
离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
开始沉淀 | 7.0 | 1.9 | 3.4 | 7.2 | 7.1 |
沉淀完全 | 9.0 | 3.2 | 4.7 | 9.2 | 9.1 |
注:金属离子起始浓度为0.1mol/L
(1)上述流程中能加快反应速率的措施有__。
(2)H2O2的作用是将Fe2+氧化为Fe3+。
①加入H2O2发生反应的离子方程式是__。
②滤渣2的主要成分是__(写化学式)。
(3)萃取剂RH可用于对溶液中的Ni2+、Co2+进行分离与富集:Co2+(水相)+2RH(有机相)![]() CoR2(有机相)+2H+(水相)
CoR2(有机相)+2H+(水相)
①萃取剂浓度对溶液中Ni2+、Co2+的萃取率影响如图所示,萃取剂浓度的最佳取值为__mol/L。
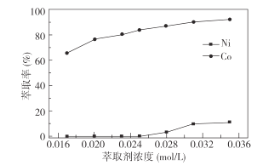
②在__(填“强碱性”或“强酸性”)介质中反萃取,使萃取剂再生而循环利用。
(4)向反萃取后的水溶液中加入稍过量NH4HCO3,得到CoCO3沉淀。将CoCO3与Li2CO3按n(Li):n(Co)=1的比例混合,鼓入空气,高温烧结,得到Li2CoO2。
①得到CoCO3沉淀的离子方程式是__。
②若使用(NH4)2CO3做沉淀剂,产物中会混有Co2(OH)2CO3,这是因为__。
③在空气中烧结反应的化学方程式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA为阿伏加德罗常数的值,下列叙述正确的是
A.1L0.1mol/LNH4Cl溶液中,![]() 的数量为0.1NA
的数量为0.1NA
B.0.1mol的14C中,含有0.6NA个中子
C.标准状况下,2.24LN2和O2的混合气体中原子数为0.2NA
D.16g甲烷和1mol白磷中含有的化学键数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.![]() 与
与![]() 互为同系物
互为同系物
B.分子组成为C4H8O2,其中属于酯的结构有4种
C.乙醇和乙醚互为同分异构体
D.具有相同的分子通式的有机物一定是同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:CO(g)+Cl2(g)![]() COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法中正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ加入CO0.8mol、Cl20.8mol,达到平衡时CO转化率大于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以甲苯为原料合成某种食用香料(有机物G)和某种治疗肺结核药物的有效成分(有机物PASNa)的路线如下:
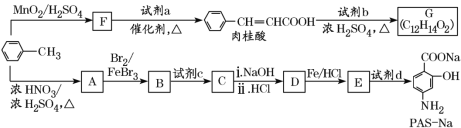
已知:①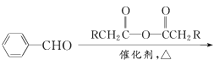
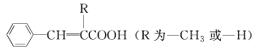
②![]()
③![]()
回答下列问题:
(1)肉桂酸中所含官能团的名称是______________。
(2)①试剂a的结构简式是________________。
②写出由A生成B的化学方程式:____________________。
(3)已知试剂b为相对分子质量为60的醇,且无支链,写出G的结构简式:________________,由肉桂酸制取G的反应类型是________。
(4)①当试剂d过量时,可以选用的试剂d是_____(填字母)。
a.NaOH b.Na2CO3 c.NaHCO3
②参照题中信息,设计以![]() 为起始原料制备
为起始原料制备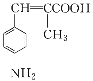 的合成路线。
的合成路线。
____________________。
(5)在肉桂酸分子中碳碳双键催化加氢后得到化合物X(分子式为C9H10O2),X有多种同分异构体,符合下列条件的有________种。写出其中一种处于对位且核磁共振氢谱中比例为6:1:2:2:1的结构简式______________________________。
a.苯环上有两个取代基
b.能发生银镜反应
c.与Na作用有H2产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的顺序为SO2>I->Fe2+>H2O2>Cl-,则下列反应不可能发生的是
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气净化原理为2NO(g)+2CO(g)N2(g)+2CO2(g)ΔH=-746.5kJ·mol-1,如图为在不同初始浓度的CO和不同催化剂Ⅰ、Ⅱ作用下(其他条件相同),体积为2L的密闭容器中n(N2)随反应时间的变化曲线,下列说法正确的是( )
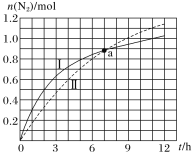
A.a点时,催化剂Ⅰ、Ⅱ作用下CO的转化率相等
B.0~6h内,催化剂Ⅰ的催化效果比催化剂Ⅱ的好
C.0~5h内,催化剂Ⅰ作用下CO的反应速率为0.32mol·L-1·h-1
D.0~12h内,催化剂Ⅱ作用下反应放出的热量比催化剂Ⅰ的多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.除去FeSO4 溶液中的 Fe3+, 可向溶液中加入铜粉, 通过反应 Cu + 2Fe3+ = Cu2+ + 2Fe2+除去 Fe3+
B.常温下,pH为5的 NH4Cl 溶液和pH为5的稀盐酸中,水的电离程度相同
C.由于存在水的电离,0.1 molL-1 的 H2C2O4溶液中, c(H+)/c(C2O![]() )略大于2
)略大于2
D.向氨水中滴加等浓度的盐酸溶液,滴加过程中,c(NH![]() )先增大后减小
)先增大后减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com