
| 3.45g |
| 23g/mol |
| 0.15mol×1 |
| 2 |
| 6g |
| 303.3g |
| 54g×0.15mol |
| 2mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4LH2O含有的分子数为NA |
| B、常温常压下,1.06gNa2CO3含有的Na+离子数为0.01NA |
| C、通常状况下,NA个CO2分子占有的体积为22.4 L |
| D、常温常压下,48gO2和O3的混合气体中含有的氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH- | ||||
B、用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1-+2H2O
| ||||
| C、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ | ||||
| D、钢铁发生电化学腐蚀的负极反应式:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
| B、(x-y)mol | ||
C、
| ||
| D、(x+y)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C |
| 产生白色沉定,溶液仍为蓝色 | 产生蓝色沉定,溶液变为无色 | 产生蓝色沉淀,溶液为无色 |
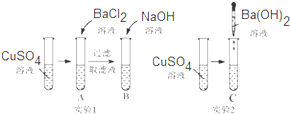
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)现有以下物质①NaOH溶液 ②干冰 ③稀硫酸 ④铜 ⑤醋酸 ⑥BaSO4固体 ⑦蔗糖 ⑧食盐晶体 ⑨酒精 ⑩熔融的KNO3,其中属于电解质的是:
(1)现有以下物质①NaOH溶液 ②干冰 ③稀硫酸 ④铜 ⑤醋酸 ⑥BaSO4固体 ⑦蔗糖 ⑧食盐晶体 ⑨酒精 ⑩熔融的KNO3,其中属于电解质的是:查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
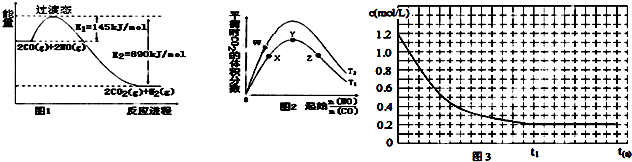
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com