
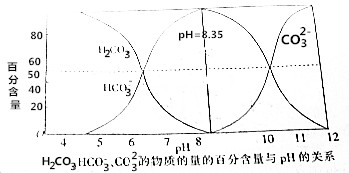
| A�� | ̼����Һ�У�c��H+����c��HCO3-�� | |
| B�� | pH=8.35��������Һ�У�c��H2CO3��+c��H+��=c��CO32-��+c��OH-�� | |
| C�� | ��Na2CO3��NaHCO3�Ļ����Һ�У���c��CO32-��=c��HCO3-������c��Na+��+c��H+��=3c��HCO3-��+c��OH-�� | |
| D�� | pH=12��������Һ�У�c��CO32-����c��HCO3-����c��OH-����c��H+�� |
���� A��̼����Һ�У�̼���������붼����H+��
B��pH=pH=8.35��������Һ�ʼ��ԣ���Һ������Ϊ̼�����ƣ�
C����Na2CO3��NaHCO3�Ļ����Һ�У���c��CO32-��=c��HCO3-�������ݵ���غ��жϣ�
D��pH=12�������У�����ͼ֪��Һ������Ϊ̼���ƣ�̼�������ˮ��̶�ԶԶ����̼��������ӣ���Һ�ʼ��ԣ�
��� �⣺A��̼����Һ�У�̼���������붼����H+������̼����Һ�У�c��H+����c��HCO3-������A��ȷ��
B��pH=pH=8.35��������Һ�ʼ��ԣ���Һ������Ϊ̼�����ƣ����ݵ���غ��C��H+��+C��Na+��=c��OH-��+C��HCO3-��+2C��CO32-�������������غ��C��HCO3-��+C��CO32-��+C��H2CO3��=C��Na+����
���Ե�C��H+��+C��H2CO3��=c��OH-��+C��CO32-������B��ȷ��
C����Na2CO3��NaHCO3�Ļ����Һ�У����ݵ���غ��C��H+��+C��Na+��=c��OH-��+C��HCO3-��+2C��CO32-������c��CO32-��=c��HCO3-�������Ե�c��Na+��+c��H+��=3c��HCO3-��+c��OH-������C��ȷ��
D��pH=12�������У�����ͼ֪��Һ������Ϊ̼���ƣ�̼�������ˮ��̶�ԶԶ����̼��������ӣ���Һ�ʼ��ԣ�CO32-��HCO3-��ˮ�������������ӣ�������Һ�д���c��CO32-����c��OH-����c��HCO3-����c��H+������D����
��ѡD��
���� ���⿼������Ũ�ȴ�С�Ƚϣ�Ϊ��Ƶ���㣬��ȷ��Һ�����ʼ������ʡ��������Һ������ǽⱾ��ؼ���ע�����غ㡢�����غ��������ã���Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25��ʱ����0.02 mol•L-1�İ�ˮ��a mol•L-1������������ϣ�����仯���Բ��ƣ�����Ӧ����Һ�����ԣ����ú�a�Ĵ���ʽ��ʾNH3•H2O�ĵ��볣��ΪKb=$\frac{a��1{0}^{-7}}{0.02-a}$ | |
| B�� | ��������Һ�м�ˮϡ�ͣ���Ӧ��ƽ�����淴Ӧ�����ƶ� | |
| C�� | ����������Һ�м������������ᣬ����Һ�л������ɫ���� | |
| D�� | ��֪��H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ•mol-1����1 L 0.1 mol•L-1��ˮ�����������ᷴӦ�ų�����������5.73 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��Ӧ�����У����ӵ��������Ŀһ�������ı� | |
| B�� | ���ij��ѧ��Ӧ�ġ�H�͡�S��С��0����Ӧһ�����Է����� | |
| C�� | ��ѧ��Ӧ�����У�һ���л�ѧ���Ķ��Ѻ��γ� | |
| D�� | ���е����ȷ�Ӧһ��Ҫ�ڼ��ȵ������²��ܽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������γ�ˮ����ζ����Ҫ�ɷ� | |
| B�� | ��̼�����ܽ�����Ҵ���������������� | |
| C�� | ������������֬��NaOH��Һ��Ӧ���д����� | |
| D�� | �����������£�CH3CO18OC2H5��ˮ�������CH3CO18OH��C2H5OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+��Al3+��NO3-��ALO2- | B�� | H+��Na+��Fe2+��ClO- | ||
| C�� | Na+��Ba2+��Cl-��NO3- | D�� | K+��NH4+��CO32-��OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=5��H2S��Һ�У�c��H+��=c��HS-��=1��10-5mol•L-1 | |
| B�� | ��0.1mol•L-1��ˮ��pHΪ11������ΪNH2•H2O?NH4++OH- | |
| C�� | 0.01mol•L-1NaHCO3��Һ�����ʵĵ��뷽��ʽΪNa++H++CO32- | |
| D�� | CH3COOH��Һ��ˮϡ�ͺ���Һ��$\frac{c��C{H}_{3}COOH��}{c��C{H}_{3}CO{O}^{-}��}$��ֵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com