
【题目】工业上制取CuCl2的生产流程如下:
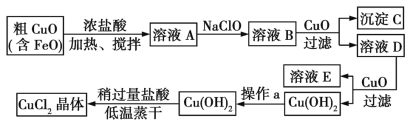
请结合下表数据,回答问题:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
溶度积(25 ℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
(1)在溶液A中加入NaClO的目的是_________________。
(2)在溶液B中加入CuO主要涉及的离子反应方程式为________________。
(3)操作a为___________。
(4)在Cu(OH)2中加入盐酸使Cu(OH)2转化为CuCl2,采用稍过量盐酸和低温蒸干的目的是___。
【答案】氧化Fe2+生成Fe3+有利于沉淀分离 ![]() 洗涤 抑制 Cu2+水解
洗涤 抑制 Cu2+水解
【解析】
在粗氧化铜(含氧化亚铁)中加盐酸,将金属氧化物溶解转变成氯化铜和氯化亚铁;然后加次氯酸钠,将氯化亚铁氧化成氯化铁;再加氧化铜调节溶液的pH值促进氯化铁水解最终转变成氢氧化铁沉淀除去;继续加氧化铜调节pH值后过滤分离得到氢氧化铜,通过操作a洗涤沉淀,再采用稍过量盐酸和低温蒸干得到氯化铜晶体,据此分析解答。
(1)根据表中完全沉淀时的pH范围可知,Fe2+沉淀时Cu2+已基本沉淀完全,所以必须先将Fe2+转变为Fe3+才能完全除去,所以溶液A中加入NaClO的目的是氧化Fe2+ 生成Fe3+ 有利于沉淀分离,反应的离子方程式为:2H++ClO+2 Fe2+=2 Fe3++Cl+H2O,
故答案为:氧化Fe2+生成Fe3+ 有利于沉淀分离;
(2) 在溶液B中加CuO调节溶液的pH使Fe3+完全沉淀,有关的反应为:![]() ,
,
故答案为:![]()
(3) 操作a为洗涤,目的是洗涤氢氧化铜表面的可溶性杂质,
故答案为:洗涤;
(4) 因为溶液中存在以下平衡:Cu2++2H2OCu(OH)2+2H+,加入过量盐酸和低温,能使平衡逆移,防止Cu2+水解,
故答案为:抑制Cu2+水解


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分Co2O3),含少量Fe2O3、MnO2、Al2O3、CaO、MgO、碳及有机物等)制取草酸钴(CoC2O3)的工艺流程如下:
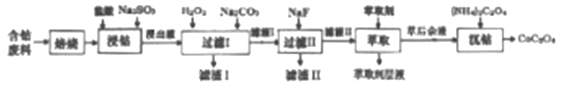
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等。
②部分阳离子一氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀时的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③Kap(MgF2)=7.35×10-11,Kap(CaF2)=1.05×10-10
回答下列问题:
(1)焙烧的目的是_________;浸钴过程中Co3+转化为Co2+,反应的离子方程式为_____________。
(2)加入H2O2的目的是__________,加入Na2CO3溶液,调pH至5.2,滤渣Ⅰ主要成分为__________。
(3)加入过量NaF溶液,可将Ca2+、Mg2+除去,若所得滤液中c(Ca2+)=1.0×10-5mol·L-1,则滤液中c(Mg2+)为_______________。
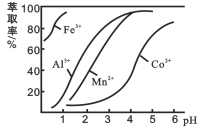
(4)萃取剂对金属离子的萃取率与pH的关系如下图所示。滤液Ⅱ中加入萃取剂的作用是_________;萃取时,溶液的pH需要控制在一定范围内才比较适宜,其pH范围约为__________。
(5)已知含钴废料中含Co2O3质量分数为a%,若取mg该含钴废料按照上述流程,理论上最多能制得CoC2O4的质量为__________g(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有新合成的一种烃,其碳骨架呈三棱柱体(如图所示,碳碳键的键长相等)。
![]()
(1)写出该烃的分子式:________________。
(2)该烃的一氯代物有________种。
(3)该烃的四氯代物有________种。
(4)该烃的同分异构体有多种,其中一种不能使酸性高锰酸钾溶液褪色,但在一定条件下能跟液溴、氢气等发生反应,这种同分异构体的结构简式为________________。请写出该同分异构体与氢气反应的化学方程式并注明反应类型:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入润洗过的锥形瓶中,并加入1或2滴酚酞溶液
⑤滴入一滴标准液后,溶液颜色由无色变为红色立即停止滴定,记录液面读数
请回答:

(1)以上步骤有错误的是(填编号)________。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______中。(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:______(填编号)
A 酸式滴定管未润洗
B 滴定前,滴定管尖嘴无气泡,滴定后有气泡
C 锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D 滴定结束时仰视滴定管,并记录数据
E 滴定过程中有一滴标准液飞溅出锥形瓶
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_______________。
II.利用中和滴定的原理,在工业生产中还可以进行氧化还原滴定测定物质含量。
(5)水泥中钙经处理得草酸钙沉淀经稀H2SO4处理后,用![]() 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反为:
标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反为:![]() .实验中称取0.400g水泥样品,滴定时消耗了0.0500 mol·L-1的
.实验中称取0.400g水泥样品,滴定时消耗了0.0500 mol·L-1的![]() 溶液36.00 mL,则该水泥样品中钙的质量分数为__________
溶液36.00 mL,则该水泥样品中钙的质量分数为__________
(6)滴定终点的现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
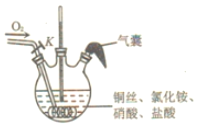
【题目】氯化亚铜![]() 是有机合成中应用广泛的催化剂。它微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化,但在干燥的空气中稳定,见光会分解。实验室制备CuCl的过程如下:
是有机合成中应用广泛的催化剂。它微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化,但在干燥的空气中稳定,见光会分解。实验室制备CuCl的过程如下:
Ⅰ、检査图装置气密性,依次向三颈瓶中加入铜丝、![]() 、
、![]() 、HCl,关闭K;
、HCl,关闭K;
Ⅱ、加热至![]() 时停止加热,铜丝表面产生无色气泡,液面上方气体逐渐变为红棕色,气囊鼓起;
时停止加热,铜丝表面产生无色气泡,液面上方气体逐渐变为红棕色,气囊鼓起;
Ⅲ、打开K,通入![]() ,待气囊变瘪、瓶内红棕色气体消失时关闭K,冷却至室温,制
,待气囊变瘪、瓶内红棕色气体消失时关闭K,冷却至室温,制![]()
Ⅳ、将液体转移至烧杯中用足量蒸馏水稀释,产生白色沉淀,过滤得CuCl粗品和滤液;
Ⅴ、粗品用![]() 乙醇洗涤、烘干得CuCl。
乙醇洗涤、烘干得CuCl。
请回答下列问题:
⑴实验室中CuC1的保存方法是______
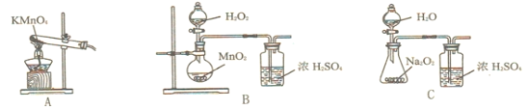
⑵通入![]() 的目的是______,为便于观察和控制产生
的目的是______,为便于观察和控制产生![]() 的速率,制备
的速率,制备![]() 的装置最好选用______
的装置最好选用______![]() 填字母
填字母![]()
⑶①三颈瓶中生成![]() 的总反应的离子方程式为______
的总反应的离子方程式为______
②步骤Ⅳ中产生白色沉淀的化学方程式为______
⑷步骤V中洗涤时试剂选用![]() 乙醇的原因是______
乙醇的原因是______
⑸![]() 纯度测定:称取样品
纯度测定:称取样品![]() 置于预先放入玻璃珠30粒和10mL过量的
置于预先放入玻璃珠30粒和10mL过量的![]() 溶液的锥形瓶中,不断摇动;待样品溶解后,加水50mL和指示剂2滴;立即用
溶液的锥形瓶中,不断摇动;待样品溶解后,加水50mL和指示剂2滴;立即用![]() 硫酸铈标准溶液滴定至终点并记录读数,再重复实验两次,测得数据如表所示。(已知:
硫酸铈标准溶液滴定至终点并记录读数,再重复实验两次,测得数据如表所示。(已知:![]() ,
,![]() )
)
实验序号 | 1 | 2 | 3 |
滴定起始读数 |
|
|
|
滴定终点读数 |
|
|
|
![]() 玻璃珠的作用______
玻璃珠的作用______
![]() 的纯度为______
的纯度为______![]() 保留三位有效数字
保留三位有效数字![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C是一种常见的工业原料,实验室制备C的化学方程式如下,下列说法正确的( )
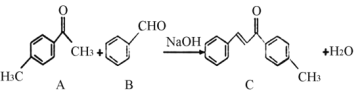
A.l mol的C最多能与7 mol的H2反应
B.分子C中所有碳原子一定共平面
C.可以用酸性KMnO4溶液鉴别A和B
D.A的同分异构体中含有苯环和醛基的结构有14种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)“民以食为天,食以安为先”。近年来屡屡发生的 劣质奶粉、苏丹红、多宝鱼等食品安全事件严重威胁消费者的健康和生命安全。下列有关蛋白质的说法正确的是____________(填序号)。
A.蛋内质是重要的营养物质,也是提供人体所需能最的主要物质
B.蛋白质在淀粉酶的作用下,可水解成葡萄糖等
C.蛋白质水解的最终产物是氨基酸
(2)奶粉中蛋内质含量的国家标准是:每100 g婴幼儿奶粉中含蛋白质1225 g。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨, 由氨的量计算出氮的量,再由氮的量求出蛋白质的含量(蛋白质含氮量按16%计算)。某市质检局取100 g市场中的某个品牌的奶粉样品进行检验。该样品进行反应后生成的![]() 和 7.5 g 19. 6%的稀硫酸恰好完全反应,通过计算可判断出这种奶粉__________(填“属于”或“不属于”)合格奶粉。
和 7.5 g 19. 6%的稀硫酸恰好完全反应,通过计算可判断出这种奶粉__________(填“属于”或“不属于”)合格奶粉。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组测定不同温度下、不同初始浓度的某溶液中R的水解速率,c(R)随时间的变化曲线如图。下列说法不正确的是
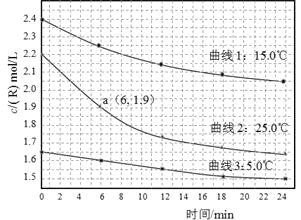
A.在0-6min之间,25℃时R的水解速率为0.05 mol·L—1·min—1
B.在0-24min之间,曲线3对应水解速率最小
C.由曲线1可以得出结论:其它条件不变,水解速率随浓度增大而增大
D.由曲线2、3可以得出结论:其它条件不变,水解速率随温度升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物在有机合成、能源开发等工农业方面具有十分广泛的应用。
Ⅰ.在25℃、101kPa时,1.00g C6H6(l)燃烧生成CO2和H2O(l)时,放出41.8kJ的热量,表示C6H6(l)燃烧热的热化学方程式为___________________。
Ⅱ.乙二醇(HOCH2CH2OH)气相氧化法
已知:2H2(g)+O2(g) 2H2O(g)ΔH=-484kJ/mol
OHC-CHO(g)+2H2(g) HOCH2CH2OH(g) ΔH=-78kJ/mol
则乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g) OHC-CHO(g)+2H2O(g)的ΔH=________;相同温度下,该反应的化学平衡常数K=____________(用含K1、K2的代数式表示)。
Ⅲ. 甲醇的合成。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应如下:CO(g)+2H2(g)CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
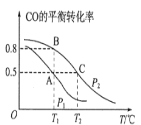
①A、B两点对应的压强大小关系是PA________PB(填“>、<、=”)。
②A、B、C三点的平衡常数KA,KB,KC的大小关系是__________。
③下列叙述能说明上述反应能达到化学平衡状态的是______________(填代号)。
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,经5min达到化学平衡,则用氢气表示该反应的化学速率v(H2)=______,再加入1.0molCO后重新到达平衡,则CO的转化率______(填“增大,不变,减小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com