
ΓΨΧβΡΩΓΩ¬»Μ·―«Ά≠![]() «”–ΜζΚœ≥…÷–”Π”ΟΙψΖΚΒΡ¥ΏΜ·ΦΝΓΘΥϋΈΔ»ή”ΎΥ°Θ§≤Μ»ή”Ύ““¥ΦΘ§¬Ε÷Ο”Ύ≥± ΣΒΡΩ’Τχ÷–“Ή±Μ―θΜ·Θ§ΒΪ‘ΎΗ…‘οΒΡΩ’Τχ÷–Έ»Ε®Θ§ΦϊΙβΜαΖ÷ΫβΓΘ Β―ι “÷Τ±ΗCuClΒΡΙΐ≥Χ»γœ¬ΘΚ
«”–ΜζΚœ≥…÷–”Π”ΟΙψΖΚΒΡ¥ΏΜ·ΦΝΓΘΥϋΈΔ»ή”ΎΥ°Θ§≤Μ»ή”Ύ““¥ΦΘ§¬Ε÷Ο”Ύ≥± ΣΒΡΩ’Τχ÷–“Ή±Μ―θΜ·Θ§ΒΪ‘ΎΗ…‘οΒΡΩ’Τχ÷–Έ»Ε®Θ§ΦϊΙβΜαΖ÷ΫβΓΘ Β―ι “÷Τ±ΗCuClΒΡΙΐ≥Χ»γœ¬ΘΚ
ΔώΓΔΦλ•ΥΆΦΉΑ÷ΟΤχΟή–‘Θ§“ά¥Έœρ»ΐΨ±ΤΩ÷–Φ”»κΆ≠ΥΩΓΔ![]() ΓΔ
ΓΔ![]() ΓΔHClΘ§ΙΊ±’KΘΜ
ΓΔHClΘ§ΙΊ±’KΘΜ
ΔρΓΔΦ”»»÷Ν![]() ±ΆΘ÷ΙΦ”»»Θ§Ά≠ΥΩ±μΟφ≤ζ…ζΈό…ΪΤχ≈ίΘ§“ΚΟφ…œΖΫΤχΧε÷πΫΞ±δΈΣΚλΉΊ…ΪΘ§ΤχΡ“ΙΡΤπΘΜ
±ΆΘ÷ΙΦ”»»Θ§Ά≠ΥΩ±μΟφ≤ζ…ζΈό…ΪΤχ≈ίΘ§“ΚΟφ…œΖΫΤχΧε÷πΫΞ±δΈΣΚλΉΊ…ΪΘ§ΤχΡ“ΙΡΤπΘΜ
ΔσΓΔ¥ρΩΣKΘ§Ά®»κ![]() Θ§¥ΐΤχΡ“±δ±ώΓΔΤΩΡΎΚλΉΊ…ΪΤχΧεœϊ ß ±ΙΊ±’KΘ§ά以÷Ν “Έ¬Θ§÷Τ
Θ§¥ΐΤχΡ“±δ±ώΓΔΤΩΡΎΚλΉΊ…ΪΤχΧεœϊ ß ±ΙΊ±’KΘ§ά以÷Ν “Έ¬Θ§÷Τ![]()
ΔτΓΔΫΪ“ΚΧεΉΣ“Τ÷Ν…’±≠÷–”ΟΉψΝΩ’τΝσΥ°œΓ ΆΘ§≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§Ιΐ¬ΥΒΟCuCl¥÷ΤΖΚΆ¬Υ“ΚΘΜ
ΔθΓΔ¥÷ΤΖ”Ο![]() ““¥Φœ¥Β”ΓΔΚφΗ…ΒΟCuClΓΘ
““¥Φœ¥Β”ΓΔΚφΗ…ΒΟCuClΓΘ
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Δ≈ Β―ι “÷–CuC1ΒΡ±Θ¥φΖΫΖ® «______
ΔΤΆ®»κ![]() ΒΡΡΩΒΡ «______Θ§ΈΣ±ψ”ΎΙέ≤λΚΆΩΊ÷Τ≤ζ…ζ
ΒΡΡΩΒΡ «______Θ§ΈΣ±ψ”ΎΙέ≤λΚΆΩΊ÷Τ≤ζ…ζ![]() ΒΡΥΌ¬ Θ§÷Τ±Η
ΒΡΥΌ¬ Θ§÷Τ±Η![]() ΒΡΉΑ÷ΟΉνΚΟ―Γ”Ο______
ΒΡΉΑ÷ΟΉνΚΟ―Γ”Ο______![]() ΧνΉ÷ΡΗ
ΧνΉ÷ΡΗ![]()
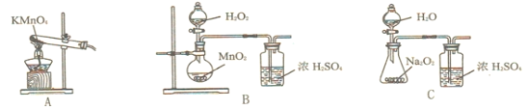
Δ«ΔΌ»ΐΨ±ΤΩ÷–…ζ≥…![]() ΒΡΉήΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ______
ΒΡΉήΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ______
ΔΎ≤Ϋ÷ηΔτ÷–≤ζ…ζΑΉ…Ϊ≥ΝΒμΒΡΜ·―ßΖΫ≥Χ ΫΈΣ______
Δ»≤Ϋ÷ηV÷–œ¥Β” ± ‘ΦΝ―Γ”Ο![]() ““¥ΦΒΡ‘≠“ρ «______
““¥ΦΒΡ‘≠“ρ «______
Δ…![]() ¥ΩΕ»≤βΕ®ΘΚ≥Τ»Γ―υΤΖ
¥ΩΕ»≤βΕ®ΘΚ≥Τ»Γ―υΤΖ![]() ÷Ο”Ύ‘Λœ»Ζ≈»κ≤ΘΝß÷ι30ΝΘΚΆ10mLΙΐΝΩΒΡ
÷Ο”Ύ‘Λœ»Ζ≈»κ≤ΘΝß÷ι30ΝΘΚΆ10mLΙΐΝΩΒΡ![]() »ή“ΚΒΡΉΕ–ΈΤΩ÷–Θ§≤ΜΕœ“ΓΕ·ΘΜ¥ΐ―υΤΖ»ήΫβΚσΘ§Φ”Υ°50mLΚΆ÷Η ΨΦΝ2ΒΈΘΜΝΔΦ¥”Ο
»ή“ΚΒΡΉΕ–ΈΤΩ÷–Θ§≤ΜΕœ“ΓΕ·ΘΜ¥ΐ―υΤΖ»ήΫβΚσΘ§Φ”Υ°50mLΚΆ÷Η ΨΦΝ2ΒΈΘΜΝΔΦ¥”Ο![]() ΝρΥανφ±ξΉΦ»ή“ΚΒΈΕ®÷Ν÷’Βψ≤ΔΦ«¬ΦΕΝ ΐΘ§‘Ό÷ΊΗ¥ Β―ιΝΫ¥ΈΘ§≤βΒΟ ΐΨί»γ±μΥυ ΨΓΘ(“―÷ΣΘΚ
ΝρΥανφ±ξΉΦ»ή“ΚΒΈΕ®÷Ν÷’Βψ≤ΔΦ«¬ΦΕΝ ΐΘ§‘Ό÷ΊΗ¥ Β―ιΝΫ¥ΈΘ§≤βΒΟ ΐΨί»γ±μΥυ ΨΓΘ(“―÷ΣΘΚ![]() Θ§
Θ§![]() )
)
Β―ι–ρΚ≈ | 1 | 2 | 3 |
ΒΈΕ®Τπ ΦΕΝ ΐ |
|
|
|
ΒΈΕ®÷’ΒψΕΝ ΐ |
|
|
|
![]() ≤ΘΝß÷ιΒΡΉς”Ο______
≤ΘΝß÷ιΒΡΉς”Ο______
![]() ΒΡ¥ΩΕ»ΈΣ______
ΒΡ¥ΩΕ»ΈΣ______![]() ±ΘΝτ»ΐΈΜ”––ß ΐΉ÷
±ΘΝτ»ΐΈΜ”––ß ΐΉ÷![]() ΓΘ
ΓΘ
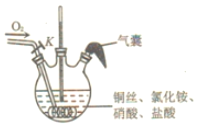
ΓΨ¥πΑΗΓΩΗ…‘οΓΔΟή±’ΒΡ»ίΤς÷–Θ§±ήΙβ±Θ¥φ ΫΪ»ΐΨ±ΤΩ÷–ΒΡ![]() ΉΣΜ·ΈΣ
ΉΣΜ·ΈΣ![]() B
B ![]()
![]() ≥ΐ»ΞCuCl±μΟφΗΫΉ≈ΒΡ
≥ΐ»ΞCuCl±μΟφΗΫΉ≈ΒΡ![]() Θ§”÷Ρή―ΗΥΌΜ”ΖΔ¥χΉΏCuCl±μΟφΒΡΥ°ΖίΘ§Ζά÷ΙΤδ±Μ―θΜ· Φ”ΥΌ―υΤΖ»ήΫβ
Θ§”÷Ρή―ΗΥΌΜ”ΖΔ¥χΉΏCuCl±μΟφΒΡΥ°ΖίΘ§Ζά÷ΙΤδ±Μ―θΜ· Φ”ΥΌ―υΤΖ»ήΫβ ![]()
ΓΨΫβΈωΓΩ
Δ≈”…–≈œΔΩ…÷ΣΘ§ΒΟΒΫ Β―ι “÷–CuC1ΒΡ±Θ¥φΖΫΖ®ΓΘ
ΔΤ¥ρΩΣKΘ§Ά®»κ―θΤχΘ§¥ΐΤχΡ“±δ±ώΓΔΤΩΡΎΚλΉΊ…ΪΤχΧεœϊ ßΘ§ΥΒΟςΕΰ―θΜ·ΒΣ”κ―θΤχΓΔΥ°ΉΣΜ·≥…![]() ΘΜΗυΨίΆΦ ΨΩ…÷ΣΘ§BΉΑ÷ΟΩ…“‘ΗυΨίΉΕ–ΈΤΩΡΎΤχ≈ίΒΡΩλ¬ΐ≈–Εœ≤ζ…ζ
ΘΜΗυΨίΆΦ ΨΩ…÷ΣΘ§BΉΑ÷ΟΩ…“‘ΗυΨίΉΕ–ΈΤΩΡΎΤχ≈ίΒΡΩλ¬ΐ≈–Εœ≤ζ…ζ![]() ΒΡΥΌ¬ Ϋχ––ΩΊ÷ΤΘ§ΕχAΓΔCΉΑ÷ΟΈόΖ®≈–ΕœΆ®»κ―θΤχΒΡΥΌ¬ ΓΘ
ΒΡΥΌ¬ Ϋχ––ΩΊ÷ΤΘ§ΕχAΓΔCΉΑ÷ΟΈόΖ®≈–ΕœΆ®»κ―θΤχΒΡΥΌ¬ ΓΘ
Δ«ΔΌΆ≠ΥΩΓΔ¬»Μ·Α±ΓΔœθΥαΓΔ―ΈΥαΖ¥”Π…ζ≥…![]() ΚΆΈό…ΪΤχ≈ίNOΘ§–¥≥ωΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΓΘ
ΚΆΈό…ΪΤχ≈ίNOΘ§–¥≥ωΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΓΘ
ΔΎ≤Ϋ÷ηΔτ÷–≤ζ…ζΑΉ…Ϊ≥ΝΒμΒΟΒΫΜ·―ßΖΫ≥Χ ΫΓΘ
Δ»“ρCuClΈΔ»ή”ΎΥ°Θ§≤…”Ο![]() ““¥Φœ¥Β”Θ§Φ»≥ΐ»ΞCuCl±μΟφΗΫΉ≈ΒΡ
““¥Φœ¥Β”Θ§Φ»≥ΐ»ΞCuCl±μΟφΗΫΉ≈ΒΡ![]() Θ§”÷Ρή―ΗΥΌΜ”ΖΔ¥χΉΏCuCl±μΟφΒΡΥ°ΖίΘ§Ζά÷ΙΤδ±Μ―θΜ·ΓΘ
Θ§”÷Ρή―ΗΥΌΜ”ΖΔ¥χΉΏCuCl±μΟφΒΡΥ°ΖίΘ§Ζά÷ΙΤδ±Μ―θΜ·ΓΘ
Δ»ΔΌ≤ΘΝß÷ιΒΡΉς”ΟΈΣΦ”ΥΌ―υΤΖ»ήΫβΓΘ
ΔΎΦΤΥψ≥ωœϊΚΡΒΟΤΫΨυ÷ΒΘ§‘ΌΗυΨίΙΊœΒ ΫΫ®ΝΔΒ» ΫΫχ––ΦΤΥψΓΘ
Δ≈”…–≈œΔΩ…÷ΣΘ§ Β―ι “÷–CuC1ΒΡ±Θ¥φΖΫΖ® «Η…‘οΓΔΟή±’ΒΡ»ίΤς÷–Θ§±ήΙβ±Θ¥φΘΜΙ ¥πΑΗΈΣΘΚΗ…‘οΓΔΟή±’ΒΡ»ίΤς÷–Θ§±ήΙβ±Θ¥φΓΘ
ΔΤ¥ρΩΣKΘ§Ά®»κ―θΤχΘ§¥ΐΤχΡ“±δ±ώΓΔΤΩΡΎΚλΉΊ…ΪΤχΧεœϊ ßΘ§ΥΒΟςΕΰ―θΜ·ΒΣ”κ―θΤχΓΔΥ°ΉΣΜ·≥…![]() Θ§Ι Ά®»κ―θΤχΒΡΡΩΒΡ «ΈΣΝΥΫΪ»ΐΨ±ΤΩ÷–ΒΡ
Θ§Ι Ά®»κ―θΤχΒΡΡΩΒΡ «ΈΣΝΥΫΪ»ΐΨ±ΤΩ÷–ΒΡ![]() Ζ¥”Π…ζ≥…
Ζ¥”Π…ζ≥…![]() ΘΜΗυΨίΆΦ ΨΩ…÷ΣΘ§BΉΑ÷ΟΩ…“‘ΗυΨίΉΕ–ΈΤΩΡΎΤχ≈ίΒΡΩλ¬ΐ≈–Εœ≤ζ…ζ
ΘΜΗυΨίΆΦ ΨΩ…÷ΣΘ§BΉΑ÷ΟΩ…“‘ΗυΨίΉΕ–ΈΤΩΡΎΤχ≈ίΒΡΩλ¬ΐ≈–Εœ≤ζ…ζ![]() ΒΡΥΌ¬ Ϋχ––ΩΊ÷ΤΘ§ΕχAΓΔCΉΑ÷ΟΈόΖ®≈–ΕœΆ®»κ―θΤχΒΡΥΌ¬ Θ§Ι ―Γ‘ώBΉΑ÷ΟΘΜΙ ¥πΑΗΈΣΘΚΫΪ»ΐΨ±ΤΩ÷–ΒΡ
ΒΡΥΌ¬ Ϋχ––ΩΊ÷ΤΘ§ΕχAΓΔCΉΑ÷ΟΈόΖ®≈–ΕœΆ®»κ―θΤχΒΡΥΌ¬ Θ§Ι ―Γ‘ώBΉΑ÷ΟΘΜΙ ¥πΑΗΈΣΘΚΫΪ»ΐΨ±ΤΩ÷–ΒΡ![]() ΉΣΜ·ΈΣ
ΉΣΜ·ΈΣ![]() ΘΜ BΓΘ
ΘΜ BΓΘ
Δ«ΔΌΆ≠ΥΩΓΔ¬»Μ·Α±ΓΔœθΥαΓΔ―ΈΥαΖ¥”Π…ζ≥…![]() ΚΆΈό…ΪΤχ≈ίNOΘ§ΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ
ΚΆΈό…ΪΤχ≈ίNOΘ§ΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ![]() ΘΜΙ ¥πΑΗΈΣΘΚ
ΘΜΙ ¥πΑΗΈΣΘΚ![]() ΓΘ
ΓΘ
ΔΎ≤Ϋ÷ηΔτ÷–≤ζ…ζΑΉ…Ϊ≥ΝΒμΒΡΜ·―ßΖΫ≥Χ ΫΈΣ![]() ΘΜΙ ¥πΑΗΈΣΘΚ
ΘΜΙ ¥πΑΗΈΣΘΚ![]() ΓΘ
ΓΘ
Δ»“ρCuClΈΔ»ή”ΎΥ°Θ§≤…”Ο![]() ““¥Φœ¥Β”Θ§Φ»≥ΐ»ΞCuCl±μΟφΗΫΉ≈ΒΡ
““¥Φœ¥Β”Θ§Φ»≥ΐ»ΞCuCl±μΟφΗΫΉ≈ΒΡ![]() Θ§”÷Ρή―ΗΥΌΜ”ΖΔ¥χΉΏCuCl±μΟφΒΡΥ°ΖίΘ§Ζά÷ΙΤδ±Μ―θΜ·ΘΜΙ ¥πΑΗΈΣΘΚΦ»≥ΐ»ΞCuCl±μΟφΗΫΉ≈ΒΡ
Θ§”÷Ρή―ΗΥΌΜ”ΖΔ¥χΉΏCuCl±μΟφΒΡΥ°ΖίΘ§Ζά÷ΙΤδ±Μ―θΜ·ΘΜΙ ¥πΑΗΈΣΘΚΦ»≥ΐ»ΞCuCl±μΟφΗΫΉ≈ΒΡ![]() Θ§”÷Ρή―ΗΥΌΜ”ΖΔ¥χΉΏCuCl±μΟφΒΡΥ°ΖίΘ§Ζά÷ΙΤδ±Μ―θΜ·ΓΘ
Θ§”÷Ρή―ΗΥΌΜ”ΖΔ¥χΉΏCuCl±μΟφΒΡΥ°ΖίΘ§Ζά÷ΙΤδ±Μ―θΜ·ΓΘ
Δ»ΔΌ≤ΘΝß÷ιΒΡΉς”ΟΈΣΦ”ΥΌ―υΤΖ»ήΫβΘ§Ι ¥πΑΗΈΣΘΚΦ”ΥΌ―υΤΖ»ήΫβΓΘ
ΔΎ”…![]() ΓΔ
ΓΔ![]() Ω…÷ΣΘ§¥φ‘Ύ
Ω…÷ΣΘ§¥φ‘Ύ![]() Θ§ Β―ι1ΓΔ2ΓΔ3œϊΚΡ±ξΉΦ“ΚΧεΜΐΖ÷±πΈΣ
Θ§ Β―ι1ΓΔ2ΓΔ3œϊΚΡ±ξΉΦ“ΚΧεΜΐΖ÷±πΈΣ![]() ΓΔ
ΓΔ![]() ΓΔ
ΓΔ![]() Θ§ΒΎ“ΜΉι ΐΨίΈσ≤νΫœ¥σΘ§”Π…α»ΞΘ§‘ρœϊΚΡΒΡ±ξΉΦ“ΚΒΡΤΫΨυΧεΜΐΈΣ
Θ§ΒΎ“ΜΉι ΐΨίΈσ≤νΫœ¥σΘ§”Π…α»ΞΘ§‘ρœϊΚΡΒΡ±ξΉΦ“ΚΒΡΤΫΨυΧεΜΐΈΣ![]() Θ§ΗυΨί
Θ§ΗυΨί![]() ΓΔ
ΓΔ![]() Ω…ΒΟΙΊœΒ Ϋ
Ω…ΒΟΙΊœΒ Ϋ![]() Θ§‘ρ
Θ§‘ρ![]() Θ§Υυ“‘CuClΒΡ¥ΩΕ»ΈΣ
Θ§Υυ“‘CuClΒΡ¥ΩΕ»ΈΣ![]() ΘΜΙ ¥πΑΗΈΣΘΚ
ΘΜΙ ¥πΑΗΈΣΘΚ![]() ΓΘ
ΓΘ


 –¬ΩΈ±ξΫΉΧί‘ΡΕΝ―ΒΝΖœΒΝ–¥πΑΗ
–¬ΩΈ±ξΫΉΧί‘ΡΕΝ―ΒΝΖœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΖ¥”ΠA+BΓζC ΓςH ΘΦ0Θ§Ζ÷ΝΫ≤ΫΫχ–– ΔΌ A+BΓζX ΓςHΘΨ0 ΔΎ XΓζC ΓςHΘΦ0 ΓΘœ¬Ν– Ψ“βΆΦ÷–Θ§Ρή’ΐ»Ζ±μ ΨΉήΖ¥”ΠΙΐ≥Χ÷–ΡήΝΩ±δΜ·ΒΡ «
A.  B.
B. 
C.  D.
D. 
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥ΘΈ¬Ε»œ¬Θ§ΫΪCl2ΜΚ¬ΐΆ®»κΥ°÷–÷Ν±ΞΚΆΘ§»ΜΚσ‘ΌΒΈΦ”0.1mol/LΒΡNaOH»ή“ΚΘ§’ϊΗωΙΐ≥Χ÷–»ή“ΚΒΡpH±δΜ·«ζœΏ»γΆΦΥυ ΨΓΘ“―÷ΣdΒψΥυ ΨΒΡ»ή“Κ÷–Θ§ΡΤ‘ΣΥΊ”ꬻ‘ΣΥΊΒΡΈο÷ ΒΡΝΩœύΒ»Θ§œ¬Ν–―Γœν’ΐ»ΖΒΡ «( )
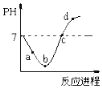
A.aΒψ ±Θ§“―Ψ≠ΒΈ»κNaOH»ή“Κ
B.bΒψΥυ ΨΒΡ»ή“Κ÷–Θ§÷Μ¥φ‘ΎΝΫ÷÷Ζ÷Ή”
C.aΓΔbΓΔcΓΔdΥΡΗωΒψΒ±÷–Θ§dΒψΥ°ΒΡΒγάκ≥ΧΕ»Ήν¥σ
D.cΒψΥυ ΨΒΡ»ή“Κ÷–Θ§c(Na+)=c(Cl-)+c(HClO)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ Β―ι “¥”Κ§ΒβΖœ“Κ![]() ≥ΐ
≥ΐ![]() ΆβΘ§Κ§”–
ΆβΘ§Κ§”–![]() ΓΔ
ΓΔ![]() ΓΔ
ΓΔ![]() Β»
Β»![]() ÷–ΜΊ ’ΒβΘ§Τδ Β―ιΙΐ≥Χ»γœ¬ΘΚ
÷–ΜΊ ’ΒβΘ§Τδ Β―ιΙΐ≥Χ»γœ¬ΘΚ
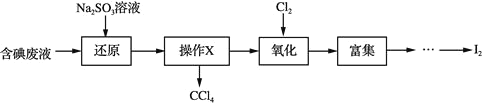
œ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «
A.ΓΑΜΙ‘≠Γ±≤Ϋ÷ηΖΔ…ζΒΡΖ¥”ΠΈΣΘΚ![]()
![]()
B.ΓΑ≤ΌΉςXΓ±ΈΣΨ≤÷ΟΓΔΖ÷“ΚΘ§ΥυΒΟ![]() Ω…”ΟΉςΓΑΗΜΦ·Γ±ΒΡίΆ»ΓΦΝ
Ω…”ΟΉςΓΑΗΜΦ·Γ±ΒΡίΆ»ΓΦΝ
C.ΓΑ―θΜ·Γ±Ιΐ≥Χ÷–Θ§ΈΣ Ι![]() Άξ»Ϊ±Μ―θΜ·Θ§–η≥Λ ±ΦδΆ®»κ
Άξ»Ϊ±Μ―θΜ·Θ§–η≥Λ ±ΦδΆ®»κ![]()
D.ΓΑΗΜΦ·Γ±Φ¥![]() ΗΜΦ·”Ύ”–Μζ»ήΦΝΘ§Ά§ ±≥ΐ»ΞΡ≥–©‘”÷ άκΉ”
ΗΜΦ·”Ύ”–Μζ»ήΦΝΘ§Ά§ ±≥ΐ»ΞΡ≥–©‘”÷ άκΉ”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΐΝρΥαΡΤ![]() ≥Θ”ΟΉςΤ·ΑΉΦΝΓΔ―θΜ·ΦΝΒ»ΓΘΡ≥―–ΨΩ–ΓΉιάϊ”Ο»γΆΦΉΑ÷Ο÷Τ±Η
≥Θ”ΟΉςΤ·ΑΉΦΝΓΔ―θΜ·ΦΝΒ»ΓΘΡ≥―–ΨΩ–ΓΉιάϊ”Ο»γΆΦΉΑ÷Ο÷Τ±Η![]() ≤ΔΧΫΨΩΤδ–‘÷
≤ΔΧΫΨΩΤδ–‘÷ ![]() Φ”»»ΦΑΦ–≥÷“«Τς¬‘»Ξ
Φ”»»ΦΑΦ–≥÷“«Τς¬‘»Ξ![]() ΓΘ
ΓΘ
“―÷ΣΘΚ![]()
![]()
![]()
![]()
![]()
![]()
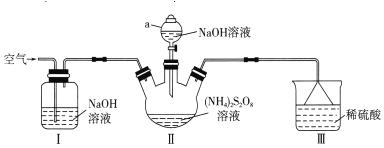
Δ≈“«ΤςaΒΡΟϊ≥Τ «______ΓΘΉΑ÷ΟΔώ÷–NaOH»ή“ΚΒΡΉς”Ο «______ΓΘ
ΔΤΉΑ÷ΟΔρΖΔ…ζΖ¥”ΠΒΡΆ§ ±Θ§–η“Σ≥÷–χΆ®»κΩ’ΤχΒΡΡΩΒΡ «______ΓΘ
Δ«ΉΑ÷ΟΔσΒΡΉς”Ο «______ΓΘ
Δ»![]() »ή“Κ”κΆ≠Ζ¥”Π÷Μ…ζ≥…ΝΫ÷÷―ΈΘ§«“Ζ¥”Πœ»¬ΐΚσΩλΓΘ
»ή“Κ”κΆ≠Ζ¥”Π÷Μ…ζ≥…ΝΫ÷÷―ΈΘ§«“Ζ¥”Πœ»¬ΐΚσΩλΓΘ
ΔΌΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ______ΓΘ
ΔΎΡ≥Ά§―ßΆΤ≤βΖ¥”Πœ»¬ΐΚσΩλΒΡ‘≠“ρΩ…Ρή «…ζ≥…ΒΡ![]() Ε‘Ζ¥”ΠΤπ¥ΏΜ·Ής”ΟΓΘ…ηΦΤ Β―ιΖΫΑΗ―ι÷ΛΗΟΆΤ≤β «Ζώ’ΐ»Ζ______ΓΘ(Ι©―Γ ‘ΦΝΘΚCuΓΔ
Ε‘Ζ¥”ΠΤπ¥ΏΜ·Ής”ΟΓΘ…ηΦΤ Β―ιΖΫΑΗ―ι÷ΛΗΟΆΤ≤β «Ζώ’ΐ»Ζ______ΓΘ(Ι©―Γ ‘ΦΝΘΚCuΓΔ![]() »ή“ΚΓΔ
»ή“ΚΓΔ![]() »ή“ΚΓΔ
»ή“ΚΓΔ![]() »ή“ΚΓΔ’τΝσΥ°)
»ή“ΚΓΔ’τΝσΥ°)
Δ…≤βΕ®≤ζΤΖ¥ΩΕ»ΘΚ≥Τ»Γ![]() ―υΤΖΘ§”Ο’τΝσΥ°»ήΫβΘ§Φ”»κΙΐΝΩKIΘ§≥δΖ÷Ζ¥”ΠΚσΘ§‘ΌΒΈΦ”ΦΗΒΈ÷Η ΨΦΝΘ§”Ο
―υΤΖΘ§”Ο’τΝσΥ°»ήΫβΘ§Φ”»κΙΐΝΩKIΘ§≥δΖ÷Ζ¥”ΠΚσΘ§‘ΌΒΈΦ”ΦΗΒΈ÷Η ΨΦΝΘ§”Ο![]() ±ξΉΦ»ή“ΚΒΈΕ®Θ§¥οΒΫΒΈΕ®÷’Βψ ±Θ§œϊΚΡ±ξΉΦ»ή“ΚΒΡΧεΜΐΈΣ
±ξΉΦ»ή“ΚΒΈΕ®Θ§¥οΒΫΒΈΕ®÷’Βψ ±Θ§œϊΚΡ±ξΉΦ»ή“ΚΒΡΧεΜΐΈΣ![]() ΓΘ(“―÷ΣΘΚ
ΓΘ(“―÷ΣΘΚ![]() )
)
ΔΌ―Γ”ΟΒΡ÷Η ΨΦΝ «______ΘΜ¥οΒΫΒΈΕ®÷’ΒψΒΡœ÷œσ «______ΓΘ
ΔΎ―υΤΖΒΡ¥ΩΕ»ΈΣ______%ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΛ“Β…œ÷Τ»ΓCuCl2ΒΡ…ζ≤ζΝς≥Χ»γœ¬ΘΚ
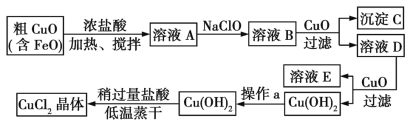
«κΫαΚœœ¬±μ ΐΨίΘ§ΜΊ¥πΈ ΧβΘΚ
Έο÷ | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
»ήΕ»Μΐ(25 Γφ) | 8.0ΓΝ10-16 | 2.2ΓΝ10-20 | 4.0ΓΝ10-38 |
Άξ»Ϊ≥ΝΒμ ±ΒΡpHΖΕΈß | Γί9.6 | Γί6.4 | 3~4 |
(1)‘Ύ»ή“ΚA÷–Φ”»κNaClOΒΡΡΩΒΡ «_________________ΓΘ
(2)‘Ύ»ή“ΚB÷–Φ”»κCuO÷ς“Σ…φΦΑΒΡάκΉ”Ζ¥”ΠΖΫ≥Χ ΫΈΣ________________ΓΘ
(3)≤ΌΉςaΈΣ___________ΓΘ
(4)‘ΎCu(OH)2÷–Φ”»κ―ΈΥα ΙCu(OH)2ΉΣΜ·ΈΣCuCl2Θ§≤…”Ο…‘ΙΐΝΩ―ΈΥαΚΆΒΆΈ¬’τΗ…ΒΡΡΩΒΡ «___ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩάύΆΤΥΦΈ§ «Μ·―ßΫβΧβ÷–≥Θ”ΟΒΡ“Μ÷÷ΥΦΈ§ΖΫΖ®Θ§œ¬Ν–”–ΙΊΖ¥”ΠΖΫ≥Χ ΫΘ®ΜράκΉ”ΖΫ≥Χ ΫΘ©ΒΡάύΆΤ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
“―÷Σ | άύΆΤ | |
A | ΫΪFeΦ”»κCuSO4»ή“Κ÷–ΘΚ Fe + Cu2+ = Cu + Fe2+ | ΫΪNaΦ”»κΒΫCuSO4»ή“Κ÷–ΘΚ 2Na + Cu2+ = Cu + 2Na+ |
B | œΓΝρΥα”κBa(OH)2»ή“ΚΖ¥”Π÷Ν»ή“Κ≥ ÷––‘ΘΚ 2H++SO42©¹+Ba2++2OH©¹=BaSO4Γΐ+2H2O | NaHSO4»ή“Κ”κBa(OH)2»ή“ΚΖ¥”Π≥ ÷––‘ΘΚ 2H++SO42©¹+Ba++2OH©¹=BaSO4Γΐ+2H2O |
C | ΧζΚΆ¬»ΤχΖ¥”Π2Fe+3Cl2 | ΧζΚΆΒΞ÷ Ζ¥”Π2Fe+3I2 |
D | œρCaΘ®ClOΘ©2»ή“Κ÷–Ά®»κ…ΌΝΩCO2ΘΚ Ca2++2ClO©¹+CO2+H2O=CaCO3Γΐ+2HClO | œρCaΘ®ClOΘ©2»ή“Κ÷–Ά®»κ…ΌΝΩSO2ΘΚ Ca2++2ClO©¹+SO2+H2O=CaSO3Γΐ+2HClO |
A.AB.BC.CD.D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
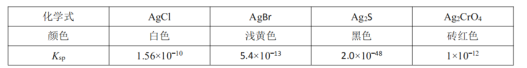
ΓΨΧβΡΩΓΩ―«œθθΘ¬»![]() «”–ΜζΈοΚœ≥…÷–ΒΡ÷Ί“Σ ‘ΦΝΘ§ΤδΖ–ΒψΈΣ
«”–ΜζΈοΚœ≥…÷–ΒΡ÷Ί“Σ ‘ΦΝΘ§ΤδΖ–ΒψΈΣ![]() Θ§“ΉΥ°ΫβΓΘ“―÷ΣΘΚ
Θ§“ΉΥ°ΫβΓΘ“―÷ΣΘΚ![]() ΈΔ»ή”ΎΥ°Θ§Ρή»ή”ΎœθΥαΘ§
ΈΔ»ή”ΎΥ°Θ§Ρή»ή”ΎœθΥαΘ§![]() Θ§Ρ≥―ßœΑ–ΓΉι‘Ύ Β―ι “”Ο
Θ§Ρ≥―ßœΑ–ΓΉι‘Ύ Β―ι “”Ο![]() ΚΆNO÷Τ±ΗClNO≤Δ≤βΕ®Τδ¥ΩΕ»Θ§œύΙΊ Β―ιΉΑ÷Ο»γΆΦΥυ ΨΓΘ
ΚΆNO÷Τ±ΗClNO≤Δ≤βΕ®Τδ¥ΩΕ»Θ§œύΙΊ Β―ιΉΑ÷Ο»γΆΦΥυ ΨΓΘ
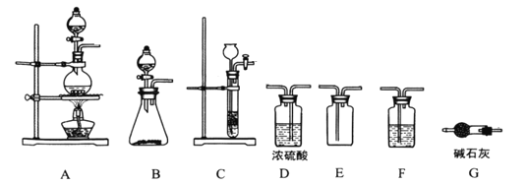
Δ≈÷Τ±Η![]() ΒΡΖΔ…ζΉΑ÷ΟΩ…“‘―Γ”Ο_______(ΧνΉ÷ΡΗ¥ζΚ≈)ΉΑ÷ΟΘ§ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ___________ΓΘ
ΒΡΖΔ…ζΉΑ÷ΟΩ…“‘―Γ”Ο_______(ΧνΉ÷ΡΗ¥ζΚ≈)ΉΑ÷ΟΘ§ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ___________ΓΘ
ΔΤ”ϊ ’Φ·“ΜΤΩΗ…‘οΒΡ¬»ΤχΘ§―Γ‘ώΚœ ΒΡΉΑ÷ΟΘ§ΤδΝ§Ϋ”Υ≥–ρΈΣ![]() ________________(ΧνΉ÷ΡΗ¥ζΚ≈)ΓΘ
________________(ΧνΉ÷ΡΗ¥ζΚ≈)ΓΘ
Δ« Β―ι “Ω…”ΟΆΦ ΨΉΑ÷Ο÷Τ±Η―«œθθΘ¬»Θ§Φλ―ιΉΑ÷ΟΤχΟή–‘≤ΔΉΑ»κ“©ΤΖΘ§¥ρΩΣ![]() Θ§»ΜΚσ‘Ό¥ρΩΣ
Θ§»ΜΚσ‘Ό¥ρΩΣ![]() Θ§Ά®»κ“ΜΕΈ ±ΦδΤχΧεΘ§ΤδΡΩΒΡ «____________Θ§»ΜΚσΫχ––ΤδΥϊ≤ΌΉςΘ§Β±Z÷–”–“ΜΕ®ΝΩ“ΚΧε…ζ≥… ±Θ§ΆΘ÷Ι Β―ιΓΘ
Θ§Ά®»κ“ΜΕΈ ±ΦδΤχΧεΘ§ΤδΡΩΒΡ «____________Θ§»ΜΚσΫχ––ΤδΥϊ≤ΌΉςΘ§Β±Z÷–”–“ΜΕ®ΝΩ“ΚΧε…ζ≥… ±Θ§ΆΘ÷Ι Β―ιΓΘ
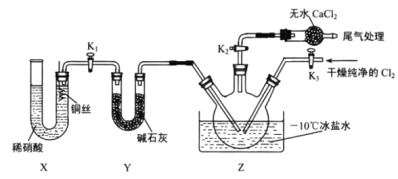
Δ»“―÷ΣΘΚClNOΥ°Ϋβ…ζ≥…![]() –¥≥ωΜ·―ßΖ¥”ΠΖΫ≥Χ Ϋ__________________ΓΘ
–¥≥ωΜ·―ßΖ¥”ΠΖΫ≥Χ Ϋ__________________ΓΘ
ΔΌ”ϊ…ηΦΤ Β―ι÷ΛΟς![]() «»θΥαΘ§–η―Γ‘ώ»γœ¬_____________ ‘ΦΝΩΣ’Ι Β―ι
«»θΥαΘ§–η―Γ‘ώ»γœ¬_____________ ‘ΦΝΩΣ’Ι Β―ι![]() Χν―Γœν
Χν―Γœν![]() ΓΘ
ΓΘ
A. ![]() »ή“Κ B.
»ή“Κ B. ![]() »ή“Κ C. Κλ…Ϊ ·»ο ‘÷Ϋ D. άΕ…Ϊ ·»ο ‘÷Ϋ
»ή“Κ C. Κλ…Ϊ ·»ο ‘÷Ϋ D. άΕ…Ϊ ·»ο ‘÷Ϋ
![]() “―÷Σœ¬Ν–Έο÷ ‘Ύ≥ΘΈ¬œ¬ΒΡ
“―÷Σœ¬Ν–Έο÷ ‘Ύ≥ΘΈ¬œ¬ΒΡ![]() »γΆΦΘΚ
»γΆΦΘΚ
Ά®Ιΐ“‘œ¬ Β―ι≤βΕ®ClNO―υΤΖΒΡ¥ΩΕ»ΓΘ»ΓZ÷–ΥυΒΟ“ΚΧε![]() »ή”ΎΥ°Θ§≈δ÷Τ≥…
»ή”ΎΥ°Θ§≈δ÷Τ≥…![]() »ή“ΚΘΜ»Γ≥ω
»ή“ΚΘΜ»Γ≥ω![]() ―υΤΖ»ή”ΎΉΕ–ΈΤΩ÷–Θ§”Ο
―υΤΖ»ή”ΎΉΕ–ΈΤΩ÷–Θ§”Ο![]() ±ξΉΦ»ή“ΚΒΈΕ®÷Ν÷’ΒψΘ§”ΠΦ”»κΒΡ÷Η ΨΦΝ «_______________ΓΘ
±ξΉΦ»ή“ΚΒΈΕ®÷Ν÷’ΒψΘ§”ΠΦ”»κΒΡ÷Η ΨΦΝ «_______________ΓΘ
A.![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
œϊΚΡ±ξΉΦ»ή“ΚΒΡΧεΜΐΈΣ![]() Θ§ΒΈΕ®÷’ΒψΒΡœ÷œσ « ________________Θ§―«œθθΘ¬»
Θ§ΒΈΕ®÷’ΒψΒΡœ÷œσ « ________________Θ§―«œθθΘ¬»![]() ΒΡ÷ ΝΩΖ÷ ΐΈΣ________ΓΘ
ΒΡ÷ ΝΩΖ÷ ΐΈΣ________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫΪ0.1mol”–ΜζΜ·ΚœΈοA”κ±ξΉΦΉ¥Ωωœ¬5.6L―θΤχΜλΚœΘ§“ΜΕ®ΧθΦΰœ¬ΝΫ’ΏΆξ»ΪΖ¥”ΠΘ§÷Μ”–COΓΔCO2ΚΆH2O»ΐ÷÷≤ζΈοΘ§ΫΪ»Ϊ≤Ω≤ζΈο“ά¥ΈΆ®»κΉψΝΩΒΡ≈®ΝρΥαΚΆΦν ·Μ“÷–Θ§≈®ΝρΥα‘ω÷Ί5.4ΩΥΘ§Φν ·Μ“‘ω÷Ί4.4ΩΥΘ§ΜΙ”–±ξΉΦΉ¥Ωωœ¬2.24LΤχΧεΒΡ Θ”ύΘ§«σΘΚ
Θ®1Θ©”–ΜζΜ·ΚœΈοAΒΡΖ÷Ή” Ϋ_______Θ®“Σ«σ–¥≥ωΆΤάμΙΐ≥ΧΘ©ΘΜ
Θ®2Θ©»τ”–ΜζΜ·ΚœΈοAΡή”κΡΤΖ¥”ΠΖ≈≥ω«βΤχΘ§«κ–¥≥ωAΒΡΫαΙΙΦρ Ϋ_________ΘΜ
Θ®3Θ©–¥≥ωΥυ”–±»AΕύ“ΜΗωΓΣCH2ΓΣ‘≠Ή”Ά≈ΒΡΆ§œΒΈοΒΡΫαΙΙΦρ Ϋ_________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com