
【题目】W,X,Y,Z,N六种主族元素,它们在周期表中位置如图所示,下列说法不正确的是( ) 
A.原子半径:X>Y>W
B.单质的氧化性:W>Z
C.溴与元素M同主族,气态氢化物的稳定性比M的强
D.元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.用酸性高锰酸钾溶液可以鉴别己烯、甲苯和苯
B.用系统命名法命名顺﹣2﹣丁烯、反﹣2﹣丁烯分别与HCl加成产物的结果不同
C.聚乳酸(  )分子中存在酯基、羧基、羟基
)分子中存在酯基、羧基、羟基
D.有机物CH3CO18OH和C2H5OH在浓硫酸催化作用下产物为CH3CO18OC2H5和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中10种元素回答以下问题:

Ⅰ.填写下列空白:
(1)写出⑧元素在周期表的位置______________________;
(2)实验室制取②氢化物的化学方程式_______________________________________;
②的氢化物与其最高价氧化物水化物反应生成的物质是________________(填名称)
(3)⑦的氯化物物理性质非常特殊,如熔点为190℃,但在180℃就开始升华。据此判断该氯化物是________(填“共价化合物”或“离子化合物”),可以证明你判断正确的实验依据为:_____________________________________________________________________。
(4)用电子式表示④、⑥两元素结合成化合物的形成过程____________________________。
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂;X是一种氢化物,常温下为液体,则:
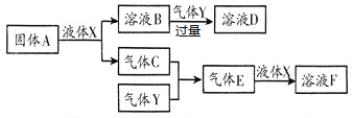
(1)A的电子式为_________________;
(2)气体Y是一种大气污染物,无色有刺激性气味,直接排放会形成酸雨。写出溶液D与酸性高锰酸钾溶液反应的离子方程式:_________________________________________;
(3)在含2molF的浓溶液中加入1mol锌片加热使之充分反应,产生气体的体积为_____ L(标准状况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸苯甲酯( ![]() )广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精.已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯.其合成路线如下:
)广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精.已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯.其合成路线如下: 
据此回答下列问题:
(1)X生成Y的化学方程式为 , 生成物Y中含有官能团的名称为 .
(2)![]() 发生反应④所需的条件是 , 该反应的反应类型为 .
发生反应④所需的条件是 , 该反应的反应类型为 .
(3)实验室为鉴别A和B两者的水溶液,可以选用的化学试剂是 .
A.纯碱溶液
B.NaOH溶液
C.金属钠
D.银氨溶液
(4)上述反应①~⑤中原子的理论利用率为100%、符合绿色化学要求的反应是(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,表中的①~⑧中元素,用元素符号或化学式填空回答:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | |||||
三 | ④ | ⑤ | ⑥ | ⑦ | ||||
四 | ⑧ |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为___________。
(2)②元素的原子L层有______个电子,其最高价氧化物的化学式为________,气态氢化物的化学式为________,实验室制备其气态氢化物的化学方程式为__________。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是_______,碱性最强的是______,呈两性的是__________________。
(5)写出①单质在空气中燃烧的化学方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同质量的SO2和SO3它们之间的关系是
A. 所含硫原子的物质的量之比为1:1
B. 氧原子的物质的量之比为3:2
C. 氧元素的质量比为5:6
D. 硫元素的质量比为4:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法正确的是( )
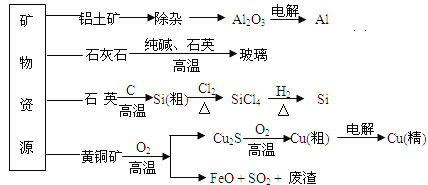
(注:铝土矿中含有A12O3、SiO2、Fe2O3)
A. 在铝土矿制备较高纯度A1的过程中只用到NaOH溶液、CO2气体、冰晶石
B. 石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C. 在制粗硅时,氧化剂与还原剂的物质的量之比为1∶2
D. 黄铜矿(CuFeS2)与O2反应产生的Cu2S、SO2均是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定碳酸钠和碳酸氢钠混合样品中碳酸氢钠的质量分数,可通过加热分解得到的CO2质量进行计算,某同学设计的实验装置示意图如图: 
请回答:
(1)仪器a的作用是 .
(2)装置B中冰水的作用是 .
(3)该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸氢钠的质量分数偏低的是 .
A.样品分解不完全
B.装置
C.C之间缺少CO2的干燥装置
D.产生CO2气体的速率太快,没有被碱石灰完全吸收
E.反应完全后停止加热,通入过量的空气.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com