
【题目】下列说法正确的是( )
A.用酸性高锰酸钾溶液可以鉴别己烯、甲苯和苯
B.用系统命名法命名顺﹣2﹣丁烯、反﹣2﹣丁烯分别与HCl加成产物的结果不同
C.聚乳酸(  )分子中存在酯基、羧基、羟基
)分子中存在酯基、羧基、羟基
D.有机物CH3CO18OH和C2H5OH在浓硫酸催化作用下产物为CH3CO18OC2H5和H2O
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】下列有机反应方程式书写错误的是( )
A.![]() +HNO3
+HNO3 ![]()
![]() +H2O
+H2O
B.CH2═CH2+H2O ![]() CH3CH2OH
CH3CH2OH
C.2CH3CHO+O2 ![]() 2CH3COOH
2CH3COOH
D.CH4+Cl2 ![]() CH3Cl+HCl
CH3Cl+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为V L的密闭容器中通入a mol CO和b mol O2,点燃充分反应后容器内碳原子数和氧原子数之比为( )
A. a:b B. a:2b
C. a:(a+2b) D. a:2(a+b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某课外小组制取乙炔并测定乙炔的某些性质的实验. 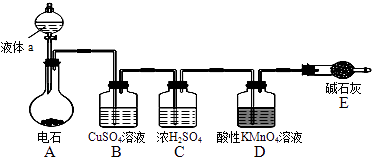
(1)写出实验室制取乙炔的化学方程式: .
(2)实验室制取乙炔时,分液漏斗中的液体a通常是 .
(3)CuSO4溶液的作用是 .
(4)装置D中的现象是: .
(5)工业上常用乙炔、饱和食盐水等物质作原料来合成聚氯乙烯,请写出相关方程式:
; ; ; .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。已知NOCl是一种红褐色液体或黄色气体,其熔点64.5℃,沸点5.5℃,遇水易水解。
(1)实验室制备原料气NO和Cl2的装置如下图所示:

①实验室制NO时,装置A中烧瓶内发生反应的化学方程式为_______。
②实验室制Cl2时,装置B中盛放的试剂为________,其作用是________。
(2)将上述收集到的Cl2充入集气瓶中,按图示装置制备亚硝酰氯。
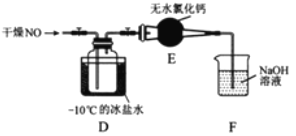
①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为________。
②装置D中的现象为________。
③装置E中无水氯化钙的作用为________。
④某同学认为装置F不能吸收NO,为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是________。
(3)NO可用间接电化学法除去,其原理如下图所示:

①阴极的电极反应式为______________________。
②吸收塔内发生反应的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用H++ OH-= H2O来表示的化学反应是( )
A. CuO溶于稀H2SO4 B. 澄清石灰水和HNO3溶液反应
C. KOH溶液和碳酸溶液反应 D. Ba(OH)2溶液和H2SO4溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.纳米材料是指一种称为“纳米”的新物质制成的材料
B.复合材料一般有强度高、质量轻、耐高温、耐腐蚀等优异性能,其综合性质超过了单一材料
C.淀粉和纤维素通式都是(C6H10O5)n , 都是天然高分子化合物
D.合成纤维的主要原料是石油、天然气、煤等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年6月20日,2016年全球最受关注的十大化学成果发布,其中有两项与空气中的二氧化碳处理利用技术有关。其一为美国伊利诺斯大学芝加哥分校和阿贡国家实验室科学家联合设计的新型太阳能电池,可直接把大气中的二氧化碳转化为合成气(CO和H2)该设计同时具有环保和经济价值,不仅可以减缓二氧化碳的排放,而且可以生成重要的化工原料。
(1)下列材料也可以用于制造太阳能电池的是____________。
A.Ag2O B.Fe3O4 C.Si D.SiO2
(2)下图装置可实现二氧化碳到一氧化碳的转化

①电源的正极为______(“A”或“B")。
②阴极发生反应的电极方程式为:___________.
(3)CO 和H2可用于合成甲醇。
①已知CO、H2、CH3OH(1)的燃烧热为283.0kJ/mol、285. 8kJ/mol、726.5kJ/mol,写出 由CO和H2制备CH3OH(1)的热化学方程式__________。
②在398K,1L的恒容容器中充入0.1molCO和0.2molH2,发生反应CO(g)+2H2(g)=CH3OH(g),反应过程中气体的压强如下表所示(atm为标准大气压)。
时间(min) | 0 | 1 | 5 | 10 | 30 | 50 |
压强(atm) | 10 | 9.3 | 8.0 | 7.2 | 4 | 4 |
5min内该反应的平均速率用CO可表示为______,该温度下的平衡常数是_____。达到平衡后,向该容器中通入0.05mol的气态CH3OH,再次达到平衡时,CH3OH的体积分数比原平衡时_____( 填“大”或“小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W,X,Y,Z,N六种主族元素,它们在周期表中位置如图所示,下列说法不正确的是( ) 
A.原子半径:X>Y>W
B.单质的氧化性:W>Z
C.溴与元素M同主族,气态氢化物的稳定性比M的强
D.元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com