
°æƒø°øœ¬±Ì «‘™Àÿ÷Ð∆⁄±Ìµƒ“ª≤ø∑÷£¨’Î∂‘±Ì÷–µƒ¢Ÿ°´¢‚÷–10÷÷‘™Àÿªÿ¥“‘œ¬Œ £∫

¢Ò£ÆÃÓ–¥œ¬¡–ø’∞◊£∫
£®1£©–¥≥ˆ¢ý‘™Àÿ‘⁄÷Ð∆⁄±ÌµƒŒª÷√______________________£ª
£®2£© µ—È “÷∆»°¢⁄«‚ªØŒÔµƒªØ—ß∑Ω≥à Ω_______________________________________£ª
¢⁄µƒ«‚ªØŒÔ”Î∆‰◊Ó∏þº€—ıªØŒÔÀƪ،Ô∑¥”¶…˙≥…µƒŒÔ÷ «________________£®ÃÓ√˚≥∆£©
£®3£©¢þµƒ¬»ªØŒÔŒÔ¿Ì–‘÷ ∑«≥£Ãÿ ‚£¨»Á»€µ„Œ™190°Ê£¨µ´‘⁄180°ÊæÕø™ º…˝ª™°£æð¥À≈–∂œ∏√¬»ªØŒÔ «________(ÃÓ°∞π≤º€ªØ∫œŒÔ°±ªÚ°∞¿Î◊”ªØ∫œŒÔ°±)£¨ø…“‘÷§√˜ƒ„≈–∂œ’˝»∑µƒ µ—È“¿æðŒ™£∫_____________________________________________________________________°£
£®4£©”√µÁ◊” Ω±Ì æ¢Ð°¢¢Þ¡Ω‘™ÀÿΩ·∫œ≥…ªØ∫œŒÔµƒ–Œ≥…π˝≥Ã____________________________°£
¢Ú£Æ”……œ ˆ≤ø∑÷‘™Àÿ◊È≥…µƒŒÔ÷ º‰£¨‘⁄“ª∂®Ãıº˛œ¬£¨ø…“‘∑¢…˙œ¬Õº÷–µƒ±‰ªØ£¨∆‰÷–A «“ª÷÷µ≠ª∆…´πÃã¨ø…◊˜π©—ıº¡£ªX «“ª÷÷«‚ªØŒÔ£¨≥£Œ¬œ¬Œ™“∫㨑ڣ∫
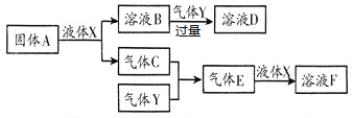
£®1£©AµƒµÁ◊” ΩŒ™_________________£ª
£®2£©∆¯ÃÂY «“ª÷÷¥Û∆¯Œ€»æŒÔ£¨ŒÞ…´”–¥Ãº§–‘∆¯Œ∂£¨÷±Ω”≈≈∑≈ª·–Œ≥…À·”Í°£–¥≥ˆ»Ð“∫D”ÎÀ·–‘∏þ√ÃÀ·ºÿ»Ð“∫∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫_________________________________________£ª
£®3£©‘⁄∫¨2molFµƒ≈®»Ð“∫÷–º”»Î1mol–ø∆¨º”»» π÷Æ≥‰∑÷∑¥”¶£¨≤˙…˙∆¯ÃµƒÃª˝Œ™_____ L£®±Í◊º◊¥øˆœ¬£©
°æ¥∞∏°ø µ⁄»˝÷Ð∆⁄µ⁄IVA◊£® 2NH4Cl + Ca(OH)2==°˜==CaCl2 + 2H2O + 2NH3°¸ œıÀ·Ôß π≤º€ªØ∫œŒÔ ¬»ªØ¬¡‘⁄»€»⁄◊¥Ã¨œ¬≤ªƒÐµºµÁ ![]()
![]() 2MnO4- +5HSO3-+ H+£Ω 3H2O+5SO42-+2Mn2+ 22.4
2MnO4- +5HSO3-+ H+£Ω 3H2O+5SO42-+2Mn2+ 22.4
°æΩ‚Œˆ°ø£®1£©∏˘æð‘™Àÿ÷Ð∆⁄±Ì÷™¢ý‘™ÀÿŒ™¡Ú£¨‘⁄÷Ð∆⁄±ÌµƒŒª÷√µ⁄»˝÷Ð∆⁄µ⁄IVA◊°£
£®2£©∏˘æð‘™Àÿ÷Ð∆⁄±Ì÷™¢⁄Œ™N‘™Àÿ£¨«‚ªØŒÔµƒªØ—ß ΩŒ™NH3°£ µ—È “”√NH4Cl ∫Õ Ca(OH)2Õ®π˝º”»»∑¥”¶£¨…˙≥…CaCl2 °¢H2O ∫ÕNH3°¸¿¥÷∆»°NH3£¨∑¥”¶∑Ω≥Ã ΩŒ™2NH4Cl+ Ca(OH)![]() CaCl2 +2H2O+2NH3°¸°£¥∞∏£∫2NH4Cl+Ca(OH)
CaCl2 +2H2O+2NH3°¸°£¥∞∏£∫2NH4Cl+Ca(OH)![]() CaCl2+2H2O+2NH3°¸°£¢⁄µƒ«‚ªØŒÔŒ™NH3£¨◊Ó∏þº€—ıªØŒÔµƒÀƪ،Ԍ™HNO3¡Ω’þ∑¥”¶…˙≥…œıÀ·Ôߣ¨À˘“‘¥∞∏Œ™£∫œıÀ·Ôß°£
CaCl2+2H2O+2NH3°¸°£¢⁄µƒ«‚ªØŒÔŒ™NH3£¨◊Ó∏þº€—ıªØŒÔµƒÀƪ،Ԍ™HNO3¡Ω’þ∑¥”¶…˙≥…œıÀ·Ôߣ¨À˘“‘¥∞∏Œ™£∫œıÀ·Ôß°£
£®3£©“ÚŒ™¢þŒ™Al,À¸µƒµƒ¬»ªØŒÔŒ™AlCl3∏˘æðÀ¸µƒ»€µ„Œ™190°Ê£¨µ´‘⁄180°ÊæÕø™ º…˝ª™°£»€∑–µ„∂º∫еգ¨À˘“‘≈–∂œ∏√¬»ªØŒÔ «π≤º€ªØ∫œŒÔ£¨ø…“‘÷§√˜ƒ„≈–∂œ’˝»∑µƒ µ—È“¿æðŒ™£∫¬»ªØ¬¡‘⁄»€»⁄◊¥Ã¨œ¬≤ªƒÐµºµÁ°£
£®4£©“ÚŒ™¢ÐŒ™F°¢¢ÞŒ™Mg,”√µÁ◊” Ω±Ì æ¡Ω‘™ÀÿΩ·∫œ≥…ªØ∫œŒÔµƒ–Œ≥…π˝≥ÃŒ™£∫
![]()
II£®1£©”…A «µ≠ª∆…´πÃÃÂø…◊˜π©—ıº¡÷™AŒ™Na2O2πÃã¨∆‰µÁ◊” ΩŒ™![]()
(2)∏˘æðøÚÕº∫Õ÷ æ÷™£¨C «O2£¨Y «SO2£¨E «SO3£¨F «¡ÚÀ·£¨∆¯ÃÂC”Î∆¯ÃÂY∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫SO2+O2![]() 2SO3
2SO3
£®3£©“ÚŒ™F¡ÚÀ·£¨‘⁄∫¨2mol≈®¡ÚÀ·»Ð“∫÷–º”»Î1mol–ø∆¨º”»»ø…ƒÐ∑¢…˙µƒ∑¥”¶£¨![]() Zn+H2SO4= ZnSO4+H2
Zn+H2SO4= ZnSO4+H2![]() £¨∏˘æð∑¥”¶πÿœµZn
£¨∏˘æð∑¥”¶πÿœµZn![]() SO2; Zn
SO2; Zn![]() 2,÷™µ¿1mol–ø∆¨ÕÍ»´∑¥”¶∑≈≥ˆ∆¯ÃÂŒ™1mol£¨∆‰∆¯Ã‘⁄±Íøˆœ¬Œ™22.4L¥∞∏£∫22.4°£
2,÷™µ¿1mol–ø∆¨ÕÍ»´∑¥”¶∑≈≥ˆ∆¯ÃÂŒ™1mol£¨∆‰∆¯Ã‘⁄±Íøˆœ¬Œ™22.4L¥∞∏£∫22.4°£



| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø‘⁄ê˝Œ™V Lµƒ√б’»ð∆˜÷–Õ®»Îa mol CO∫Õb mol O2£¨µ„»º≥‰∑÷∑¥”¶∫Û»ð∆˜ƒ⁄ú‘≠◊” ˝∫Õ—ı‘≠◊” ˝÷Ʊ»Œ™(°°°°)
A. a:b B. a:2b
C. a:(a£´2b) D. a:2(a£´b)
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡–Àµ∑®≤ª’˝»∑µƒ «£®°°°°£©
A.ƒ…√◊≤ƒ¡œ «÷∏“ª÷÷≥∆Œ™°∞ƒ…√◊°±µƒ–¬ŒÔ÷ ÷∆≥…µƒ≤ƒ¡œ
B.∏¥∫œ≤ƒ¡œ“ª∞„”–«ø∂»∏þ°¢÷ ¡ø«·°¢ƒÕ∏þŒ¬°¢ƒÕ∏Ø ¥µ»”≈“Ï–‘ƒÐ£¨∆‰◊€∫œ–‘÷ ≥¨π˝¡Àµ•“ª≤ƒ¡œ
C.µÌ∑€∫ÕœÀŒ¨ÀÿÕ® Ω∂º «£®C6H10O5£©n £¨ ∂º «ÃÏ»ª∏þ∑÷◊”ªØ∫œŒÔ
D.∫œ≥…œÀŒ¨µƒ÷˜“™‘≠¡œ « ؔհ¢ÃÏ»ª∆¯°¢√∫µ»
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øΩÒƒÍ6‘¬20»’,2016ƒÍ»´«Ú◊Ó Ðπÿ◊¢µƒ ƥ۪ؗß≥…π˚∑¢≤º,∆‰÷–”–¡ΩœÓ”Îø’∆¯÷–µƒ∂˛—ıªØú¥¶¿Ì¿˚”√ºº ı”–πÿ°£∆‰“ªŒ™√¿π˙“¡¿˚≈µÀπ¥Û—ß÷•º”∏Á∑÷–£∫Õ∞¢π±π˙º“ µ—È “ø∆—ߺ“¡™∫œ…˺∆µƒ–¬–Õô—كеÁ≥ÿ,ø…÷±Ω”∞—¥Û∆¯÷–µƒ∂˛—ıªØú◊™ªØŒ™∫œ≥…∆¯(CO∫ÕH2)∏√…˺∆Õ¨ ±æþ”–ª∑±£∫Õæ≠º√º€÷µ,≤ªΩˆø…“‘ºıª∫∂˛—ıªØúµƒ≈≈∑≈,∂¯«“ø…“‘…˙≥…÷ÿ“™µƒªØπ§‘≠¡œ°£
£®1£©œ¬¡–≤ƒ¡œ“≤ø…“‘”√”⁄÷∆‘Ïô—كеÁ≥ÿµƒ «____________°£
A.Ag2O B.Fe3O4 C.Si D.SiO2
£®2£©œ¬Õº◊∞÷√ø… µœ÷∂˛—ıªØúµΩ“ª—ıªØúµƒ◊™ªØ

¢ŸµÁ‘¥µƒ’˝º´Œ™______(°∞A°±ªÚ°∞B")°£
¢⁄“ıº´∑¢…˙∑¥”¶µƒµÁº´∑Ω≥Ã ΩŒ™:___________.
£®3£©CO ∫ÕH2ø…”√”⁄∫œ≥…º◊¥º°£
¢Ÿ“—÷™CO°¢H2°¢CH3OH(1)µƒ»º…’»»Œ™283.0kJ/mol°¢285. 8kJ/mol°¢726.5kJ/mol,–¥≥ˆ ”…CO∫ÕH2÷∆±∏CH3OH(1)µƒ»»ªØ—ß∑Ω≥à Ω__________°£
¢⁄‘⁄398K£¨1Lµƒ∫„»ð»ð∆˜÷–≥‰»Î0.1molCO∫Õ0.2molH2,∑¢…˙∑¥”¶CO(g)+2H2(g)=CH3OH(g),∑¥”¶π˝≥Ã÷–∆¯Ãµƒ—π«ø»Áœ¬±ÌÀ˘ æ(atmŒ™±Í◊º¥Û∆¯—π)°£
±º‰(min) | 0 | 1 | 5 | 10 | 30 | 50 |
—π«ø(atm) | 10 | 9.3 | 8.0 | 7.2 | 4 | 4 |
5minƒ⁄∏√∑¥”¶µƒ∆Ωæ˘ÀŸ¬ ”√COø…±Ì 挙______,∏√Œ¬∂»œ¬µƒ∆Ω∫‚≥£ ˝ «_____°£¥ÔµΩ∆Ω∫‚∫Û£¨œÚ∏√»ð∆˜÷–Õ®»Î0.05molµƒ∆¯Ã¨CH3OH,‘Ÿ¥Œ¥ÔµΩ∆Ω∫‚ ±,CH3OHµƒÃª˝∑÷ ˝±»‘≠∆Ω∫‚ ±_____( ÃÓ°∞¥Û°±ªÚ°∞–°°±)°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡–¥Î ©ƒÐº”øÏFe”Î0.1mol/Lµƒœ°H2SO4∑¥”¶≤˙…˙H2µƒ∑¥”¶ÀŸ¬ µƒ «£® £©
A.‘ˆº”Feµƒ”√¡øB.ΩµµÕŒ¬∂»
C.Ω´œ°¡ÚÀ·∏ƒŒ™98%µƒ≈®¡ÚÀ·D.µŒº”…Ÿ¡øµƒCuSO4»Ð“∫
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡–”Δ–ª˙ŒÔΩ·ππ°¢–‘÷ œýπÿµƒ– ˆ≤ª’˝»∑µƒ «£® £©
A.±Ω∑÷◊”÷–À˘”–‘≠◊”æ˘‘⁄Õ¨“ª∆Ω√Ê
B.º◊ÕÈ «“ª÷÷ŒÞ…´£¨”–≥ÙŒ∂µƒ∆¯ÃÂ
C.º◊ÕÈ∫Õ¬»∆¯∑¥”¶…˙≥…“ª¬»º◊ÕȔαΩ∫ÕœıÀ·∑¥”¶…˙≥…œıª˘±Ωµƒ∑¥”¶¿ý–ÕœýÕ¨
D.±Ω≤ªƒÐ π‰ÂÀÆ“Ú∑¢…˙ªØ—ß∑¥”¶Õ …´
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øA°¢B°¢C°¢D «‘™Àÿ÷Ð∆⁄±Ì÷–«∞10∫≈‘™Àÿ£¨À¸√«µƒ‘≠◊”∞Îæ∂“¿¥Œºı–°£ÆDƒÐ∑÷±”ÎA°¢B°¢C–Œ≥…µÁ◊”◊Ð ˝œýµ»µƒ∑÷◊”M°¢N°¢W£¨«“‘⁄M°¢N°¢W∑÷◊”÷–£¨A°¢B°¢C »˝‘≠◊”∂º≤…»°sp3‘”ªØ£Æ
£®1£©A°¢B°¢Cµƒµ⁄“ªµÁ¿ÎƒÐ”…–°µΩ¥ÛµƒÀ≥–ÚŒ™£®”√‘™Àÿ∑˚∫≈±Ì 棩£Æ
£®2£©M «∫¨”–£®ÃÓ°∞º´–‘°±ªÚ°∞∑«º´–‘°±£©π≤º€º¸µƒ£®ÃÓ°∞º´–‘°±ªÚ°∞∑«º´–‘°±£©∑÷◊”£Æ
£®3£©W∑÷◊”µƒø’º‰ππ–ÕŒ™ £Æ
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øW£¨X£¨Y£¨Z£¨N¡˘÷÷÷˜◊‘™Àÿ£¨À¸√«‘⁄÷Ð∆⁄±Ì÷–Œª÷√»ÁÕºÀ˘ 棨œ¬¡–Àµ∑®≤ª’˝»∑µƒ «£® £© 
A.‘≠◊”∞Îæ∂£∫X£æY£æW
B.µ•÷ µƒ—ıªØ–‘£∫W£æZ
C.‰Â”Α™ÀÿMÕ¨÷˜◊£¨∆¯Ã¨«‚ªØŒÔµƒŒ»∂®–‘±»Mµƒ«ø
D.‘™ÀÿNŒª”⁄Ω Ù”Î∑«Ω Ùµƒ∑÷ΩÁœþ∏ΩΩ¸£¨ø…“‘Õ∆∂œN‘™Àÿµƒµ•÷ ø…◊˜∞εºÃÂ≤ƒ¡œ
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø¶©£Æ”√50mL 0.50mol/L—ŒÀ·∏˙50mL 0.55mol/L NaOH»Ð“∫÷–∫Õ∑¥”¶π˝≥Ã÷–À˘∑≈≥ˆµƒ»»¡øº∆À„÷–∫Õ»» °£
£®1£©…’±≠º‰ÃÓ¬˙≈ðƒ≠ÀСœµƒ◊˜”√ «___________________________________£ª
£®2£©¥Û…’±≠…œ»Ù≤ª∏«”≤÷Ω∞£¨«Ûµ√µƒ÷–∫Õ»» ˝÷µ______£®ÃÓ°∞∆´¥Û°±°¢°∞∆´–°°±°¢°∞ŒÞ”∞œÏ°±£©
£®3£©»ÁÕºÀ˘ 棨“«∆˜Aµƒ√˚≥∆ «____________________£ª

£®4£©÷ÿ∏¥»˝¥Œ µ—È£¨º«¬ºµƒ µ—È ˝æð»Áœ¬£∫
µ—È”√∆∑ | »Ð“∫Œ¬∂» | |||
t1 | t2 | |||
¢Ÿ | 50 mL 0.55 mol°§L-1 NaOH»Ð“∫ | 50 mL 0.5 mol°§L-1 HCl»Ð“∫ | 20 °Ê | 23.3 °Ê |
¢⁄ | 50 mL 0.55 mol°§L-1 NaOH»Ð“∫ | 50 mL 0.5 mol°§L-1 HCl»Ð“∫ | 20 °Ê | 25.5 °Ê |
¢€ | 50 mL 0.55 mol°§L-1 NaOH»Ð“∫ | 50 mL 0.5 mol°§L-1 HCl»Ð“∫ | 20 °Ê | 23.5 °Ê |
“—÷™£∫Q=cm¶§t£¨∑¥”¶∫ۻГ∫µƒ±»»»»ðcŒ™4.18 kJ°§°Ê-1°§kg-1£¨∏˜ŒÔ÷ µƒ√Ð∂»æ˘Œ™1 g°§cm-3°£º∆À„¶§H=___________kJ/mol
£®5£© µ—È÷–∏ƒ”√80mL 0.50mol/L—ŒÀ·∏˙100mL 0.55mol/L NaOH»Ð“∫Ω¯––∑¥”¶£¨”Î…œ ˆ µ—Èœý±»£¨À˘∑≈≥ˆµƒ»»¡ø______£®ÃÓ°∞œýµ»°¢°∞≤ªœýµ»°±£©£¨À˘«Û÷–∫Õ»»______£®ÃÓ°∞œýµ»°¢°∞≤ªœýµ»°±£©£Æ
¢Ú£Æƒ≥—–æø–‘—ßœ∞–°◊ȅ˺∆¡À“ª◊È µ—È¿¥ÃΩæø‘™Àÿ÷Ð∆⁄¬…°£º◊Õ¨—ß“ª¥Œ–‘ÕÍ≥…N°¢C°¢Siµƒ∑«Ω Ù–‘«ø»ıµƒ±»Ωœ£ª““Õ¨—ßÕÍ≥…¡À—ı‘™Àÿµƒ∑«Ω Ù–‘±»¡Ú«øµƒ µ—È°£

£®1£©¥”“‘œ¬À˘∏¯ŒÔ÷ ÷–—°≥ˆº◊Õ¨—߅˺∆µƒ µ—ÈÀ˘”√µΩŒÔ÷ £∫
¢Ÿœ°HNO3»Ð“∫¢⁄œ°—ŒÀ·¢€ÃºÀ·∏∆¢ÐNa2SiO3 »Ð“∫¢ðSiO2
‘º¡AŒ™_________£ª ‘º¡CŒ™_________£®ÃÓ–Ú∫≈£©
£®2£©““Õ¨—߅˺∆µƒ µ—ÈÀ˘”√µΩ ‘º¡AŒ™________£ª◊∞÷√C÷–∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™___________________________°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com