
【题目】(1)已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2 C(s)+O2(g)═CO2(g)△H3
则反应4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H的表达式为_____
(2)已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P 198,Cl—Cl 243,P—Cl 331。


则反应P4(白磷,s)+6Cl2(g)=4PCl3(s)的反应热ΔH=_____。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1 molCH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=_____。
【答案】12△H3+5△H2-2△H1 -1326 kJ·mol-1 -1160kJ/mol
【解析】
(1)已知:①6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
②2H2(g)+O2(g)═2H2O(g)△H2
③C(s)+O2(g)═CO2(g)△H3
由盖斯定律:5×②+12×③-2×①得:4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g) △H=12△H3+5△H2-2△H1;
(2)根据图示,1分子P4、PCl3中分别含有6个P—P键、3个P—Cl键,反应热为断裂6 mol P—P键、6 mol Cl—Cl键吸收的能量和形成12 mol P—Cl键放出的能量之差,即ΔH=(6×198 kJ·mol-1+6×243 kJ·mol-1)-12×331 kJ·mol-1=-1326 kJ·mol-1;
(3)1 molCH4还原NO2至N2,整个过程中放出的热量为867kJ,得反应③CH4(g)+2NO2(g)=N2(g) +CO2(g)+2H2O(g)ΔH3=-867kJ/mol;
已知①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
由盖斯定律:2×③-①得:②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=2×ΔH3-ΔH1=-1160kJ/mol。


科目:高中化学 来源: 题型:
【题目】下列关于氯气的说法不正确的是( )
A. 氯气和液氯是两种不同的物质
B. 可以用浓硫酸除去氯气中的水蒸气
C. 氯气是一种有毒气体,但可用于自来水的杀菌消毒
D. 尽管氯气的化学性质很活泼,但是纯净的液氯能用钢瓶贮存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计方案或判断中正确的是
A.加入足量铜粉后,搅拌、可过滤可除去Cu(NO3)2溶液中混有的AgNO3
B.通过装有NaOH溶液的确洗气瓶来除去CO2中混有的HCl气体
C.某无色未知溶液中加入BaCl2溶液,有白色沉淀,可推断溶液中的一定含有SO42-
D.未知溶液中加入盐酸产生使澄清石灰水变浑浊的气体,则溶液中一定大量含CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组同学用下图所示装置在实验室制氯气并探究其相关性质(夹持设备已略)。

(1)制备氯气选用的药品为:漂白粉固体和浓盐酸,相关的化学反应方程式为_______________。
(2)装置B的作用之一是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中①、②、③依次放入_____(选填表中字母)。
① | ② | ③ | |
a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 硅胶 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性强弱。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为________色,说明氯的非金属性大于溴;之后打开活塞,将装置D中少量溶液加入装置E中,振荡;观察到的现象是___________________,则说明溴的非金属性大于碘。
(5)有同学提出该实验方案仍有不足,请说明其中的不足及后果。
①_________________________;②______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.可用丁达尔效应区分溶液与胶体B.生石灰与水混合的过程只发生物理变化
C.从物质分类看纯碱既是碱又是盐D.CuSO4·5H2O是一种混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述正确的是( )
H++CH3COO-,下列叙述正确的是( )
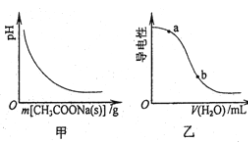
A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
C.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
D.0.10mol·L-1的CH3COOH溶液中加水稀释,溶液中c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】圣路易斯大学研制的新型乙醇燃料电池, 用能传递质子(H+)的介质作溶剂, 反应为C2H5OH+3O2→2CO2+3H2O,下图是该电池的示意图,下列说法正确的是( )

A.a极为电池的正极
B.电池正极的电极反应为:4H+ + O2 + 4e-=== 2H2O
C.电池工作时电流由a极沿导线经灯泡再到b极
D.电池工作时,1mol乙醇被氧化时就有6 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是_____________________________________。
(2)B中溶液发生反应的离子方程式是_________________________________________。
(3)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是___________________。
(4)过程Ⅲ实验的目的是___________________________________________________。
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下____________________,得电子能力逐渐减弱。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了有关晶体的知识其中错误的是( )
A | B | C | D | |
晶体 | 硫化钾 | 干冰 | 金刚石 | 碘 |
组成晶体的微粒 | 阴阳离子 | 分子 | 原子 | 分子 |
晶体微粒间存在的作用力 | 离子键 | 共价键 | 共价键 | 范德华力 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com