
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单的二苯乙炔类化合物是![]() 。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
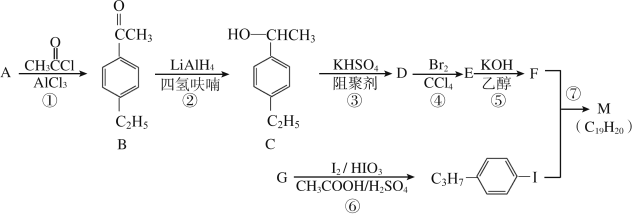
回答下列问题:
(1)A的结构简式为_______。
(2)D分子中最多有_____个碳原子共平面,与D化学式相同且符合下列条件的同分异构体有__种。(①与D具有相同的官能团,②苯环上的三元取代物)
(3)①的反应类型是________。
(4)⑤的化学方程式为________。
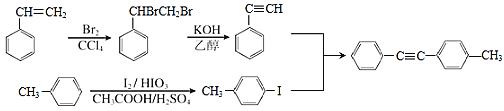
(5)参照上述合成路线,设计一条由苯乙烯和甲苯为起始原料制备![]() 的合成路线:______________。
的合成路线:______________。
【答案】 10 6 取代反应
10 6 取代反应 ![]()
【解析】
A、G是互为同系物的单取代芳烃,由B的结构可知反应①为取代反应,A为![]() ,B发生还原反应生成C,D能与溴的四氯化碳反应生成E,E在氢氧化钾、乙醇条件下反应得到F,可知E为卤代烃,D含有不饱和键,故反应③为消去反应,则D为
,B发生还原反应生成C,D能与溴的四氯化碳反应生成E,E在氢氧化钾、乙醇条件下反应得到F,可知E为卤代烃,D含有不饱和键,故反应③为消去反应,则D为![]() ,E为
,E为![]() ,F为
,F为![]() ,由M的分子式可知,反应⑦属于取代反应,M的结构简式为
,由M的分子式可知,反应⑦属于取代反应,M的结构简式为![]() ;A、G是互为同系物的单取代芳烃,结合反应⑥的产物可知G为
;A、G是互为同系物的单取代芳烃,结合反应⑥的产物可知G为![]() 。据此分析解答。
。据此分析解答。
(1)根据上述分析,A为![]() ,故答案为:
,故答案为:![]() ;
;
(2)D为![]() ,苯环为平面结构、碳碳双键为平面结构,碳碳单键可以旋转,使2个平面共面,即分子中所有的碳原子都可能共面,分子中最多有10个碳原子共平面。D的同分异构体与D具有相同的官能团且为苯环上的三元取代物,苯环上的取代基为:-CH3、-CH3、-CH=CH2,2个甲基有邻、间、对3种位置结构,对应的-CH=CH2分别有2种、3种、1种位置,故符合条件的同分异构体共有2+3+1=6种,故答案为:10;6;
,苯环为平面结构、碳碳双键为平面结构,碳碳单键可以旋转,使2个平面共面,即分子中所有的碳原子都可能共面,分子中最多有10个碳原子共平面。D的同分异构体与D具有相同的官能团且为苯环上的三元取代物,苯环上的取代基为:-CH3、-CH3、-CH=CH2,2个甲基有邻、间、对3种位置结构,对应的-CH=CH2分别有2种、3种、1种位置,故符合条件的同分异构体共有2+3+1=6种,故答案为:10;6;
(3)根据上述分析,反应①为取代反应,故答案为:取代反应;
(4)反应⑤为卤代烃的消去反应,反应的化学方程式为:![]() ,故答案为:
,故答案为:![]() ;
;
(5)以苯乙烯和甲苯为起始原料制备![]() 。根据题干流程图,需要合成
。根据题干流程图,需要合成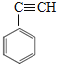 和
和![]() ;合成
;合成 ,可以由苯乙烯与溴发生加成反应得到
,可以由苯乙烯与溴发生加成反应得到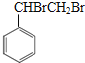 ,再在KOH/乙醇条件下发生消去反应生成
,再在KOH/乙醇条件下发生消去反应生成 ;合成
;合成![]() ,可以通过甲苯在I
,可以通过甲苯在I![]() ,最后
,最后 与
与![]() 发生取代反应得到
发生取代反应得到![]() ,合成路线为:
,合成路线为: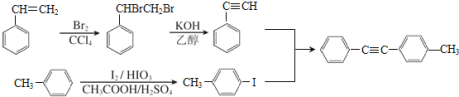 ,故答案为:
,故答案为: 。
。


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+OH→CH3COO+CH3CH2O+H2O
B. 醋酸溶液与新制氢氧化铜反应:2H++Cu(OH)2→Cu2++2H2O
C. 苯酚钠溶液中通入少量二氧化碳:2![]() +CO2+H2O
+CO2+H2O![]() 2
2![]() +CO
+CO![]()
D. 乙醛溶液与新制氢氧化铜碱性悬浊液共热CH3CHO+2Cu(OH)2+OH![]() CH3COO+ Cu2O↓+3H2O
CH3COO+ Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】紫草宁(shikonin,见下图)是从生长在亚洲学名叫Lithospermum erythrorhizon的一种植物的根部提取出来的红色化合物。几个世纪以来用做民间药物,如今用于配制治疗跌打损伤的膏药。下列说法不正确的是( )
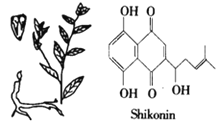
A. 紫草宁的分子式为C16H16O5
B. 等量的紫草宁与NaOH溶液、浓溴水反应,消耗NaOH、Br2 的物质的量之比为3:4
C. 紫草宁既能发生氧化反应又能发生还原反应
D. 常温下紫草宁不易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行如下实验,研究化学反应中的热量变化。
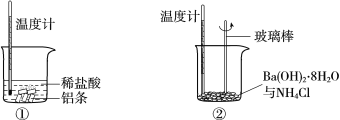
请回答下列问题:
(1)反应后①中温度升高,②中温度降低。由此判断铝条与盐酸的反应是________反应(填“放热”或“吸热”,下同),Ba(OH)2·8H2O与NH4Cl的反应是________反应。
(2)①中反应的离子方程式是_________,该反应的还原剂是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】凯夫拉纤维是生产防弹衣的主要材料之一,其结构片段如下:
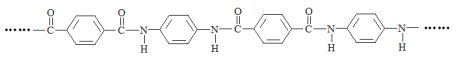
下列说法不正确的是( )
A. 凯夫拉纤维在发生水解反应的过程中,![]() 中的C—N键断裂
中的C—N键断裂
B. 凯夫拉纤维的结构简式为: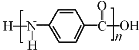
C. 完全水解产物的单个分子中,苯环上的氢原子具有相同的化学环境
D. 通过质谱法测定凯夫拉纤维的平均相对分子质量,可得其聚合度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有氧化还原反应:3H2O2 + 2H2CrO4 =2Cr(OH)3 + 3O2 ↑+ 2H2O
①用单线桥标出反应中的电子转移数目和方向_____________;
②其中Cr被___________,H2O2作___________剂;
③反应转移了0.3mol电子,则产生的气体在标准状态下体积约为__________。
(2)①将用砂纸打磨过的铝片用坩埚钳夹住在酒精灯上点燃,现象是:________;
②在试管中加入少量Na2O2再加入少量水,用带火星的木条伸入试管,再滴入几滴酚酞,可观察到的现象是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用饱和硫酸亚铁、浓硫酸和硝酸钾反应可以制得纯度为98%的NO,其反应为FeSO4+KNO3+H2SO4(浓)![]() Fe2(SO4)3+NO↑+K2SO4+H2O(未配平)。下列有关说法不正确的是
Fe2(SO4)3+NO↑+K2SO4+H2O(未配平)。下列有关说法不正确的是
A. 该反应的氧化剂是KNO3
B. 氧化产物与还原产物的物质的量之比为2∶3
C. Fe2(SO4)3、K2SO4、H2O均为电解质
D. 该反应中生成144gH2O,转移电子的物质的量为12mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Fe和Fe2O3组成的3.84 g 混合物中加入120 mL某浓度的盐酸,恰好完全反应,生成672mLH2(标准状况下),若向反应后的溶液中滴入几滴KSCN溶液,溶液不呈红色。试求:
(1)原混合物中Fe2O3和Fe的质量分别为_______、________;
(2)原盐酸的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应:COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H=-34kJ/mol
H2S(g)+CO2(g) △H=-34kJ/mol
氢解反应:COS(g)+H2(g) ![]() H2S(g)+CO(g) △H=+7kJ/mol。
H2S(g)+CO(g) △H=+7kJ/mol。
已知:2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol。
写出表示CO燃烧热的热化学方程式:______________。
(2)氢解反应达到平衡后,保持体系的温度和总压强不变,通入适量的He,正反应速率____(填“增大”“减小”或“不变”,下同),COS的转化率_______。
(3)某温度下,向体积为2L的恒容密闭容器中通入2molCOS(g)和4molH2O(g),发生水解反应,5min后反应达到平衡,测得COS(g)的转化率为75%。
回答下列问题:
①反应从起始至5min内,v(H2S)=_______mol·L-1·min-1。
②该温度下,上述水解反应的平衡常数K=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com