
【题目】有如下合成路线,甲经二步转化为丙,下列叙述不正确的是( ) 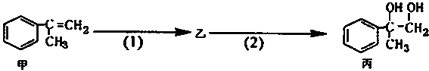
A.丙中可能含有未反应的甲,可用溴水检验是否含甲
B.反应(1)的无机试剂是液溴,铁作催化剂
C.甲和丙均可与酸性KMnO4溶液发生反应
D.反应(2)反应属于取代反应
【答案】B
【解析】解:甲中含有碳碳双键、丙中含有两个醇羟基,甲和溴发生加成反应生成乙,乙发生水解反应生成丙,
A.甲中含有碳碳双键、丙中含有醇羟基,甲能和溴发生加成反应而使溴水褪色、丙和溴不反应,所以可以用溴水检验是否含有甲,故A正确;
B.反应(1)是碳碳双键的加成反应,不需要催化剂,故B错误;
C.甲中含有碳碳双键、丙中含有醇羟基,所以二者都可以被酸性高锰酸钾溶液氧化,故C正确;
D.(2)属于卤代烃的水解反应,卤代烃的水解反应也属于取代反应,故D正确;
故选B.
【考点精析】根据题目的已知条件,利用有机物的结构和性质的相关知识可以得到问题的答案,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解.


科目:高中化学 来源: 题型:
【题目】电化学是研究电能与化学能相互转化的科学.请回答:
(1)原电池是将能转化为能的装置,一般较活泼的金属做
极,发生反应.电子流向极(填“正”或“负”).
(2)分析图,写出有关的电极反应式:
锌棒上的电极反应式为
碳棒上的电极反应式为 . 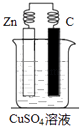
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将30mL 0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为( )
A.0.3 mol/LB.0.03 mol/LC.0.05 mol/LD.0.04 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是原子序数依次增大的前四周期元素,A是周期表中原子半径最小的元素,它们组成的单质或化合物有如图转化关系,其中甲、丙和戊是单质,乙、丁和己是氧化物,其中丁是两性氧化物,戊是紫红色金属。请回答下列问题:

(1)D元素的元素符号为______________,C元素在周期表中的位置为_____________。
(2)用电子式表示己的形成过程_____________。
(3)反应①在工业生产中通常称作_____________反应。
(4)甲、戊与浓硝酸可形成原电池,其中________________(填化学式)作负极,正极电极反应式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,能在溶液中大量共存的是( )
A.K+、H+、SO42-、OH-B.Na+、Ca2+、CO32-、NO3-
C.Na+、H+、Cl-、CO32-D.Na+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】参考下列(a)~(c)项回答问题:
(a)皂化值是使1g油脂皂化所需要的KOH的毫克数.
(b)碘值是使100g油脂加成碘的克数.
(c)各种油脂的皂化值、碘值列表如下:
花生油 | 亚麻仁油 | 牛油 | 黄油 | 硬化大豆油 | 大豆油 | |
皂化值 | 190 | 180 | 195 | 226 | 193 | 193 |
碘值 | 90 | 182 | 38 | 38 | 5 | 126 |
(1)单纯由(C17H33COO)3C3H5(相对分子质量884)形成的油,皂化值是
(2)在横线上填入适当的词句:
亚麻仁油比花生油所含的多,黄油比牛油的小.硬化大豆油的碘值小的原因是 .
(3)为使碘值为180的鱼油100g硬化所需要的H2的体积为升(标准状况下)?
(4)结构简式为 ![]() 的酯,若皂化值为430,求n为 .
的酯,若皂化值为430,求n为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体与其他分散系的本质区别在于( )
A. 胶体的分散系能通过滤纸空隙,而浊液的分散质不能
B. 分散质粒子直径大小不同
C. 产生丁达尔现象
D. 胶体在一定条件下能稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的溶液中,能够大量共存的离子组是
A. Al3+、Ca2+、Cl-、NO3- B. Ba2+、K+、CO32-、Cl-
C. Na+、Cu2+、NO3-、HCO3- D. Na+、Fe2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素为原子序数依次增大的短周期元素。A为原子半径最小的元素,A和B可形成4原子10电子的分子X;C的最外层电子数是内层的3倍;D原子的最外层电子数是最内层电子数的一半;E是地壳中含量最多的金属元素;F元素的最高正价与最低负价代数和为6。请回答下列问题:
(1)A和C按原子个数比1∶1形成4原子分子Y,Y的结构式是___________。
(2)分子X的电子式是__________;D可以在液态X中发生类似于与A2C的反应,写出反应的化学方程式_________________________________。
(3)实验证明,熔融的EF3 不导电,其原因是_______________________。
(4)E的单质可溶于A、C、D形成的化合物Z的水溶液中。拉曼光谱证实此反应生成的阴离子主要以E(CA)4- 的形式存在,写出E溶于Z溶液的离子方程式:_____________________。
(5)工业品Z的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
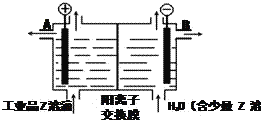
①该电解槽的阳极反应式是_________________。
②通电开始后,阴极附近溶液pH___________(“增大”、“减小”或“不变”)。
③除去杂质后的Z溶液从液体出口_________(填写“A”或“B”)导出。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com