
【题目】实验过程中,下列溶液的导电能力变化不大的是
A. ![]() 溶液中滴入
溶液中滴入![]() 溶液至过量
溶液至过量
B. 醋酸溶液中滴入氨水至过量
C. 澄清石灰水中通入![]() 至过量
至过量
D. ![]() 溶液中加入适量的NaOH固体
溶液中加入适量的NaOH固体
【答案】D
【解析】导电能力的大小,要比较单位体积内离子浓度的大小。A、氢氧化钡是强电解质,加入硫酸后,反应生成硫酸钡沉淀和水,导电能力下降直至为零,然后随着H2SO4溶液的滴入,导电性增强,A错误;B、醋酸是弱酸,导电能力不大,加入氨水后,生成醋酸铵是强电解质,导电能力增强,导电性变化大,B错误;C、氢氧化钙是强电解质,通入二氧化碳后会产生白色沉淀碳酸钙和水,导电能力几乎变为零,再通入二氧化碳,会生成碳酸氢钙,导电性又会逐渐增强,溶液的导电能力变化较大,C错误;D、氯化铵为强电解质,加入NaOH后生成弱电解质一水合氨和强电解质NaCl,离子的浓度变化不大,故导电性变化不大,D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中常含有的NOx、SO2、H2S等污染物,容易形成酸雨,破坏环境。其综合治理是当前重要的研究课题。
Ⅰ.以下是对酸雨的若干项评价,其中不正确的是__________
a.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.导致臭氧层空洞
d.二氧化碳的过量排放,是形成酸雨的主要原因之一
Ⅱ.电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。

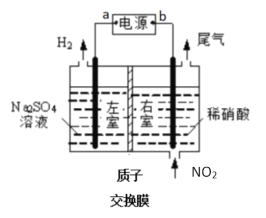
(1)电解NO制备NH4NO3原理如上方左图所示:
①阳极为石墨_____(填1或2),该电极的反应式为_____________。
②为使电解的副产物也完全转化为NH4NO3,需要补充的物质X的化学式为___________。
(2)用上方右图装置进行模拟电解NO2气体实验,可回收硝酸。
①外接电源a极为______极,左室发生的电极反应式为_____________。
②若有标准状况下2.24L NO2被吸收,通过质子交换膜(只允许质子通过)的H+为______mol。
③用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中增加了1 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28L H2。原气体中NO和NO2的体积比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿的主要成分是Al2O33H2O,还含有SiO2、Fe2O3等杂质。工业上从铝土矿中提取Al可采用如图所示工艺流程。(部分操作名称及反应条件已略去)

(1)B是___,X是___,若将盐酸与X互换,则B是___。
(2)生成C的离子方程式是___。
(3)D中的溶质是___,通入CO2后生成F的化学方程式是___,F的一种用途是___。
(4)由M生成铝的化学方程式是___,当有5.4g铝生成时,转移电子___mol。
(5)上述流程中的CO2能否用盐酸代替?理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业的重要反应之一:2SO2(g)+O2(g)![]() 2SO3(g)下列叙述不正确的是( )
2SO3(g)下列叙述不正确的是( )
A.其他条件不变,升高温度可增大SO3的生成速率
B.使用合适的催化剂,是为了增大化学反应速率
C.该反应达到化学平衡状态时,SO2可100%转化为SO3
D.该反应达到化学平衡状态时,SO3的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K 时,把0.5 mol N2O4气体通入体积为5 L的真空密闭容器中,立即出现红棕色。反应进行到2 s时,NO2的浓度为0.02 mol/L。在60 s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法正确的是
A.前2 s,以N2O4浓度变化表示的平均反应速率为0.01 mol·L-1·s-1
B.在2 s时,体系内压强为反应前的1.1倍
C.平衡时,体系内含N2O40.25 mol
D.平衡时,若往容器内充入氮气,则可提高N2O4的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
A. 该溶液的pH=4 B. 升高温度,溶液的pH增大 C. 此酸的电离平衡常数约为1×10-7 D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某实验小组探究碳酸氢铵溶液中各微粒物质的量浓度随溶液pH的变化如图所示(忽略溶液体积变化),则下列说法错误的是( )
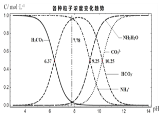
A.由图可知碳酸的Ka1数量级约为10-7
B.向NH4HCO3溶液加入与NH4HCO3等物质的量NaOH的溶液,HCO3-会先与NaOH反应
C.常温下将NH4HCO3固体溶于水,溶液显碱性
D.NH4HCO3作肥料时不能与草木灰混用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.水是极弱的电解质,它能微弱电离生成相同物质的量的H+和OH-
B.稀溶液中c(H+)c(OH-)=KW,任何条件下KW都保持不变
C.无论在什么条件下,中性溶液的c(H+)一定等于1×10-7mol/L
D.H2O![]() H++OH-是一吸热反应,所以温度升高,KW也随之减小
H++OH-是一吸热反应,所以温度升高,KW也随之减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,H2CO3的Ka1=4.2×10-7,Ka2=5.6×10-11。室温下向10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液。如图是溶液中含碳元素微粒物质的量分数随pH降低而变化的图象(CO2因有逸出未画出).下列说法错误的是( )

A.A点所示溶液的c(H+)=5.6×10-11
B.B点所示溶液:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)=0.05mol/L
C.A点→B点发生反应的离子方程式为CO32-+H+=HCO3-
D.分步加入酚酞和甲基橙,用滴定法可测定Na2CO3与NaHCO3混合物的组成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com