
【题目】为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究:
(查阅资料)2KNO3![]() 2KNO2+O2↑ Fe(NO3)2
2KNO2+O2↑ Fe(NO3)2![]() FexOy+NO2↑+O2↑
FexOy+NO2↑+O2↑
实验一:探究Fe(NO3)2热分解固体产物中铁元素的价态。该小组甲同学将分解后的固体产物溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
(1)(提纯猜想)
猜想一:铁元素只显+2价;
猜想二:铁元素_____________;
猜想三:铁元素既有+2价又有+3价。
(实验操作)①向一份溶液中滴入KSCN溶液;向另一份溶液中滴入酸性KMnO4稀溶液。
(2)(实验现象)实验①_____________________;实验②____________________。
(3)(实验结论)猜想二成立,则Fe(NO3)2分解的化学方程式是_________________。
实验二:
(4)探究Fe(NO3)2热分解气体产物的性质。小组乙同学进行料如下实验,请完成实验空缺部分内容。限选试剂和用品:浓H2SO4溶液、4mol/LNaOH溶液、0.1mol/LBaCl2溶液、带火星的木条、0.1mol/L酸性KMnO4溶液、蒸馏水。
实验步骤 | 预期现象和结论 |
步骤1:取少量Fe(NO3)2固体于试管中,加热分解。 | ____________________________________,说明分解产生的气体中含有NO2。 |
步骤2:将产生的气体依次通过盛有足量_________________、浓硫酸的洗气瓶,______________________在最后一个出口检验。 | _____________________________________,说明分解产生的气体中含O2。 |
实验三:KNO3中混有Fe(NO3)2,为确定其中铁元素的含量,小组丙同学进行如下实验:①取混合物样品10g,充分加热分解;②将固体产物溶解、过滤,取沉淀进行洗涤、干燥,称得其质量为3.2g。则混合物中铁元素的质量分数为__________________。(保留三位有效数字,相对原子质量:Fe:56 O:16)
【答案】只显+3价 溶液出现血红色 溶液紫红色不褪色 4Fe(NO3)2![]() 2Fe2O3+8NO2↑+O2↑ 有红棕色气体产生 4mol/LNaOH溶液 用带火星的木条 带火星的木条复燃 22.4%
2Fe2O3+8NO2↑+O2↑ 有红棕色气体产生 4mol/LNaOH溶液 用带火星的木条 带火星的木条复燃 22.4%
【解析】
(1)根据两个已知的猜想推断,猜想二必为铁元素只显+3价;
(2)根据实验结论推断,Fe(NO3)2受热分解产生的固体产物只有Fe2O3,Fe2O3与足量稀硫酸反应生成Fe3+的溶液,则Fe3+遇KSCN溶液变红,不能使酸性高锰酸钾溶液褪色;
(3)设Fe2O3的系数为1,根据铁、氮、氧原子个数守恒配平,该反应为2Fe(NO3)2![]() Fe2O3+4NO2↑+1/2O2↑,系数加倍可得:4Fe(NO3)2
Fe2O3+4NO2↑+1/2O2↑,系数加倍可得:4Fe(NO3)2![]() 2Fe2O3+8NO2↑+O2↑;
2Fe2O3+8NO2↑+O2↑;
(4)Fe(NO3)2受热分解产生的气体产物中,NO2是红棕色气体,O2是无色无味气体,有红棕色气体产生,就能说明分解产生的气体中含有NO2;由于NO2有毒,且易与水反应产生能与O2反应的NO,因此步骤2中应该先用过量4mol/LNaOH溶液吸收多余的NO2,再用浓硫酸干燥,在最后一个出气口用带火星的木条检验,若带火星木条复燃,说明分解产生的气体中含有O2;
实验三:根据题意可知,产物中m(Fe2O3)=3.2g;根据铁元素守恒可得关系式,2Fe→Fe2O3,则原料中m(Fe)= m(Fe2O3)×2×56/160=3.2g×2×56/160;由于混合物总质量为10g,则其中有铁元素的质量分数为3.2g×2×56/160÷10g×100%=22.4%。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A.醋酸钠的水解反应 ![]() +H3O+=CH3COOH+ H2O
+H3O+=CH3COOH+ H2O
B.碳酸氢钙与过量的NaOH溶液反应Ca2++2![]() +2
+2![]() =CaCO3↓+ 2H2O+
=CaCO3↓+ 2H2O+ ![]()
C.苯酚钠溶液与二氧化碳反应 C6H5O—+ CO2+ H2O=C6H5OH+![]()
D.稀硝酸与过量的铁屑反应 3Fe+8H++2![]() =3Fe3++2NO↑+4 H2O
=3Fe3++2NO↑+4 H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,能够成立的是( )
CO(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,能够成立的是( )
A. 其他条件不变仅将容器的体积缩小一半,反应速率减小
B. 保持体积不变,充入少量He气体使体系压强增大,反应速率一定增大
C. 反应达平衡状态时:v(CO)正=v(H2O)逆
D. 其他条件不变,适当增加C(s)的质量会使反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一个电化学装置的示意图。
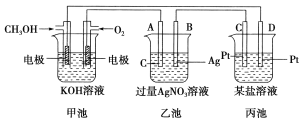
请回答下列问题:
(1)图中甲池是________(填“原电池”、“电解池”或“电镀池”)。
(2)A(石墨)电极的名称是________(填“正极”、“负极”、“阴极”或“阳极”)。
(3)写出通入CH3OH的电极的电极反应式:_________________________________。
(4)乙池中反应的化学方程式为______________________________________。
(5)当乙池中B(Ag)极质量增加5.4 g时,甲池中理论上消耗O2的体积为________L(标准状况),此时丙池中某电极析出1.6 g某金属,则丙池中的某盐溶液可能是________(填字母)。
A. MgSO4 B.CuSO4 C. NaCl D. AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴酸银(AgBrO3)的溶解度随温度变化曲线如图所示。下列说法正确的是( )
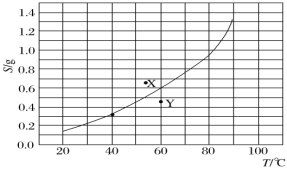
(注:X、Y点是图中所对应的质量的溴酸银放入100克水中,充分溶解后所得到的分散系)
A.溴酸银的溶解是一个熵增、焓减过程
B.对应温度下,X点的分散系中,v(溶解)>v(沉淀)
C.Y点的分散系中,c(Ag+)·c(BrO![]() )>6.25×10-4
)>6.25×10-4
D.60℃时溴酸银饱和溶液中c(BrO![]() )≈0.025mol·L-1
)≈0.025mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以CO2、H2为原料合成乙烯的方程式为:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。在常压下,按n(CO2)∶n(H2)=1∶3(总物质的量为4a mol)的投料比充入密闭容器中发生反应。测得温度对CO2的平衡转化率和催化剂催化效率影响情况如下图所示。
C2H4(g)+4H2O(g) ΔH。在常压下,按n(CO2)∶n(H2)=1∶3(总物质的量为4a mol)的投料比充入密闭容器中发生反应。测得温度对CO2的平衡转化率和催化剂催化效率影响情况如下图所示。
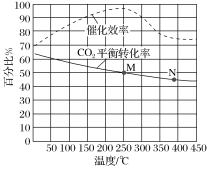
①下列说法不正确的是________。
A ΔH<0;平衡常数:KM<KN
B 改用其他催化剂,如果能加快反应速率,可能影响平衡转化率
C 若投料比改为n(CO2)∶n(H2)=3∶1,可以提高CO2的平衡转化率
D 250 ℃时,催化效率最高,但不是最佳反应温度
②250 ℃下,上述反应达平衡时容器体积为V L,则此温度下该反应的平衡常数为________(用含a、V的代数式表示)。
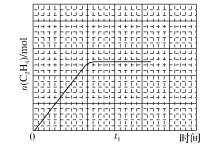
③某温度下,n(C2H4)随时间(t)的变化趋势曲线如图所示。其它条件相同时,若容器的体积为其一半,画出0~t1时刻n(C2H4)随时间(t)的变化趋势曲线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳在空气中燃烧后所得4.48 L(标准状况)的混合气体,组成为CO、CO2、N2(其他成分忽略),平均相对分子质量为30,与足量的灼热氧化铜反应,所得的气体质量增加了0.4 g:
(1)N2的体积________。
(2)原空气中O2、N2的体积比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从煤和石油中可以提炼化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平;B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
![]() 的电子式______,A的结构简式______。
的电子式______,A的结构简式______。
![]() 与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式_________,反应类型______。
与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式_________,反应类型______。
![]() 在碘水中加入B振荡静置后的现象______。
在碘水中加入B振荡静置后的现象______。
![]() 与浓硫酸与浓硝酸在
与浓硫酸与浓硝酸在![]() 反应的化学反应方程式_____________,反应类型______。
反应的化学反应方程式_____________,反应类型______。
![]() 等质量的A、B完全燃烧时消耗
等质量的A、B完全燃烧时消耗![]() 的物质的量______
的物质的量______![]() 填“
填“![]() ”或“
”或“![]() ”或“
”或“![]() ”
”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家制造出一种使用固态电解质的燃料电池,其效率更高,可用于航天航空。如图1所示装置中,以稀土金属材料作为惰性电极,在电极上分别通入CH4和空气,其中固态电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-(O2+4e-=2O2-)。
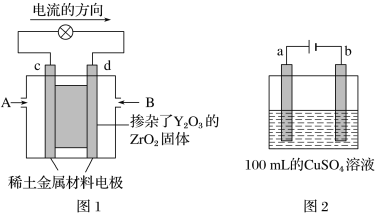
(1)c电极的名称为________(填“正极”或“负极”),d电极上的电极反应式为: ____。
(2)如图2所示用惰性电极电解100 mL 0.5 mol·L-1CuSO4溶液,a电极上的电极反应式为: __________,若a电极产生56 mL(标准状况)气体,则所得溶液的c(H+)=________(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入________(填字母)。
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com