
【题目】下列有机物分子中,不可能所有原子处于同一平面上的是:
A. CH2=CH2(乙烯) B. CH2=CH—CH3(丙烯)
C. 苯 D. 苯乙烯
【答案】B
【解析】
本题主要考查乙烯(六个原子共面)和苯(六个碳原子和六个氢原子共面)的结构问题。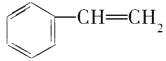 可看作由CH2=CH—代替苯分子中的氢原子[或
可看作由CH2=CH—代替苯分子中的氢原子[或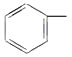 (苯基)代替乙烯中的氢原子],因碳碳单键可以旋转,故这两部分有可能在同一平面内。B项中的甲基(—CH3)为四面体结构,其中3个氢原子与碳原子一定不在同一平面内
(苯基)代替乙烯中的氢原子],因碳碳单键可以旋转,故这两部分有可能在同一平面内。B项中的甲基(—CH3)为四面体结构,其中3个氢原子与碳原子一定不在同一平面内
A. CH2=CH2平面结构,所有原子共面,故A不符合题意;B. CH2=CH—CH3甲基(—CH3)为四面体结构,其中3个氢原子与碳原子一定不在同一平面内,故B中所有原子不能共面,故B符合题意;C. 苯平面结构,所有原子共面。故C不符合题意;D. 苯乙烯可看作由CH2=CH—代替苯分子中的氢原子,它们各自组成中所有的原子都在同一平面内,故D所有原子共面,故D不符合题意。答案:B。


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示。
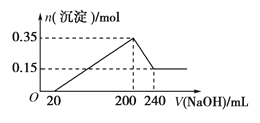
(1)加入NaOH 0~ 20mL 时发生反应离子方程式___________________,
加入NaOH 20~ 200mL 时发生反应离子方程式___________________,
加入NaOH 200~ 240mL 时发生反应离子方程式___________________,
(2)镁和铝的总质量为________g
(3)硫酸的物质的量浓度为___________ mol/L
(4)生成的氢气在标准状况下的体积为__________L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO4在水中的电离方程式为NaHSO4===Na++H++SO42-。某温度下,向c(H+)=1×10-6 mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1。下列对该溶液的叙述不正确的是
A. 该温度高于25℃
B. 由水电离出来的H+的浓度为1×10-10 mol·L-1
C. 加入NaHSO4晶体抑制了水的电离
D. 取该溶液加水稀释100倍,溶液中的c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)K2Cr2O7的水溶液中存在如下平衡:
Cr2O72-(aq)+ H2O(l)![]() 2CrO42-(aq)+ 2H+(aq),平衡常数表达式__________
2CrO42-(aq)+ 2H+(aq),平衡常数表达式__________
已知:(在水溶液中K2Cr2O7为橙红色,K2CrO4为黄色)往上述溶液中加入氢氧化钠,溶液呈___色;向已加入氢氧化钠的溶液中,再加入过量硫酸,溶液呈___________色。
(2)在KMnO4与H2C2O4反应中,可通过测定_________________来测定该反应的速率;写出酸性条件下KMnO4与H2C2O4(弱酸)反应,产生二氧化碳气体、水和Mn2+的离子反应方程式:__________________;此反应开始反应缓慢,随后反应迅速加快,其原因是______(填字母)
A.KMnO4溶液中的H+起催化作用
B.生成的CO2逸出,使生成物浓度降低
C.反应中,生成的Mn2+起催化作用
D.在酸性条件下KMnO4的氧化性增强
(3)为探讨化学反应速率的影响因素,设计的实验方案如下表。
(已知 I2+2S2O32-===S4O62-+2I-,其中Na2S2O3溶液均足量)
实验 序号 | 体积V/mL | 时间/s | |||
Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
①该实验进行的目的是_____________
②表中Vx=_______mL,比较t1、t2、t3大小____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,改变饱和氯水的pH,得到部分含氯微粒的物质的量分数与pH的关系如图所示。下列叙述不正确的是

A. 该温度下,HClO![]() H++ClO-的电离常数Ka的对值lgKa= -7.54
H++ClO-的电离常数Ka的对值lgKa= -7.54
B. 氯水中的Cl2、ClO-、HClO均能与KI发生反应
C. pH=1的氯水中,c(Cl2)>c(Cl3-)>c(HClO)>c(ClO-)
D. 已知常温下反应Cl2(aq)+Cl-(aq)![]() Cl3-(aq)的K=0.191,当pH增大时,K减小
Cl3-(aq)的K=0.191,当pH增大时,K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭恒容容器中,加入1molN2和3molH2发生反应:N2(g)+3H2(g)2NH3(g),下列叙述中能说明该反应达到平衡状态的是( )
A.![]() B.混合气体的密度保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变D.![]() :
:![]() :
:![]() :3:2
:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 用醋酸检验牙膏中的摩擦剂碳酸钙:CaCO3+2H+=Ca2++H2O+CO2↑
B. 漂白粉溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3-
C. 用氢氧化钠溶液除去镁粉中的铝:2Al+2OH-+2H2O===2AlO![]() +3H2↑
+3H2↑
D. Na2S溶液使酚酞试液变红:S2-+2H2O![]() 2OH-+H2S
2OH-+H2S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com