
����Ŀ��D��E��X��Y��Z�����ڱ��е�ǰ20��Ԫ�أ���ԭ��������������ǵ�����⻯����ӵĿռ�ṹ�������������塢�����Ρ�ֱ���Ρ������Ρ�ֱ���Σ��ش��������⣺
��1��E���⻯��ĵ���ʽΪ_____��D���⻯������м���Ϊ_____��Y���⻯��ĽṹʽΪ_____��X���⻯��е�_____Z���⻯��е㣨����ڡ����ڡ�����
��2��D��Y�γɵĻ��������ӵĵ���ʽΪ_____���ռ乹��Ϊ_____�Σ�Ϊ_____������ԡ��Ǽ��ԡ������ӡ�
��3��ȡ���������⻯���е����ֻ��ϣ�������һ�ֺ������Ӽ������ۼ�����λ���Ļ������д�����е�����һ�ֵĻ�ѧʽ_____��
���𰸡�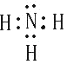 109��28�� H��S��H ����
109��28�� H��S��H ���� ![]() ֱ���� �Ǽ��� NH4Cl
ֱ���� �Ǽ��� NH4Cl
��������
D��E��X��Y��Z�Ƕ�����Ԫ�أ���ԭ���������������ǵ�����⻯����ӵĿռ�ṹ�������������塢�����Ρ�ֱ���Ρ������Ρ�ֱ���Σ��γ���������ṹ���⻯����CH4��SiH4���γ������͵��⻯����NH3��PH3���γ������ε��⻯����H2O��H2S���γ�ֱ���ͽṹ���⻯����HCl��HF���⼸��Ԫ�ص�ԭ����������������D���⻯����CH4��E���⻯����NH3��X���⻯����HF��Y���⻯����H2S��Z���⻯����HCl����D��E��X��Y��Z�ֱ���C��N��F��S��ClԪ�أ��Դ˽����⡣
D��E��X��Y��Z�Ƕ�����Ԫ�أ���ԭ���������������ǵ�����⻯����ӵĿռ�ṹ�������������塢�����Ρ�ֱ���Ρ������Ρ�ֱ���Σ��γ���������ṹ���⻯����CH4��SiH4���γ������͵��⻯����NH3��PH3���γ������ε��⻯����H2O��H2S���γ�ֱ���ͽṹ���⻯����HCl��HF���⼸��Ԫ�ص�ԭ����������������D���⻯����CH4��E���⻯����NH3��X���⻯����HF��Y���⻯����H2S��Z���⻯����HCl����D��E��X��Y��Z�ֱ���C��N��F��S��ClԪ�أ�
��1��E���⻯����NH3�������ĵ���ʽΪ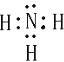 ��D���⻯����CH4������Ϊ109��28�䣬Y���⻯����H2S���ṹʽΪH��S��H��HF���Ӽ����������е�ϸߣ�
��D���⻯����CH4������Ϊ109��28�䣬Y���⻯����H2S���ṹʽΪH��S��H��HF���Ӽ����������е�ϸߣ�
�ʴ�Ϊ��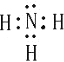 ��109��28�䣻H��S��H�����ڣ�
��109��28�䣻H��S��H�����ڣ�
��2��D��Y�γɵĻ�����ΪCS2������ʽΪ![]() ��Ϊֱ���η��ӣ��ṹ�Գƣ�Ϊ�Ǽ��Է��ӣ�
��Ϊֱ���η��ӣ��ṹ�Գƣ�Ϊ�Ǽ��Է��ӣ�
�ʴ�Ϊ��![]() ��ֱ���Σ��Ǽ��ԣ�
��ֱ���Σ��Ǽ��ԣ�
��3�����������⻯���е����ֻ��ϣ�������һ�ֺ������Ӽ������ۼ�����λ���Ļ������Ϊ��Σ���ΪNH4Cl�ȣ�
�ʴ�Ϊ��NH4Cl��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶���,��ij�ܱ������м���0.2 mol CO��0.2 mol H2O,������ӦCO��g��+H2O��g��![]() CO2��g��+H2��g��,4 minʱ��Ӧ�ﵽƽ��״̬,���n��CO����n��CO2��=3��2,����˵����ȷ����
CO2��g��+H2��g��,4 minʱ��Ӧ�ﵽƽ��״̬,���n��CO����n��CO2��=3��2,����˵����ȷ����
A.��С���������,���������ܶȲ���
B.v��CO��=v��CO2��ʱ,������Ӧ�ﵽƽ��״̬
C.ƽ��ʱCO��H2O��ת�������
D.������������·�Ӧ�Ļ�ѧƽ�ⳣ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�����������Ⱦ��������ǻ�����һ����Ҫ������
��1����N2��g��+O2��g���T2NO��g�� ��H1
��2C��s��+O2��g���T2CO��g�� ��H2
��C��s��+O2��g���TCO2��g�� ��H3
��2NO��g��+2CO��g��=N2��g��+2CO2��g����H=_______________���á�H1����H2����H3��ʾ����
��2����ҵ�ϳ��ô����������ͭ [Cu(NH3) 2] AC��Һ(ACΪCH3COO-)������ij�ϳ����е�CO���䷴ӦΪ��[Cu(NH3) 2] AC��aq��+NH3(g)+CO(g) ![]() [Cu(NH3)3] AC CO(aq) ��H<0��ѹ�£�������һ����̼����Һ�������»��[Cu(NH3) 2] AC��Һ�Ĵ�ʩ��________________��
[Cu(NH3)3] AC CO(aq) ��H<0��ѹ�£�������һ����̼����Һ�������»��[Cu(NH3) 2] AC��Һ�Ĵ�ʩ��________________��
��3������Ȼ����ȡH2����ԭ��Ϊ��CO2(g)��CH4(g) ![]() 2CO(g)��2H2(g) �����ܱ�������ͨ�����ʵ�����Ϊ0.1mol��CH4��CO2����һ�������·�����Ӧ��CH4��ƽ��ת�������¶ȼ�ѹǿ(��λPa)�Ĺ�ϵ��ͼ��ʾ��ѹǿP1_____P2���� �����ڡ���С�ڡ�����������____________________��ѹǿΪP2ʱ����Y�㣺v(��)_________v(��)������ڡ�����С�ڡ����ڡ�����
2CO(g)��2H2(g) �����ܱ�������ͨ�����ʵ�����Ϊ0.1mol��CH4��CO2����һ�������·�����Ӧ��CH4��ƽ��ת�������¶ȼ�ѹǿ(��λPa)�Ĺ�ϵ��ͼ��ʾ��ѹǿP1_____P2���� �����ڡ���С�ڡ�����������____________________��ѹǿΪP2ʱ����Y�㣺v(��)_________v(��)������ڡ�����С�ڡ����ڡ�����

��4��NOxҲ�ɱ�NaOH��Һ���ն�����NaNO3��NaNO2����֪ij�¶��£�HNO2�ĵ���ƽ�ⳣ��Ka=9.6��10��4��NaNO2��Һ�д���ƽ��NO2- +H2O![]() HNO2 +OH- ��ˮ��ƽ�ⳣ��Kh=5.0��10��11 ����¶���ˮ�����ӻ�����KW=______��
HNO2 +OH- ��ˮ��ƽ�ⳣ��Kh=5.0��10��11 ����¶���ˮ�����ӻ�����KW=______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)���������ڱ�������Ԫ�ذ��� ______________________(��Ԫ������)����Ԫ�أ�����Se�Ļ�̬ԭ�ӵĵ����Ų�ʽΪ______________________��Ԫ��X��Seͬ���ڣ�XԪ��ԭ�Ӻ���δ�ɶԵ�������࣬XΪ______________________(��Ԫ�ط���)��
(2)����ͬ���ڵ�����Ԫ���У���һ�������д�С��˳��______________________��
(3)�����ŷŵij�����Ҫ�ɷ�Ϊ3��MBT(3������2����ϩ���ṹ��ͼ)��1mol3��MBT�к���������ĿΪ____________(NAΪ����ӵ�������ֵ)���е㣺3��MBT____________(CH3)2C==CHCH2OH(������������������=��)����Ҫԭ����________________________��

(4)S��+4��+6���ּ�̬�������
�����й�����̬SO3��SO2��˵����ȷ����__________(�����)��
A.����ԭ�ӵļ۲���Ӷ��������
B.���Ǽ��Է���
C.����ԭ�ӵĺ˶Ե�����Ŀ�����
D.�����м��Լ�
��SO3���ӵĿռ乹��Ϊ__________�����以Ϊ�ȵ������������Ϊ__________(��һ��)��
(5)����Po����__________���γɵľ��壻����֪Po��Ħ������ΪMg��mol-1��ԭ�Ӱ뾶Ϊrpm�������ӵ�������ֵΪNA�����Ǿ�����ܶȵı���ʽΪ____________________g��cm-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܡ� ͭ���仯�����ڹ�ҵ������Ҫ��;�� �ش��������⣺
(1) �벹�����̬Co�ļ����Ų�ʽ�� [Ar]_________�� Co2+��_______��δ�ɶԵ��ӡ�
(2) Na3[Co(NO2)6]����������K+���Լ��� ��λ��NO2��������ԭ�ӵ��ӻ���ʽΪ________�� �ռ乹��Ϊ_____�����������÷���![]() ��ʾ�� ����m���������γɴ�������ԭ������ nΪ��ԭ�ӵĵ�������(�γ������ĵ��ӳ���)�͵õ��������ܺ� (�籽�����еĴ������ɱ�ʾΪ
��ʾ�� ����m���������γɴ�������ԭ������ nΪ��ԭ�ӵĵ�������(�γ������ĵ��ӳ���)�͵õ��������ܺ� (�籽�����еĴ������ɱ�ʾΪ![]() )����NO2���д�����Ӧ��ʾΪ____________��
)����NO2���д�����Ӧ��ʾΪ____________��
(3) �����[Cu(En)2]SO4��������������Ҷ�����ͭ(��)�� ��ͭ��һ����Ҫ��������� En ���Ҷ���(H2NCH2CH2NH2)�ļ�д��
�ٸ������[Cu(En)2]SO4��N�� O�� Cu�ĵ�һ��������С�����˳����______________��
���Ҷ��������װ�[N(CH3)3]�����ڰ��� ����Է������������ ���Ҷ��������װ��ķе�ߵö࣬ ԭ����______________________________________________________��

(4) ����Cu�����е�ԭ�Ӷѻ���ʽ��ͼ��ʾ�� ����λ��Ϊ______�� ͭ��ԭ�Ӱ뾶Ϊa nm�� �����ӵ�������ֵΪNA�� Cu���ܶ�Ϊ_________g/cm3(�г�����ʽ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����U��V��W��X���ֶ�����Ԫ�أ�ԭ���������������������Ϣ���±���

��ش��������⣺
��1��U��V����Ԫ����ɵ�һ�ֻ����������Ҫ�Ļ���ԭ�ϣ��������IJ�����Ϊ����ʯ�ͻ�����չˮƽ�ı�־��������������������ĸ�����Ϊ________��������ԭ�Ӳ�ȡ______�ӻ���
��2��V��Wԭ�ӽ���γɵ�V3W4���壬��Ӳ�ȱȽ��ʯ����V3W4�����к���________��������________���塣
��3���Һͱ��ֱ���V��X���⻯��������⻯������ж�����18�����ӡ��Һͱ��Ļ�ѧʽ�ֱ���________��____________�����߷е�Ĺ�ϵΪ����________��(����>������<��)��ԭ����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ڳ����£������������Ļ��Һ20 mL�������Һ�м���0.05 mol/L��Ba(OH)2ʱ�����ɵ�BaSO4�����������ͻ����Һ��pH����ͼ��ʾ��ϵ�����㣺

����������Һ���������������ʵ���Ũ�ȡ�_____________
��A����Һ��pHֵ��_________________
��2��ij�¶�ʱ��Ksp(AgCl)��c(Ag��)��c(Cl��)��1.8��10��10������
���ڸ�ij�¶�ʱAgCl���ܽ�ȣ�(![]() =1.34,�������һλ��Ч����)_______________
=1.34,�������һλ��Ч����)_______________
������������AgCl����ֱ�����100 mL H2O����100 mL 0.1 mol/L NaCl��Һ����100 mL 0.1 mol/L AlCl3��Һ����100 mL 0.1 mol/L MgCl2��Һ��������ܽ�ﵽƽ�⣬����ͬ�¶��£������Һ��Ag��Ũ���ɴ�С��˳��_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܼ��Ŵ�ʩ���ҹ���ʮһ�����ڼ���������ߴ�ʩ��
(1)ú��ȼ�գ�����������к����塣��úת��Ϊˮú��������Ч�����ŷš�
C(s)+O2(g)=CO2(g) ��H=��393.5 kJ��mol��1
H2(g)+ ![]() O2(g)=H2O(g) ��H=��242.0kJ��mol��1
O2(g)=H2O(g) ��H=��242.0kJ��mol��1
CO(g)+![]() O2(g)=CO2(g) ��H=��283.0kJ��mol��1
O2(g)=CO2(g) ��H=��283.0kJ��mol��1
�����������ݣ�д��C(s)��ˮ������Ӧ����CO��H2���Ȼ�ѧ����ʽ___________��
(2)����β�����ŷ��Ǵ�����Ⱦ�����Ҫ��Դ�����к���NO���塣����������ʾ�û���̿��ԭ�����Դ����������ij�x��С����̶��ݻ����ܱ������м���һ�����Ļ���̿��NO������ӦC(s)+2NO(g)![]() CO2(g)+N2(g) ��H=��574kJ��mol��1�������¶�Tʱ�����ⷴӦ�����Ƴ��±���
CO2(g)+N2(g) ��H=��574kJ��mol��1�������¶�Tʱ�����ⷴӦ�����Ƴ��±���

��0��10min�ڣ�NO��ƽ����Ӧ����v(NO)=___________mol��L��1��min��1��
���������ݲ��ٱ仯�ɱ�ʾ�÷�Ӧ�ﵽƽ�����___________��
a.������ѹǿ b����������ƽ��Ħ������ c�����������ܶ�
����������Ϊ�ɱ��ݻ���������ƽ���ı�ijһ������һ��ʱ���Ӧ�ٴδﵽԭƽ�⣬��д�����ܸı��������___________(��дһ��)��
(3)��ij�¶�Tʱ��ͬʱ������Ӧ��
2N2O5(g)![]() 2N2O4(g)+O2(g) K1
2N2O4(g)+O2(g) K1
N2O4(g)![]() 2NO2(g) K2
2NO2(g) K2
����һ����̶�Ϊ2L���ܱ������ڼ���N2O52mol��һ��ʱ��������ڵķ�Ӧ�ﵽƽ�⣬��ʱn(NO2)=0.4mol����֪K2=0.1��������K1=___________��
(4)һ�������£�������β��ͨ�뵽����������Һ��β���е������������ת��Ϊ�������ƣ���ҵ�Ͽ����������������Ʊ������ᡣ��֪��25��ʱ������(HNO2)��������(H2SO3)�ĵ���ƽ�ⳣ���ֱ����£�
Ka1 | Ka2 | |
�����ᣨHNO2�� | 7.1��10-4 | |
�����ᣨH2SO3�� | 1.54��10-2 | 1.02��10-7 |
��ش���������
�������£���0.1mol��L��1��������ϡ��100����c(H+)��___________(������������������������С��)��Kaֵ��(��������������������������С��)___________��
���������ӷ���ʽ�ܷ�������___________(����ĸ)��
a��NO2��+SO2+H2O=HNO2 +HSO3�� b�� 2HNO2+SO32��=2NO2��+SO2��+H2O
c��2NO2��+SO2 +H2O=2HNO2 +SO32�� d�� HNO2+SO32��= NO2��+ HSO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I����һ��������aA��bB![]() cC+dD�ﵽƽ��ʱ������д��
cC+dD�ﵽƽ��ʱ������д��
��1����A��B��C��D�������壬�ڼ�ѹ��ƽ�����淴Ӧ�����ƶ�����a��b��c��d��ϵ��__________________��
��2����֪B��C��D�����壬������A�����ʵ�����ƽ�ⲻ�ƶ���˵��A��__________________����״̬����
��3���������ݻ����䣬��������B������A��ת����__________________����������������С����������������
��4�������Ⱥ�C�İٷֺ�����С��������Ӧ��__________________��Ӧ��������������������������
��5������������ѹǿ���䣬��A��B��C��D�������壬�������г���ϡ�����壬��ѧƽ�������ƶ�����a��b��c��d��ϵ��__________________��
������ҵ��һ��������з�Ӧ�ϳɼ״���CO(g)��2H2(g) ![]() CH3OH(g)��
CH3OH(g)��
��1����һ���¶��£���2 mol CO��6 mol H2����2 L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c(CO)��0.5mol��L��1���÷�Ӧ��ƽ�ⳣ��K��__________________��
��2������һ����ɱ�������г���l molCO�� 2mol H2��1mol CH3OH���ﵽƽ�ⅼ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6������÷�Ӧ��__________________(����������������)��Ӧ�����ƶ���
��3�������¶Ⱥ��ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�˷�Ӧ���÷�Ӧ�ﵽƽ�ⅼ���й��������±���
���� | ��Ӧ��Ͷ����� | ��Ӧ���ת���� | CH3OH��Ũ��(mol/L) | �����仯��Q1��Q2��Q3������0�� |
1 | 2molCO��4molH2 | a1�� | c1 | �ų�Q1kJ���� |
2 | 2molCH3OH | a2�� | c2 | ����Q2kJ���� |
3 | 4molCO��8molH2 | a3�� | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ���� __________________��
A�� c1=c2 B��2Q1=Q3 C��2a1=a3 D��a1 +a2 =1 E���÷�Ӧ������2mol CH3OH����ų�(Q1+Q2)kJ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com