
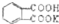 测定NaOH溶液的浓度.若每次都精确取用邻苯二甲酸氢钾为0.2040g.滴定终点时溶液的pH约为9.1(pH计测量),滴定时用酚酞做指示剂,用待测NaOH溶液滴定邻苯二甲酸氢钾,该生进行三次实验,每次消耗氢氧化钠溶液的体积如下表:
测定NaOH溶液的浓度.若每次都精确取用邻苯二甲酸氢钾为0.2040g.滴定终点时溶液的pH约为9.1(pH计测量),滴定时用酚酞做指示剂,用待测NaOH溶液滴定邻苯二甲酸氢钾,该生进行三次实验,每次消耗氢氧化钠溶液的体积如下表:| 实验编号 | 邻苯二甲酸氢钾质量(g) | 待测NaOH溶液体积(mL) |
| l | 0.2040 | 23.20 |
| 2 | 0.2040 | 19.95 |
| 3 | 0.2040 | 20.05 |
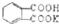 的式量为204.0,且1mol邻苯二甲酸氢钾能与1mol NaOH反应.
的式量为204.0,且1mol邻苯二甲酸氢钾能与1mol NaOH反应.| c(标准)V(标准) |
| V(待测) |
| 0.2040g |
| 204g/mol |
| 19.95+20.05 |
| 2 |
| 0.001mol |
| 0.02L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.6g铁粉在2.24L氯气中充分燃烧,失去的电子数一定为0.3NA |
| B、标准状况下,15g一氧化氮和5.6L氧气混合后的分子总数为0.5NA |
| C、在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA |
| D、78gNa2S和Na2O2的混合物中含有的离子总数大于3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol?L-1 |
| B、2.0 mol?L-1 |
| C、1.5.mol?L-1 |
| D、1.0 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
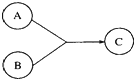 Ⅰ有机物A、B、C有如图所示转化关系,A的分子式为C3H4O2,A可与溴的四氯化碳溶液发生加成反应,1molA能与1molNaHCO3溶液恰好完全反应.B所含元素种类与A相同,是厨房的调味品,其中碳的质量分数为52.2%,氢的质量分数为13%.试回答下列问题,
Ⅰ有机物A、B、C有如图所示转化关系,A的分子式为C3H4O2,A可与溴的四氯化碳溶液发生加成反应,1molA能与1molNaHCO3溶液恰好完全反应.B所含元素种类与A相同,是厨房的调味品,其中碳的质量分数为52.2%,氢的质量分数为13%.试回答下列问题,
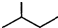 的名称为
的名称为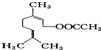
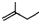
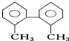 最多
最多查看答案和解析>>
科目:高中化学 来源: 题型:
| 第一份 | 第二份 | 第三份 | |
| 样品的质量/g | 7.54 | 15.08 | 35.00 |
| 二氧化硫的体积/L | 0.672 | 1.344 | 2.688 |
| 硫的质量/g | 0.80 | 1.60 | 3.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
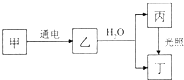 甲、乙、丙、丁4种物质均含A元素,其中甲的焰色反应呈黄色,乙为黄绿色气体单质,它们之间有如图所示的转化关系(转化过程中部分产物未标出).
甲、乙、丙、丁4种物质均含A元素,其中甲的焰色反应呈黄色,乙为黄绿色气体单质,它们之间有如图所示的转化关系(转化过程中部分产物未标出).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com