
����Ŀ����1��O��̬ԭ�Ӻ�������Ų�ʽΪ____��H2O VSEPRģ������Ϊ_____�����幹��Ϊ___��O3____���Է��ӣ�����������������������
��2�������Ȼ�ѧ�����ⶨ����������Born��Haber����������ģ���ʵ��������Hess���ɣ�����һ���Ȼ�ѧѭ����
��֪��Na(s)+ ![]() Cl2(g)= NaCl(s) ��H=��410.9 kJ��mol��1
Cl2(g)= NaCl(s) ��H=��410.9 kJ��mol��1
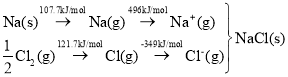
��֪��Naԭ�ӵĵ�һ������Ϊ_____kJ��mol��1��Cl-Cl������Ϊ______kJ��mol��1��NaCl������Ϊ_____kJ��mol��1��
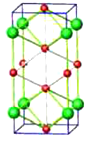
��3����ѹ��NaCl ����� Na �� Cl2 ��Ӧ�������γɲ�ͬ��ɡ���ͬ�ṹ�ľ��壬��ͼ������һ�־���ľ���������Ϊ��ԭ�ӣ� С��Ϊ��ԭ�ӣ����仯ѧʽΪ________��
��4������Na�����е�ԭ�Ӷѻ���ʽ��Ϊ���������ѻ�����������Ϊa nm���ռ�������Ϊ________���г�����ʽ����
���𰸡�1s22s22p4 �������� V�� �� 496 243.4 787.3 Na2Cl 
��������
(1)���ݺ���������Ų����۲���ӻ������ۺ��ӻ�������۷���������õȵ�����Ľṹ�ص�������
(2)��̬��̬Naԭ��ʧȥ1������ת��Ϊ��̬��̬��������Ҫ���������ΪNa�ĵ�һ�����ܣ�Cl-Cl���ļ��ܵ���1molCl2�γ� Cl(g)�����յ�������NaCl��������Na+��Cl-��̬�����γ�1molNaCl�����ͷŵ�������
(3)����һ�������и�ԭ�ӷֱ����⡢�ߡ�������ڱ������㻯ѧʽ��
(4)�ռ�������=������ԭ����ռ������뾧������ı�ֵ��
(1) Oԭ��Ϊ8��Ԫ�أ�����������Ų�ʽΪ��1s22s22p4��H2O��������ԭ�ӳɼ����Ӷ���Ϊ2���µ��Ӷ�����2���۵��Ӷ�����4����VSEPRģ������Ϊ�����壬���幹��ΪV�� ��O3��SO2�ǵȵ����壬SO2��ΪV�ͷ��ӣ�������������IJ��غϣ��Ǽ��Է��ӣ��ȵ�����Ľṹ���ƣ�O3�Ǽ��Է��ӣ�
(2)��̬��̬Naԭ��ʧȥ1������ת��Ϊ��̬��̬��������Ҫ���������ΪNa�ĵ�һ�����ܣ���Na�ĵ�һ������Ϊ496kJ/mol��ClC���ļ����ܵ���1molCl2�γ�Cl(g)�����յ���������ClCl����=2��121.7kJ/mol=243.4kJ/mol��NaCl��������Na+��Cl��̬�����γ�1molNaCl�����ͷŵ�������������H=E��-E������NaCl�ľ�����= E��-��H=(496+107+121.7-349) kJ/mol �C(��410.9 kJ��mol��1)=787.3kJ/mol��
(3)������4��Naԭ�������ϣ�2��Naԭ�������ģ�2��Naԭ���ھ����ڲ�������ԭ������=4��![]() +2��
+2��![]() +2=4��8��Clԭ�������ϣ�����ԭ�ӵ�����=8��
+2=4��8��Clԭ�������ϣ�����ԭ�ӵ�����=8��![]() =2����þ���Ļ�ѧʽΪNa2Cl��
=2����þ���Ļ�ѧʽΪNa2Cl��
(4)����Na�����е�ԭ�Ӷѻ���ʽ��Ϊ���������ѻ�����ѻ���ʽ��ͼ��ʾ��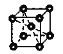 ����һ����������ԭ������=8��
����һ����������ԭ������=8��![]() +1=2����������Ϊa nm���������ΪV(����)= a3nm3�����ݾ���ͼʾ��������Խ��ߵij���=4r(Na)����r(Na)=
+1=2����������Ϊa nm���������ΪV(����)= a3nm3�����ݾ���ͼʾ��������Խ��ߵij���=4r(Na)����r(Na)=![]() nm��������ԭ�ӵ������=2��
nm��������ԭ�ӵ������=2��![]() �����ռ�������=
�����ռ�������= ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH3ClΪ��ɫ���Դ���ζ�����壬�ܶ�Ϊ2.25g/L���۵�Ϊ-24.2�����������Ҵ��ͱ������л��ܼ���
����ʵ������ȡCH3Cl��ԭ����CH3OH+HCl��Ũ��![]() CH3Cl+H2O��
CH3Cl+H2O��
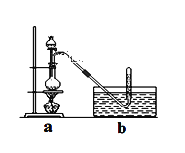
���岽�����£�������ZnCl2���壻����ȡ24g��ϸ����ˮZnCl2����ȡ20mLŨ�������Բ����ƿ��ͬʱ��ȡһ�����ļ״������Һ©���У�
������Һ©����ļ״���ε�����ƿ�в����ȣ���ZnCl2��ȫ�ܽ����CH3Cl�����ݳ���������ˮ���ռ���ش�
��1��ʵ���Ҹ���ZnCl2�����Ƶ���ˮZnCl2�ķ�����________________��
��2����Ӧ�����е�����ƿ�м״�������������٣��״���Ũ��������ʵ���Ũ�Ƚӽ�����������__________��
������ij���ϼ��أ�CH4�����е�һ��Hԭ�ӱ�Clԭ��ȡ�������ȶ����ܵ�Ӱ�죬�ɱ�ǿ���������Ը������������������ֻϴ��ƿ�ֱ�ʢ�������Լ���A��1.5%KMnO4��H+����Һ��B������ˮ��C��5%Na2SO3��Һ��D��98%H2SO4��
��1��Ϊ֤ʵ��һ���۵Ŀɿ��ԣ��������ѡ����ǡ����ϴ��ƿ����aװ�����ɵ���������ͨ��ϴ��ƿ____����ϴ��ƿ��ţ�������۲쵽_________��֤ʵ�������ϵ���ȷ�ԡ�
��2��д��ϴ��ƿ�з�����Ӧ�����ӷ���ʽ��CԪ�ص���������ΪCO2����______��
��3�����CH3Cl�Ǵ�������Ⱦ�����ϴ��ƿ֮��Ӧ��һֻʢ______��ϴ��ƿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1 mol/L CH3COOH��Һ��ˮϡ�ͻ��������CH3COONa����ʱ����������( )
A. ��Һ��pH����
B. CH3COOH���������
C. ��Һ�ĵ�����������
D. ��Һ��c(OH��)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ҫ�ɷ�ΪFeS2��Ϊԭ���Ʊ��Ȼ������壨FeCl3��6H2O���Ĺ����������£�
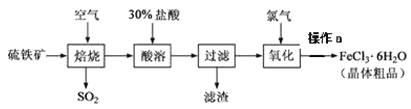
�ش��������⣺
��1����һ�������£�SO2ת��ΪSO3�ķ�ӦΪ2SO2��O2![]() 2SO3���÷�Ӧ��ƽ�ⳣ������ʽΪK��____��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ_________________��
2SO3���÷�Ӧ��ƽ�ⳣ������ʽΪK��____��������SO2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ_________________��
��2����36.5%���ܶ�Ϊ1.2g���M��3�������������500mL��30%���ܶ�Ϊ1.095g���M��3�����ᣬ���貣�������� ��___��
A�������� B���ձ� C��������ƽ D��500mL��Ͳ E��500mL����ƿ F����ͷ�ι�
��3�����ܼ����������о��豣�������������Ŀ����________________________��
________________________________________________________��
��4��ͨ��������ʱ����������Ҫ��Ӧ�����ӷ���ʽΪ_________________________���ù��̲�����β�����ü���Һ���գ�β������Ⱦ����������Ϊ________________��д��ѧʽ����
(5)����aΪ_________________________�����ˡ�ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦN2(g)+3H2(g) ![]() 2NH3(g) ��H<0�������о�Ŀ�ĺ�ʾ��ͼ������ǣ� ��
2NH3(g) ��H<0�������о�Ŀ�ĺ�ʾ��ͼ������ǣ� ��
A | B | C | D | |
�о�Ŀ�� | ѹǿ�Է�Ӧ��Ӱ�� ��p2��p1�� | �¶ȶԷ�Ӧ��Ӱ�� | ƽ����ϵ������N2��Ũ�ȶԷ�Ӧ��Ӱ�� | �����Է�Ӧ��Ӱ�� |
ʾ��ͼ |
|
|
|
|
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ����ȼ�ϵ��ԭ��ʾ��ͼ�����մ�ͼ����ʾ��������������ȷ���ǣ�������

A.a�缫�Ǹ���
B.b�缫�ĵ缫��ӦΪ��4OH--4e-====2H2O+O2��
C.����ȼ�ϵ����һ�־���Ӧ��ǰ������ɫ��Դ
D.����ȼ�ϵ����һ�ֲ���Ҫ����ԭ����������ȫ�������ڵ���ڵ����ͷ���װ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и��������һ���ܴ��������������Ϊ�� ��
A. ![]() ����Һ��:
����Һ��: ![]()
B. ��ˮ�������![]() ����Һ��:
����Һ��: ![]()
C. ![]() ����Һ��:
����Һ��: ![]()
D. ��ɫ��Һ��: ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡���ѧ���ļ������γ�(���)1mol��ѧ��ʱ�ͷ�(������)������������֪����(P4)��P4O6�ķ��ӽṹ��ͼ��ʾ��
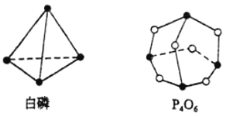
��֪��
��ѧ�� | P��P | P��O | O=O |
����(kJ��mol1) | 198 | 360 | 498 |
��ӦP4(g)+3O2(g)= P4O6(g)�ġ�H=_________��
(2)��֪��2C(s)+O2(g)=2CO(g) ��H=-221.0kJ/mol
��2H2(g)+O2(g)=2H2O(g) ��H=-483.6kJ/mol
���Ʊ�ˮú���ķ�ӦC(s)+H2O(g)=CO(g)+ H2(g)�ġ�H=_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ��ȷ�Ӧ��H2+Cl2![]() 2HCl������˵������ȷ���ǣ� ��
2HCl������˵������ȷ���ǣ� ��
A.�Ͽ�1molH��H����1molC1��C1�������յ������������γ�2molH��C1�����ų�����
B.���������е����������ڷ�Ӧ�������е�������
C.��Ӧ�������е����������ڲ��������е�������
D.�÷�Ӧ�У���ѧ��ֻת��Ϊ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com