
【题目】碳化钨(WC)是大型飞机发动机关键部位材料。
(1)基态钨原子的外围电子排布式为5d46s2,有___个未成对电子。
(2)在第二周期的非金属主族元素中,第一电离能由大到小顺序为___。
(3)硫氰化钾(KSCN)俗称玫瑰红酸钾,是铁离子的检验指示剂。
①SCN-中,中心原子碳的杂化类型是___,该离子的空间构型是___。
②SCN-的等电子体分子是___(任写一个)。
(4)C3H8和纯叠氮酸(HN3)的相对分子质量相近,但C3H8常温下是气态,而纯叠氮酸常温下是一种液体,沸点为308.8K,主要原因是___。
(5)NH3的键角是107°,NF3的键角是102.5°。NF3的键角比NH3的键角小,原因是___。
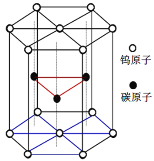
(6)碳化钨晶胞如图所示。①一个W原子与周围___个碳原子紧密相邻且等距。WC的熔点为2870℃,沸点是3000℃,硬度非常大,它的晶体类型是___。
②已知该晶胞边长为acm,高为hcm,NA为阿伏伽德罗常数。WC的摩尔质量为Mg·mol-1。该晶体密度为___g·cm-3。
【答案】4 F>N>O>C>B sp 直线型 CO2或SO2或N2O等 HN3分子间存在氢键,而C3H8分子间无氢键 氟原子含有较多的孤电子对,受到氮原子的一对孤电子对的斥力较大,故NF3的键角比NH3小 6 原子晶体 ![]()
【解析】
(1)根据价层电子排布分析末成对电子数;
(2)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,;
(3)①SCN-中,C的价层电子对=2+![]() =2;
=2;
②SCN-的一共有3个原子,价电子数有6+4+5+1(1个负电荷)=16个,由此找出等电子体;
(4)HN3分子间存在氢键;
(5)NF3的键角比NH3的键角小,原因是氟原子含有较多的孤电子对,受到氮原子的一对孤电子对的斥力较大;
(6)对照各类晶体的特征分析;根据ρ=![]() 计算。
计算。
(1)基态钨原子的外围电子排布式为5d46s2,5d4能级上4个电子末成对,有4个未成对电子。故答案为:4;
(2)同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,在第二周期的非金属主族元素中,第一电离能由大到小顺序为F>N>O>C>B。故答案为:F>N>O>C>B;
(3)①SCN-中,C的价层电子对=2+![]() =2,中心原子碳的杂化类型是sp,该离子的空间构型是直线型。故答案为:sp;;直线型
=2,中心原子碳的杂化类型是sp,该离子的空间构型是直线型。故答案为:sp;;直线型
②SCN-的一共有3个原子,价电子数有6+4+5+1(1个负电荷)=16个,直线型,用同族替换、价电子电荷迁移等方法得:SCN-的等电子体分子是CO2或SO2或N2O等(任写一个)。故答案为:CO2或SO2或N2O等;
(4)C3H8和纯叠氮酸(HN3)的相对分子质量相近,但C3H8常温下是气态,而纯叠氮酸常温下是一种液体,沸点为308.8K,主要原因是N原子电负性较大,HN3分子间存在氢键,而C3H8分子间无氢键。故答案为:HN3分子间存在氢键,而C3H8分子间无氢键;
(5)NH3的键角是107°,NF3的键角是102.5°。N的杂化方式均为sp3,NF3的键角比NH3的键角小,原因是氟原子含有较多的孤电子对,受到氮原子的一对孤电子对的斥力较大,故NF3的键角比NH3小。故答案为:氟原子含有较多的孤电子对,受到氮原子的一对孤电子对的斥力较大,故NF3的键角比NH3小;
(6)①碳化钨WC的熔点为2870℃,沸点是3000℃,硬度非常大,它的晶体类型是原子晶体。故答案为:6;原子晶体;
②已知该晶胞边长为acm,高为hcm,NA为阿伏伽德罗常数。WC的摩尔质量为Mg·mol-1。根据均摊法:晶胞中W:12×![]() +2×
+2×![]() =3,C:3,晶胞的质量为:
=3,C:3,晶胞的质量为:![]() g,晶胞的体积为:
g,晶胞的体积为:![]() ,根据ρ=
,根据ρ=![]() , 该晶体密度为ρ=
, 该晶体密度为ρ=![]() =
=![]() g·cm-3。故答案为:
g·cm-3。故答案为:![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时,用0.1molL-1NaOH溶液滴定20mL0.1molL-1CH3COOH溶液,溶液的pH随加入NaOH溶液体积的变化如图。下列说法不正确的是( )
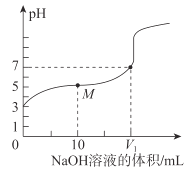
A.0.1molL-1CH3COOH溶液中,由水电离出的c(H+)<10-7molL-1
B.V1<20
C.M点溶液中离子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.二者等体积混合时,c(Na+)=c(CH3COO-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.铜和硝酸银溶液反应:Cu+Ag+=Cu2++Ag
B.铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
C.碳酸钙与稀盐酸反应:CO![]() +2H+=CO2↑+H2O
+2H+=CO2↑+H2O
D.硫酸钠溶液和氯化钡溶液反应:Ba2++SO![]() =BaSO4↓
=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,三种酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10-5 | K14.3×10-7 K25.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)一般情况下,当温度升高时,Ka__(填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是__(填序号);
a.CO![]() b.ClO-c.CH3COO-d.HCO
b.ClO-c.CH3COO-d.HCO![]()
(3)下列反应不能发生的是__(填序号)
a.CO![]() +CH3COOH=CH3COO-+CO2↑+H2O
+CH3COOH=CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO![]() +2HClO=CO2↑+H2O+2ClO-
+2HClO=CO2↑+H2O+2ClO-
d.2ClO-+CO2+H2O=CO![]() +2HClO
+2HClO
(4)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。

则HX的电离平衡常数__(填“大于”、“等于”或“小于”,下同)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)__醋酸溶液中水电离出来的c(H+),理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,在水中存在沉淀溶解平衡:CdS(s)![]() Cd2+(aq)+S2-(aq),其溶度积Ksp=c(Cd2+)·c(S2-),其在水中的沉淀溶解平衡曲线如图所示(T2>T1)。下列说法错误的是( )
Cd2+(aq)+S2-(aq),其溶度积Ksp=c(Cd2+)·c(S2-),其在水中的沉淀溶解平衡曲线如图所示(T2>T1)。下列说法错误的是( )
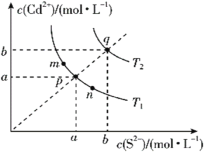
A.T1时CdS在c(S2-)=0.01mol/L的Na2S溶液中,c(Cd2+)=100a2mol/L
B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是( )
A.将装有NO2的玻璃球浸入热水中颜色加深:2NO2(g)![]() N2O4(g) ΔH>0
N2O4(g) ΔH>0
B.用Na2S处理含Hg2+废水:Hg2++S2-=HgS↓
C.Na2S2O3溶液与稀H2SO4混合产生浑浊:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O
D.闪锌矿(ZnS)经CuSO4溶液作用转变为铜蓝(CuS):ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀是应用电解原理在某些金属表面镀上一薄层其它金属或合金的方法。在铁质铆钉上镀镍(Ni)能防止铁被腐蚀,如图1。实验室模拟铁片镀镍,装置如图2。

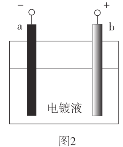
(1)b极材料是__。
(2)电镀液中含有NiSO4、NaCl和硼酸。
已知:NiSO4=Ni2++SO![]() 、Ni2++2H2ONi(OH)2+2H+
、Ni2++2H2ONi(OH)2+2H+
①a极的电极反应式是__。
②硼酸的作用是调节溶液的pH。pH较小时,a极易产生__气体,使镀层疏松多孔。pH较大时,a极会吸附__固体而使镀层含有杂质。
(3)铁质铆钉上镀镍能防止铁被腐蚀是因为镀层使铁与__等物质隔离。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种廉价的碳资源,资源化利用CO2具有重要的工业与环境意义。
(1)下列物质理论上可以作为CO2捕获剂的是____(填序号)。
A.NH4Cl溶液 B.(NH4)2CO3溶液 C.氨水 D.稀H2SO4
(2)以TiO2为催化剂的光热化学循环分解CO2反应为碳减排提供了一个新途径。该反应的机理及各分子化学键完全断裂时的能量变化如下图所示。
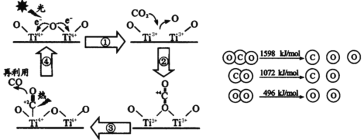
该转化过程①中会____能量(填“吸收”或“释放”);CO2分解反应的热化学方程式为______,实现该反应的能量转化方式是________。
(3)O2辅助的Al-CO2电池能有效利用CO2,且电池反应产物Al2(C2O4)。是重要的化工原料,工作原理如图所示。若正极上CO2还原生成C2O![]() ,则正极的反应式为___;电路中转移1 mol电子,需消耗CO2_____L(标准状况)。
,则正极的反应式为___;电路中转移1 mol电子,需消耗CO2_____L(标准状况)。
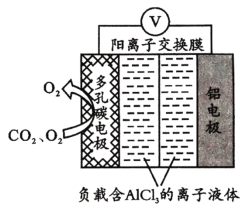
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质结构与性质下表为元素周期表的一部分。请回答下列问题:
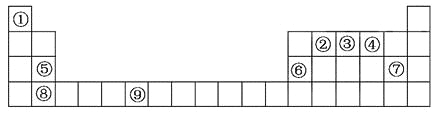
(1)上述元素中,属于s区的是_________(填元素符号)。
(2)写出元素⑨的基态原子的价电子排布图_______。
(3)元素的第一电离能:③______④(选填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为____;该分子为___分子(选填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_____________。
(5)元素⑥的单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。
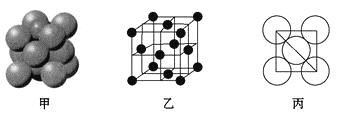
若已知⑥的原子半径为dcm,NA代表阿伏加德罗常数,元素⑥的相对原子质量为M,请回答:晶胞中⑥原子的配位数为____________,该晶体的密度为___________(用字母表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com