
����Ŀ��ijУ��ѧ��ȤС������ͼװ�ý���SO2��FeCl3��Һ�ķ�Ӧ 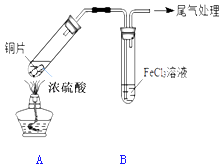
��1��д��װ��A�в���SO2�Ļ�ѧ����ʽ�� ��
��2����С��ͬѧ��ΪSO2��FeCl3��Һ�ܷ�����Ӧ�������� �� ��Ӧǰ��B����Һ����ɫ�仯Ϊ�� ��
��3�������������ʣ���Ԥ��FeCl3�����ܾ��е������ǣ��������ӷ���ʽ��ʾ����дһ�����ɣ� �� �����ʵ��֤�����Ԥ�⣨��ѡ���Լ���ʵ������������۽��б����� ��
���𰸡�
��1��Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O
CuSO4+SO2��+2H2O
��2��B���Ȼ�����Һ��ɫ�仯����dz��ɫ��Ϊdz��ɫ
��3��Fe3++3OH��=Fe��OH��3����ȡ������Һ�μ�����������Һ,�۲����ɺ��ɫ����
���������⣺��1��װ��A����ͭ��Ũ������ȷ�Ӧ��������ͭ�����������ˮ���Ʊ�����������ʽΪ��Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O��
CuSO4+SO2��+2H2O��
���Դ��ǣ�Cu+2H2SO4��Ũ�� ![]() . CuSO4+SO2��+2H2O����2��B����Һ�ɻ�ɫ��Ϊdz��ɫ��˵������������Ȼ�������������ԭ��Ӧ�����Դ��ǣ�B���Ȼ�����Һ��ɫ�仯����dz��ɫ��Ϊdz��ɫ����3���Ȼ������������ԣ�����֮�����Ӧ���ɺ��ɫ������������������Fe3++3OH��=Fe��OH��3������ȡ������Һ�μ�����������Һ���۲����ɺ��ɫ������
. CuSO4+SO2��+2H2O����2��B����Һ�ɻ�ɫ��Ϊdz��ɫ��˵������������Ȼ�������������ԭ��Ӧ�����Դ��ǣ�B���Ȼ�����Һ��ɫ�仯����dz��ɫ��Ϊdz��ɫ����3���Ȼ������������ԣ�����֮�����Ӧ���ɺ��ɫ������������������Fe3++3OH��=Fe��OH��3������ȡ������Һ�μ�����������Һ���۲����ɺ��ɫ������
���Դ��ǣ�Fe3++3OH��=Fe��OH��3����ȡ������Һ�μ�����������Һ���۲����ɺ��ɫ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.CHCl2���ӵ����幹��Ϊ����������
B.H2O��������ԭ�ӵ��ӻ��������Ϊsp2 �� ���ӵ����幹��ΪV��
C.CO2������̼ԭ�ӵ��ӻ��������Ϊsp�����ӵ����幹��Ϊֱ����
D.NH4+�����幹��Ϊ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����û�ѧ��Ӧԭ��֪ʶ�о��������CO��SO2����Ⱦ������Ҫ���壮
��1����CO���Ժϳɼ״�����֪��
CH3OH��g��+ ![]() O2��g���TCO2��g��+2H2O��l����H 1 kJmol��1
O2��g���TCO2��g��+2H2O��l����H 1 kJmol��1
CO��g��+ ![]() O2��g���TCO2��g����H2 kJmol��1
O2��g���TCO2��g����H2 kJmol��1
H2��g��+ ![]() O2��g���TH2O��l����H3 kJmol��1
O2��g���TH2O��l����H3 kJmol��1
��CO��g��+2H2��g��CH3OH��g����H=kJmol��1 ��
��2��һ��ѹǿ�£����ݻ�Ϊ2L���ܱ������г���1mol CO��2mol H2 �� �ڴ��������·�����Ӧ��CO��g��+2H2��g�� CH3OH��g����H��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ1��ʾ�� 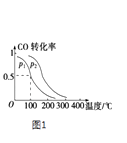
������˵����ȷ����
A���������������ܶȺ㶨����Ӧ�ﵽƽ��״̬
B���������ڸ�����Ũ�Ⱥ㶨����Ӧ�ﵽƽ��״̬
C��������Ӧ�У���H��0
D����Ӧ�У�����ʹƽ��������Ӧ�����ƶ�
��p2p1 ������ڡ�����С�ڡ����ڡ�����
��100��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=��
��3��ij����С����SO2Ϊԭ����ȡ���ᣮ
������ԭ���ԭ������SO2��O2��H2O���Ʊ����ᣬ�õ���ö�ײ������缫�������������壬ͬʱҲ��ʹ������������Һ��ֽӴ�����д���õ�ظ����ĵ缫��Ӧʽ�� ��
����Na2SO3��Һ�������SO2��NaHSO3��Һ��Ȼ�������Һ���Ƶ����ᣮ���ԭ��ʾ����ͼ2��ʾ����д����ʼʱ������Ӧ�ĵ缫��Ӧʽ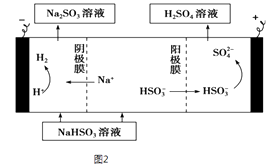
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijЩ��ѧ��Ӧ������ʽ��ʾ��A+B��C+D+H2O��ش��������⣺
��1����A��C��D��������Ԫ�أ���A�Ļ��ϼ۽���C��D֮�䣬д���÷�Ӧ�����ӷ���ʽ�� ��
��2����CΪ�Ȼ��ƣ�D��ʹ����ʯ��ˮ����ǵ���ζ���壬��A��B������ǣ��� ��
��3����AΪMnO2 �� BΪ���ᣬC�ǻ���ɫ�ĵ������壬д���÷�Ӧ�����ӷ��� ʽ ��
��4����AΪ���ʣ�BΪ���ᣬ��д��������ʽ�Ļ�ѧ����ʽ ��
��5����C��D��Ϊ�����Ҷ���ʹ����ʯ��ˮ����ǣ���D����ʹƷ����ɫ����A��B��Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��Ȼ�ѧ����ʽ��������ȷ�ĺ��ƣ� ��
A.��֪2H2O��l���T2H2��g��+O2��g����H=+571.6KJmol��1 �� ����H2��ȼ����
B.��֪C��ʯī��s��=C�����ʯ��s����H��0�����Ƚ϶��ߵ��ȶ���
C.��֪500�桢30MPa�£���0.5molN2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g�����ų�19.3KJ�����������Ƴ��÷�Ӧ���Ȼ�ѧ����ʽ
D.��֪2C��s��+2O2��g���T2CO2��g����H1��2C��s��+O2��g���T2CO��g����H2 �� ���ó���H2����H1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ԫ�����ڱ���һ���֣��ش���������
���� | IA | ��A | ��A | ��A | ��A | ��A | ��A |
1 | |||||||
2 | �� | �� | �� | ||||
3 | �� | �� | �� | ||||
��1������Ԫ�آ�����⻯��ĵ���ʽΪ �� Ԫ�آۺ͢ݶ�Ӧ���⻯����ȶ�������д��ѧʽ����ͬ����Ԫ�آں͢�Ӧ����������ˮ�������Խ�ǿ���� ��
��2����ҵ�������ʢܵ�ԭ�������û�ѧ����ʽ��ʾ����
��3����֪ijЩ��ͬ��Ԫ�ص�����Ҳ��һ���������ԣ���Ԫ�آ���Ԫ�آܵ��������������Ƶ����ʣ�д��Ԫ�آٵ�����������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ�� ��
��4��0.2mol�ĵ��ʢ���100mL2molL��1��FeBr2��Һ��Ӧ����������Fe2+��Br�������ʵ���֮���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����һ�ֺ���Ҫ�����Σ��й㷺����;�������ڽ���ʴ�̣���ˮ������ӡȾ��Ͳ�̻������ӹ�ҵ��·�弰ӫ������Ͳ�����ȣ��û�������غ�ɫ���׳��⣬100������ʱ������ijʵ��С�����һ��ʵ��װ�����Ʊ��������Ȼ������Իش� 
��1������A�����ƣ� ��
��2��ʵ��װ����ȷ������˳��I���������Ӣ�����װ�â�͢������÷ֱ����� ��
��3����μ������װ�õ������ԣ� ��
��4��װ�â����Լ�ƿ�е��Լ��ֱ������������ƣ���
��5��װ�â��з�Ӧ��ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������ң���Ҫ��Al��Al2O3��Fe2O3�ȣ���ȡ����������[Al��NO3��39H2O]���������£� 
����˵��������ǣ� ��
A.�Լ�Xѡ��ϡ���������
B.����Y����Ҫ�ɷ�ΪFe2O3
C.��ӦI �з����ķ�Ӧ֮һΪAl2O3+2OH��=2AlO2��+H2O
D.��ѹ�����ᾧ���ܸ�Ϊ��ѹ�����ᾧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�������ͼʵ��װ�ã���֤��������̼��ˮ�Ӵ�ʱ���ܺ������Ʒ�Ӧ���� 
��1������������ˮ��Ӧ�Ļ�ѧ����ʽ�� ��
��2��װ��I���Ʊ����������ѧʽ������װ��I�������˵��Լ������������ĸ���� a��ϡ���� b��ϡ���� c��С�մ� d��ʯ��ʯ
��3��ʵ��ʱ��Ӧ�ȴ��ɼ�K2 �� �ر�K1 �� �۲쵽Ԥ�������K1 �� �ٹر�K2 �� ʵ������н������ǵ�ľ������a�ڣ��۲쵽�����ǵ�ľ��ʼ�ղ���ȼ��
��Ϊ�۲쵽����ľ����ȼ�������ڢ��װһ��ʢ�м�ʯ�ҵĸ���ܣ�Ŀ������
������Ϊ��ʹ���ɼĽ��������չ۲쵽ľ����ȼ��Ҳ����֤��CO2�����˷�Ӧ��ԭ���� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com