
【题目】目前,从海水提取的溴占世界溴年产量的三分之一左右,空气吹出法是工业规模海水提溴的常用方法。其中一种工艺流程为:①海水浓缩,酸化;②通入Cl2,使Br— 转化为Br2;③通入空气、水蒸气,将Br2吹入吸收塔,与吸收剂SO2反应转化为HBr;④通入Cl2,再经过一系列处理得到产品Br2。请回答下列问题:
(1)步骤②、③操作的目的是_____(填“富集溴”或“萃取溴”);
(2)在步骤③中,生成HBr的化学方程式是___________;
(3)在步骤②中,若通入22.4LCl2(标准状况),理论上可得Br2__________g。
【答案】富集溴 SO2+Br2+2H2O= H2SO4+2 HBr 160
【解析】
①海水浓缩,酸化;②通入Cl2,使Br- 转化为Br2;③通入空气、水蒸气,将Br2吹入吸收塔,与吸收剂SO2反应转化为HBr;④通入Cl2,这主要是富集溴,再经过一系列处理得到产品Br2。
⑴步骤②、③操作的目的是富集溴;故答案为:富集溴。
⑵在步骤③中,生成HBr的化学方程式是SO2+Br2+2H2O= H2SO4+2 HBr;故答案为:SO2+Br2+2H2O= H2SO4+2 HBr。
⑶在步骤②中,若通入22.4LCl2(标准状况)即物质的量![]() ,根据方程式2Br-+Br2 = 2Cl-+Br2,理论上得到1mol Br2,质量为
,根据方程式2Br-+Br2 = 2Cl-+Br2,理论上得到1mol Br2,质量为![]() ;故答案为:160。
;故答案为:160。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于氯碱工业的说法中,正确的是( )
A.用离子交换膜法制烧碱可获得较纯净的产品,且不会对环境造成污染
B.总的离子方程式为2Cl-+2H2O=Cl2↑+2OH-+H2↑
C.当阳极附近有0.8mol NaOH生成时,导线中就有0.8mol电子通过
D.电解饱和食盐水可生产盐酸,也可以生产“84”消毒液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图:
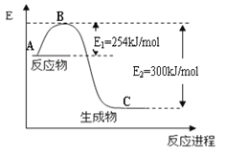
请写出NO2和CO反应的热化学方程式:___。
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g)+Q(Q>0),其化学平衡常数K与T的关系如下表:
2NH3(g)+Q(Q>0),其化学平衡常数K与T的关系如下表:
T/K | 298 | 398 | 498 | … |
K/ | 4.1×106 | K1 | K2 | … |
请完成下列问题:比较K1、K2的大小:K1___K2(填写“>”、“=”或“<”)
(3)判断该反应达到化学平衡状态的依据的是___(选填字母序号)。
A.2v(H2)正=3v(NH3)逆 B.2v(N2)正=v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。盐酸肼第一步水解反应的离子方程式___;
盐酸肼水溶液中离子浓度的排列顺序正确的是___(填序号)。
a.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
b.c(Cl-)>c([N2H5H2O]+)>c(H+)>c(OH-)
c.2c(N2H62+)+c([N2H5H2O]+)+c(H+)=c(Cl-)+c(OH-)
d.2c(N2H62+)+2c([N2H5H2O]+)+2c([N2H42H2O]=c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,能进行如图所示的多种反应。
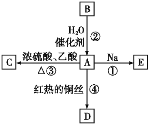
(1)A的官能团名称是_______________________,B的结构简式是________。
(2)反应②的反应类型为______________。
(3)写出反应③的化学方程式:_____________________。
(4)写出反应④的化学方程式:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)可用作火箭推进剂等。制备NH4ClO4的工艺流程如下:
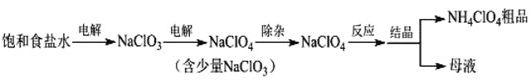
(1)电解NaClO3溶液时,ClO3-在____极发生反应,其电极反应式为____。
(2)“除杂”有两种方案。
①方案1:加入盐酸和H2O2溶液,NaClO3转化为ClO2,化学方程式为______。
方案2:加入氨水和FeCl24H2O,NaClO3转化为Cl-,离子方程式为____,如果FeCl24H2O过量会出现黑色磁性沉淀,该沉淀可能是______。(填化学式)
②比较氧化性:ClO3-_____ClO4-(填“>”或“<”)。
③两种方案相比,方案1的优点是____。(答一条即可)
(3)“反应”时用NaClO4和NH4Cl在90℃制备NH4ClO4。如果用浓盐酸和液氨代替NH4Cl,则无需加热,原因是____。
(4)该流程中可循环利用的物质是_________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以0.10mol/L的氢氧化钠溶液滴定同浓度某一元酸HA的滴定曲线如图所示(![]() )。下列表述错误的是( )
)。下列表述错误的是( )
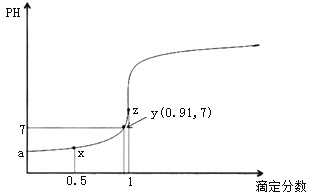
A.z点后存在某点,溶液中的水的电离程度和y点的相同
B.a约为3.5
C.z点处,![]()
D.x点处的溶液中离子满足:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】POCl3是重要的化工原料,某兴趣小组准备用三氯化磷、氯气、二氧化硫制备POC13,产物中还有一种遇水强烈水解的物质SOCl2,用下列装置完成实验。
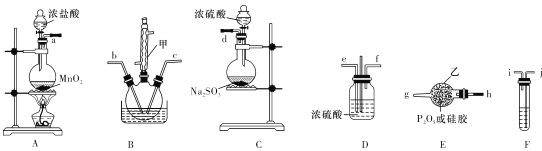
已知:PCl3熔点-93.6℃、沸点76.1℃,遇水强烈水解,易与氧气反应;POCl3遇水强烈水解,能溶于PCl3。
(1)仪器甲的名称是 ___。
(2)已知装置B制备POC13,以上仪器接口连接的顺序为a- ___b-c-g-h-d,装置F中所装试剂为 ___,装置B中发生反应的化学方程式为 ______.
(3)B中反应温度控制在60-- 65℃,其原因是 _____________
(4)用佛尔哈德法测定POC13含量:准确称取20. 20 g POCl3产品,置于盛有60. 00 ml蒸馏水的水解瓶中摇动至完全水解;将水解液配成100. 00 mL溶液,取10. 00 mL溶液于锥形瓶中;加入10. 00 mL3.200 mol/L AgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;加入指示剂,用0. 200 0 mol/L KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mLKSCN溶液。[已知:Ksp(AgCl) =3.2×10-10,Ksp(AgSCN) =2×10-12]
①滴定选用的指示剂是________:填字母代号),滴定终点的现象为____。
A.FeCl2 B.NH4Fe(SO4)2 C.淀粉 D.甲基橙
②用硝基苯覆盖沉淀的目的是____。
③产品中POC13的百分含量为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某二元碱X(OH)2水溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示,下列说法错误的是
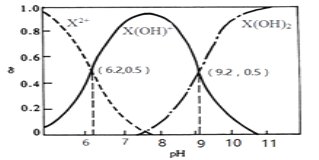
A.Kb2的数量级为10-8
B.X(OH)NO3水溶液显酸性
C.等物质的量的X(NO3)2和X(OH)NO3混合溶液中 c(X2+)>c[X(OH)+]
D.在X(OH)NO3水溶液中,c[X(OH)2]+c(OH-)= c(X2+)+ c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D为金属单质。(反应过程中生成的水及其他产物已略去)
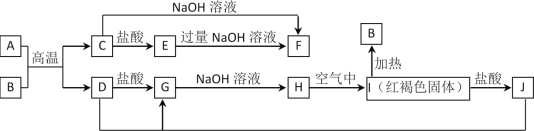
请回答以下问题:
(1)B是__________,H是_______________。(填化学式)
(2)写出J与D反应转化为G的离子方程式_________________________________。
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com