
【题目】下列关于氯碱工业的说法中,正确的是( )
A.用离子交换膜法制烧碱可获得较纯净的产品,且不会对环境造成污染
B.总的离子方程式为2Cl-+2H2O=Cl2↑+2OH-+H2↑
C.当阳极附近有0.8mol NaOH生成时,导线中就有0.8mol电子通过
D.电解饱和食盐水可生产盐酸,也可以生产“84”消毒液
科目:高中化学 来源: 题型:
【题目】超临界状态下的CO2流体溶解性与有机溶剂相似,可提取中药材的有效成分,工艺流程如下。
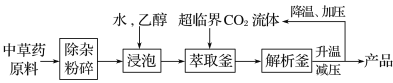
下列说法中错误的是( )
A.浸泡时加入乙醇有利于中草药有效成分的浸出
B.高温条件下更有利于超临界CO2流体萃取
C.升温、减压的目的是实现CO2与产品分离
D.超临界CO2流体萃取中药材具有无溶剂残留、绿色环保等优点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)=2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1。对此反应速率的表示,正确的是( )
A.用A表示的反应速率是0.4 mol·(L·min)-1
B.分别用B、C、D表示反应的速率,其比是3∶2∶1
C.在2 min末的反应速率,用B表示是0.3 mol·(L·min)-1
D.在这2 min内用B和C表示的平均反应速率的值相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g)ΔH<0,达到化学平衡状态,下列说法正确的是( )
2NH3(g)ΔH<0,达到化学平衡状态,下列说法正确的是( )
A.其他条件不变时,增大c(N2),H2的平衡转化率增大
B.其他条件不变时,降低温度,n(NH3)减小
C.其他条件不变时,增大压强,该反应的平衡常数增大
D.其他条件不变时,升高温度,该反应的化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙烯为主要原料,可以合成A、C、E等物质,其合成路线如图所示(部分反应条件、原料、产物已略去)。
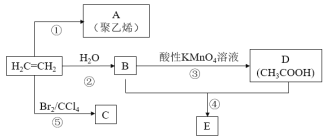
请回答下列问题:
(1)A的结构简式为______________。
(2)反应④的化学反应类型为___________________。
(3)反应⑤的化学方程式为_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积)。关于该固体混合物,下列说法正确的是

A. 一定含有Al,其质量为4.05g
B. 一定不含FeCl2,可能含有MgCl2和AlCl3
C. 一定含有MgCl2 和FeCl2
D. 一定含有(NH4)2SO4 和MgCl2,且物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液均为0.1mol·L-1,有关叙述正确的是( )
A.碳酸氢钠溶液中c(H2CO3)>c(CO32-)
B.碳酸钠溶液比碳酸氢钠溶液的pH小
C.碳酸钠溶液中c(OH-)=c(H+)+c(H2CO3)+c(CO32-)
D.碳酸钠溶液中滴加盐酸至pH=7,所得溶液的溶质只有NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要用480mL0.1molL-1的硫酸铜溶液,以下配制方法正确的是( )
A. 称取![]() 胆矾(CuSO4·5H2O),配成500mL溶液
胆矾(CuSO4·5H2O),配成500mL溶液
B. 称取![]() 胆矾(CuSO4·5H2O),加入500mL水配成溶液
胆矾(CuSO4·5H2O),加入500mL水配成溶液
C. 称取![]() 无水硫酸铜粉末,加入480mL水配成溶液
无水硫酸铜粉末,加入480mL水配成溶液
D. 称取![]() 无水硫酸铜粉末,加入500mL水配成溶液
无水硫酸铜粉末,加入500mL水配成溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,从海水提取的溴占世界溴年产量的三分之一左右,空气吹出法是工业规模海水提溴的常用方法。其中一种工艺流程为:①海水浓缩,酸化;②通入Cl2,使Br— 转化为Br2;③通入空气、水蒸气,将Br2吹入吸收塔,与吸收剂SO2反应转化为HBr;④通入Cl2,再经过一系列处理得到产品Br2。请回答下列问题:
(1)步骤②、③操作的目的是_____(填“富集溴”或“萃取溴”);
(2)在步骤③中,生成HBr的化学方程式是___________;
(3)在步骤②中,若通入22.4LCl2(标准状况),理论上可得Br2__________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com