
����Ŀ����ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g) +2H2(g)![]() CH3OH(g) ��
CH3OH(g) ��
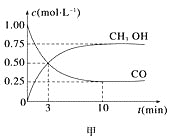

��1����ͼ�Ƿ�ӦʱCO��CH3OH(g)��Ũ����ʱ��仯������ӷ�Ӧ��ʼ��ƽ�⣬��COŨ�ȱ仯��ʾƽ����Ӧ����v(CO)=________molL-11min-1��
��2����ͼ��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯����Ӧ���ʱ���__________(������H<0��������H>0��)��Ӧ��д���÷�Ӧ���Ȼ�ѧ����ʽ��__________��
��3���÷�Ӧƽ�ⳣ��K�ı���ʽΪ____���¶����ߣ�ƽ�ⳣ��K________(��������������������������С��)��
��4�����д�ʩ�ܼӿ췴Ӧ���ʵ���__________��
A �����¶� B �����������ݻ� C �ٳ���0.1molCO D ��ʱ�����CH3OH
��5��������˵����Ӧ�ﵽƽ��״̬����__________��
A ��ϵѹǿ���ֲ��� B ����������������ֲ���
C H2��CO��Ũ����� D ÿ����1 mol CO��ͬʱ����1 mol CH3OH
���𰸡�0.075 ![]() <0 CO(g) +2H2(g)
<0 CO(g) +2H2(g)![]() CH3OH(g)
CH3OH(g) ![]() =-91 kJ/mol
=-91 kJ/mol 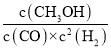 ��С AC A
��С AC A
��������
��1����ͼ��֪���÷�Ӧ��10min����ƽ��״̬���ʴӷ�Ӧ��ƽ��ʱ��v(CO)=![]() =
=![]() =0.075mol��L-1��min-1��
=0.075mol��L-1��min-1��
��2����ͼ�ҿ�֪����Ӧ�����������������������ߣ��ʸ÷�Ӧ����Ϊ���ȷ�Ӧ������Ӧ���ʱ�![]() <0����ͼ��֪���÷�Ӧ���ʱ�
<0����ͼ��֪���÷�Ӧ���ʱ�![]() =��419-510��kJ/mol=-91 kJ/mol���ʸ÷�Ӧ���Ȼ�ѧ����ʽΪ��CO(g) +2H2(g)
=��419-510��kJ/mol=-91 kJ/mol���ʸ÷�Ӧ���Ȼ�ѧ����ʽΪ��CO(g) +2H2(g)![]() CH3OH(g)
CH3OH(g) ![]() =-91 kJ/mol��
=-91 kJ/mol��
��3������ƽ�ⳣ������ʽ���壬д����ƽ�ⳣ��K=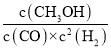 ���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�⽫�����ƶ���ƽ�ⳣ������С��
���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�⽫�����ƶ���ƽ�ⳣ������С��
��4��A�������¶��ܹ����ӻ�������Լ������Ч��ײƵ�ʣ���ѧ��Ӧ���ʼӿ죬�������⣻
B��������������������֮�����Ч��ײ���ʽ���С����ѧ��Ӧ���ʽ���С�����������⣻
C���ٳ���0.1molCO�������ڻ���������ӣ���Ч��ײ�������ӣ���ѧ��Ӧ���ʽ����������⣻
D����ʱ�����CH3OH��ʹ��Ӧ���ѹ��С����ѧ��Ӧ���ʽ���С�����������⣻
�ʴ�ΪAC��
��5��A�����º����£���������ʵ���֮����ѹǿ�����ȣ��÷�ӦΪ����ǵ������Ӧ��δ�ﵽƽ��ʱ�����������ʵ����ᷢ���仯����ѹǿҲ��仯������ϵ��ѹǿ���ֲ���ʱ����˵����Ӧ�ﵽƽ��״̬����A�������⣻
B���÷�Ӧ�����ʾ�Ϊ���壬���������غ��֪�ڷ�Ӧ�����У���������������ı䣬���������������䲻��˵����Ӧ�ﵽ��ƽ��״̬����B���������⣻
C��ƽ��ʱ��Ӧ��Ũ��������ʼŨ�Ⱥ�ת�����йأ���˵�H2��CO��Ũ�����ʱ����Ӧ��һ������ƽ��״̬����C���������⣻
D�����ݻ�ѧ��Ӧ����ת����ϵ��֪������ʱ��ÿ����1 mol CO��ͬʱһ��������1 mol CH3OH����D���������⣻
�ʴ�ΪA��


 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȩ������ͭ�������������£����Ա��������������ᡣ���ݴ�ԭ�����ʵ���Ƶò����Թ�C���ռ�������������Һ(��ͼ��ʾ���Թ�A��װ��40%����ȩˮ��Һ������ͭ��ĩ���ձ�B��װ��ijҺ��)����֪��60�桫80��ʱ��˫�����������������ɷ�����ȩ��������Ӧ����������ʮ���η�Ӧ������ȫ���й����ʵķе������
���� | ��ȩ | ���� | ���� | �Ҷ��� | ˮ |
�е�(��) | 20.8 | 117.9 | 290 | 197.2 | 100 |

��ش��������⣺
(1)�Թ�A����60����80��ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ_______________��
(2)��ͼ��ʾ��ʵ��IJ�ͬ�Σ���Ҫ�����¶ȼ����Թ�A�ڵ�λ�ã���ʵ�鿪ʼʱ�¶ȼ�ˮ�����λ��Ӧ���Թ�A�ķ�ӦҺ�У�Ŀ����___________�����Թ�A�ڵ���Ҫ��Ӧ��ɺ��¶ȼ�ˮ�����λ��Ӧ���Թ�A��֧�ܿڴ���Ŀ����_________��
(3)�ձ�B��������ʹ�Թ�A�ڵķ�ӦҺ�������ȷ�����Ӧ��ʹ���ɵ����������������Թ�C���ձ�B��ʢװ��Һ�������____��(д��һ�ּ��ɣ��������������)��ijͬѧ��Ϊ�Թ�C������ڱ�ˮԡ�У���Ŀ����________��
(4)��C�в�Ʒ��������ʱ��������ƿ�м�������___���Գ�ȥ���к��е�����ˮ��
A��Ũ���� B��CaO C��CuSO4��Һ D����ˮCaCl2
(5)�����������ᾫƷ�ʹ�Ʒ�ķ�������������_____��
A������ˮ�۲�ʵ������
B��������������������Һ���ټ���������Һ��ˮԡ���ȹ۲�ʵ������
C������̼��������Һ����۲�ʵ������
D����������Na���ʣ���۲�ʵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ���������ŵ�ش�ijЩ������������ȡ�������װ��

����˵������ȷ����( )
A.����װ���У�ʯīI��ʯī���������
B.��Ԫ����װ�â��б���ԭ����װ�â��б�����
C.װ�â١����еķ�Ӧ���ɵ�����I2ʱ��������ͨ���ĵ�����֮��Ϊ1��5
D.װ�â���MnO2�ĵ缫��ӦʽΪMnO2+2H2O+2e-=Mn2++4OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����۳����ںϳɻ����л����ԭ�ϣ�ijʵ��С����ڵ��۵�ˮ����������ºϳ�·�ߡ�
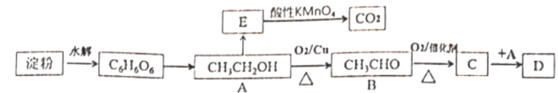
���У�E�����ϩ����D�Ǿ���ˮ����ζ�����ʡ�
(1) E�Ľṹ��ʽΪ_____
(2) C�еĹ�����������____
(3)д��A��B�Ļ�ѧ����ʽ___________�� ��Ӧ����Ϊ________
(4)д��C��D�Ļ�ѧ����ʽ___________����Ӧ����Ϊ_________
(5)Ҫ֤�������Ѿ�����ˮ�⣬ѡ��ļ����Լ���_____
(6) E��CO2��Ӧ�У�MnO![]() ����ԭΪMn2+��д����Ӧ�����ӷ���ʽ_______
����ԭΪMn2+��д����Ӧ�����ӷ���ʽ_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��WΪԭ������������������ֶ�����Ԫ�أ�����ZΪ����Ԫ�أ�X��WΪͬһ����Ԫ�ء�X��Z��W�γɵ����������ֱ�Ϊ�ס��ҡ�����x��y2��z��w�ֱ�ΪX��Y��Z��W�ĵ��ʣ����ǻ������ת����ϵ��ͼ��ʾ�������ж���ȷ���ǣ� ��
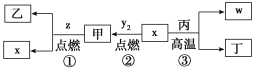
A.��Ӧ�١�������������ԭ��Ӧ�������ڷ�������ԭ��Ӧ
B.Y�����Ӱ뾶��Z�����Ӱ뾶С
C.��Ӧ�ۿ���֤��X�ķǽ�����ǿ��W
D.һ�������£�x���Ӧ���ɶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڼ��CO��ij�����������Ĺ���ԭ����ͼ��ʾ������˵������ȷ����

A.���������л�ѧ��ת��Ϊ����
B.����һ��ʱ�����Һ��pH��������
C.�缫I�Ϸ�����Ӧ��CO - 2e- + H2O = CO2 + 2H+
D.�缫II�Ϸ�����Ӧ��O2 + 2H2O + 4e- = 4OH![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������0.1mol��L-1��ˮ10mL��������ˮϡ�͵�1L�����б仯����ȷ����( )
�ٵ���̶������[NH3��H2O]�����![]() ��Ŀ�����[OH-]����ݵ�������ǿ��
��Ŀ�����[OH-]����ݵ�������ǿ��![]() �����
�����![]() ��С
��С
A.�٢ڢ�B.�٢ۢ�C.�٢ۢ�D.�ڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬ�¶��£����������Ϊ1L���ܱ������з�����Ӧ��CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ��H=-867 kJ.mol-1��ʵ������ʼ��ƽ��ʱ���й��������������˵����ȷ����
N2(g)+CO2(g)+2H2O(g) ��H=-867 kJ.mol-1��ʵ������ʼ��ƽ��ʱ���й��������������˵����ȷ����
������� | �¶�/K | ��ʼ���ʵ���/mol | ƽ�����ʵ���/mol | ||||
CH4 | NO2 | N2 | CO2 | H2O | NO2 | ||
I | T1 | 0.50 | 1.2 | 0 | 0 | 0 | 0.40 |
II | T2 | 0.30 | 0.80 | 0.20 | 0.20 | 0.40 | 0.60 |
III | T3 | 0.40 | 0.70 | 0.70 | 0.70 | 1.0 | |
A.T1<T2
B.�������¶ȣ�����Ӧ���ʼ�С���淴Ӧ��������ƽ������
C.ƽ��ʱ������I�з�Ӧ�ų�������Ϊ693.6 kJ
D.����III�з�Ӧ��ʼʱv ��(CH4) <v��(CH4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ͬ���칹����Ŀ���жϣ���ȷ����
A.���飨C4H10)�Ķ��ȴ�����10��
B.����ʽΪC4H8��ϩ������˳���칹�干5��
C.����![]() ������һ����ԭ�ӱ�����(-C4H9)��ȡ����ͬ���칹�壨�����������칹����8��
������һ����ԭ�ӱ�����(-C4H9)��ȡ����ͬ���칹�壨�����������칹����8��
D.����ʽΪC5H12O�Ĵ���4��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com