


科目:高中化学 来源: 题型:
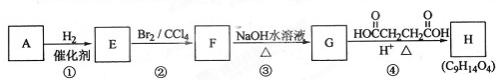
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 结构、性质信息 |
| X | 最外层电子数等于次外层电子数 |
| Y | 单质在常温下是固体,基态原子的M层上有1个未成对的p电子 |
| Z | 元素正三价离子的3d能级为半充满 |
| W | 元素基态原子的M层全充满,N层只有一个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(HA)>c(HB) |
| B、c(A-)>c(B-) |
| C、c(H+)>c(OH-) |
| D、c(A-)+c(B-)>c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阳极产生H2 |
| B、阳极产生O2 |
| C、阴产生Li和H2 |
| D、阴极只产生H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
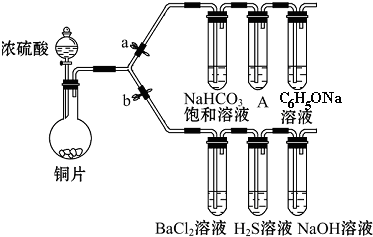
查看答案和解析>>
科目:高中化学 来源: 题型:
 T℃时,容积固定为1L的密闭容器甲中充入2molSO2、1molO2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,维持温度为T℃,4min后达到平衡,测得平衡时n(SO3)=1.2mol.
T℃时,容积固定为1L的密闭容器甲中充入2molSO2、1molO2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,维持温度为T℃,4min后达到平衡,测得平衡时n(SO3)=1.2mol.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| B、用燃烧法检验衣服面料是羊毛还是化学纤维 |
| C、用分液法分离水和油 |
| D、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com